▎药明康德内容团队报道
3月24日消息,因明生物宣布其下属企业誉颜制药研发的注射用重组A型肉毒毒素临床试验申请已获得中国国家药品监督管理局药品审评中心(CDE)批准,即将在中国开展以改善中度至重度眉间纹为适应症的药物临床试验。

因明生物成立于2019年,该公司已建立一条包括10余种在研药物的产品管线,涵盖眼科药物、重组蛋白肉毒素、小分子免疫药物及细胞治疗等领域。该公司开发的眼科新药
QA102
、QA108,HKP1小分子抑制剂
PRJ1-3024
、新型CAR-T细胞治疗产品
XYF19
均已在临床开发中。
本次获批临床的注射用重组A型肉毒毒素是因明生物的核心产品之一,研发代号为YY001
。
公开资料显示,肉毒毒素是厌氧梭状芽孢杆菌产生的神经毒素,根据抗原性不同可分为A、B、C、D、E、F、G等7型,其中A型毒性最强。
A型肉毒毒素产生高活性的作用原理已得到深入的研究并获得普遍的共识,也是临床应用最广泛的肉毒毒素。目前已上市的A型肉毒毒素的产品都来自致病性肉毒杆菌,安全生产风险较高。此外,绝大多数A型肉毒毒素产品都有活性蛋白纯度低的缺陷。

根据因明生物官网资料,该公司
创新性设计的YY001是一款重组A型肉毒毒素,它不仅表达了与天然A型肉毒素结构完全一致的高纯度毒素蛋白,同时满足了提高纯度和安全生产的需求。
而高纯度也保证了重组蛋白具有高蛋白比活性,因此临床治疗时使用的蛋白量更少,安全性更高。
据悉,临床前药效学和毒理学的研究已验证了这种重组蛋白的功效,并提供了完整的安全性数据,这些研究支撑了YY001临床试验方案在安全性和有效性方面的设计。本次YY001获批临床也意味着因明生物肉毒毒素项目管线迎来了首个进入临床的在研产品。
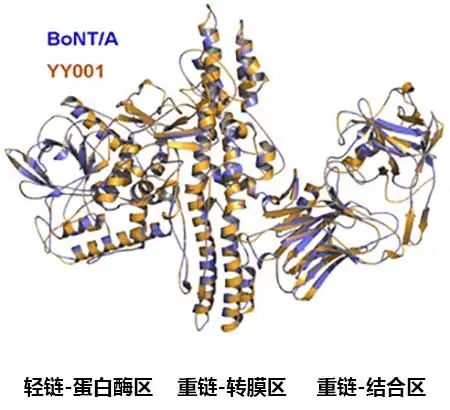
▲YY001与天然A型肉毒毒素分子立体结构的同源模拟分析
(图片来源:参考资料[1])
誉颜制药首席科学官杨武博士
在新闻稿中表示,通过全新的重组蛋白的技术路线生产肉毒毒素可以显著降低安全风险、并大幅提高产品纯度。这条新技术路线是极为复杂的系统工程,门槛极高、难度极大。在过去的几十年里,全球仅有极个别的海外公司实现了重组蛋白肉毒毒素的生产。誉颜制药通过自主创新,在科学、技术、工程、生产和管理等领域实现了全面的突破。
因明生物首席运营官、誉颜制药董事长兼CEO刘淼先生表示,誉颜制药自主创新研发生产的新一代重组A型肉毒毒素是因明生物旗下重要的管线产品。公司将全力推进注射用重组A型肉毒素的临床试验工作,并积极探索更多的适应症,为人类的健康做出贡献。
参考资料:
[1]因明生物官网。From https://www.ming-med.com/yimeimed/
本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈。转发授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。







 个人中心
个人中心
 我是园区
我是园区




