



汉肽生物医药集团有限公司
12月北京前途汇年会期间
汉肽生物医药集团有限公司是一家专注于合成生物学技术开发的高新技术企业, 主要从事于新型基因重组多肽药物的设计、生产和销售。
公司在山东、天津、江苏拥有6千余平方米的科研中心,山东淄博高青和江苏连云港的生产基地占地8万平方米。拥有以海归及国内领军人物组成的一流研发团队,搭建完成了基因编辑、酶工程、多肽高通量合成及质量管理与控制实验室。以药物的合理设计为基础,结合先进的合成生物学技术,实现基因重组多肽药物、新型抗体药物及活性小分子化合物的 “绿色智造” 。
我们以先进技术在制药行业的应用为基础,实现新型生物医药的绿色生产,为人民的健康护航。
目前公司有技术研发人员40多人,下设“一院两中心两生产基地”:山东大学-汉肽生物研究院、医药研发中心(山东汉肽生物医药有限公司淄博分公司)和医美产品开发中心(山东汉肽医美生物科技有限公司)以及高青生产基地和江苏东海生产基地。



汉肽生物医药集团有限公司与山东大学本着“优势互补、互惠互利、服务地方、共同发展”的原则,就产学研长期合作及共建“山东大学-汉肽生物技术研究院”达成协议,在研究院的框架下实现资源共享、开展合作研究。
以汉肽生物研发中心为技术依托和纽带,山东大学-汉肽生物技术研究院将整合汉肽生物与山东大学的人才、技术、产业、市场、资金等资源和众多医疗科研平台优势,围绕创新药设计与筛选技术进行合作研发。
研究院研发方向主要包括免疫调节创新药、治疗多药耐药菌感染的创新药、GLP-1类创新药等的开发;围绕抗衰老产品的设计和应用进行合作研发,主要包括防止皮肤衰老的外用产品和防止人体机能衰老的保健类食品及药品的开发,共同为推进全民健康事业而贡献力量。



汉肽生物基于新型合成生物学平台的GLP-1类似物研发在2020年初取得了关键性的技术突破,并打通了从蛋白合成到多肽收获的工艺路线。该技术在国内属于首创,此前,一直为国外所垄断。拥有该技术以后,GLP-1类药物的国产化变得非常容易实现。
而且可以预期的是,该技术能带动一大批GLP-1类小分子重组多肽一类创新药物的涌现。尤其是在目前国际形势巨变的前提下,该技术对于我国生物医药产业及人民健康安全带来的保障不可估量。
糖尿病是影响我国居民健康的一类重大疾病。糖尿病是常见病、多发病,目前在全球范围内,糖尿病的患病率和发病率急剧攀升。根据国际糖尿病联盟(IDF)2017年的统计数据显示:全球糖尿病成人患者约有4.25亿,中国20~79岁人群中糖尿病患者约有1.144亿,居世界首位。
胰高血糖素样肽-1(GLP-1)是人体肠道L细胞分泌的一种肽类激素,能够刺激β细胞的增殖和分化,促进胰岛素分泌。这一过程是葡萄糖依赖性的,其效应的强弱和葡萄糖浓度有关。血糖浓度越高,其活性越强,血糖浓度越低其活性越弱甚至失去活性。因而不会产生低血糖等副作用,号称智能型降血糖药,这也是最近GLP-1类药物销售份额超过胰岛素类药物的原因所在。此外GLP-1受体激动剂在降血糖的同时还有额外的心血管收益,可以减少食物摄取并延缓胃排空,有明显的减肥控制体重作用。
目前国内市场的GLP-1类药物依旧被诺和诺德等外国医药企业独占。国内也有一些制药公司尝试过或者正在进行该类药物的研发,但是这几年来并未见到太重大的技术突破。
重组技术生产多肽或者蛋白质存在一个问题就是对于分子量大的蛋白产量还不错,但是对于只有几十个氨基酸的短肽来说,效率非常低下以至于没有工业价值。
在前期,国内一些医药研发企业开始把多肽固相合成技术引入到GLP-1类药物的生产中来。不过这种技术说到底还是化学合成技术,和原研厂家的生产技术完全不一致,很难通过药审中心的技术评定。
化学合成技术带来的氨基酸消旋问题使得最终产品中可能存在D型氨基酸杂质带来的旋光异构体。给后期杂质的清除带来的非常严重的困难。
目前也有厂家开始进行诸如大肠杆菌系统的重组蛋白研发,但是存在诸如内毒素杂质问题,收率问题,纯化问题等各种问题,导致没有太大的起色。
注射用利拉鲁肽(商品名Victoza/Saxenda等)原研公司为诺和诺德,由Novo Nordisk 1996年开始研发,2009年于丹麦上市,随后于2009年6月与2010年1月分别获得EMA与FDA批准,用于治疗2型糖尿病,商品名Victoza。
①工程菌构建和筛选:
所用工程菌:芽孢杆菌HTBV-02
载体:pHTN3-1
融合基因:融合蛋白+利拉鲁肽(LG)主链
通过转化筛选到多个阳性转化子,选择其中产量较高的一个作为生产菌株保存,己建立种子库并进行传代稳定性考察。
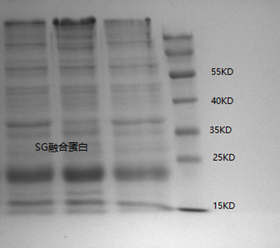
②融合蛋白发酵产量检测:
融合蛋白大小约20KD,切下的LG主链大小约为3.4KD。
目前摇瓶发酵产量一般在0.5g/L左右,发酵罐产量与摇瓶相比较低,目前正在优化条件。

③亲和层析:
发酵液中的融合蛋白采用镍柱亲和层析,目前收率达到90%以上,流穿液与洗杂液SDS-PAGE未检测到融合蛋白。
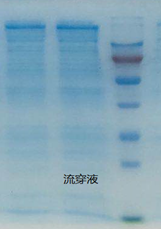
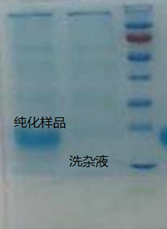
④酶切后纯化及冻干:
酶切后的样品经过反相纯化得到利拉鲁肽主链,再进行旋蒸浓缩,得到的样品检测后可进行下一步酰化修饰。

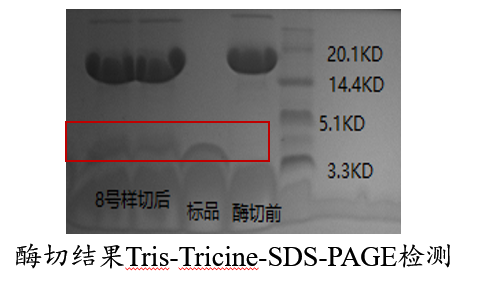
⑤酶切结果检测:
融合蛋白酶切后进行Tris-Tricine-SDS-PAGE检测和液相检测,液相检测显示酶切产物与LG主链标品在同一位置出峰。
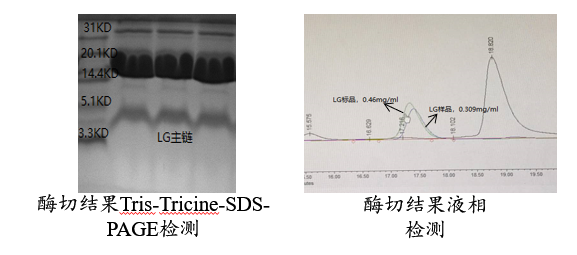
⑥项目周期:
构建工程菌株
筛选高表达工程菌株
建立菌株种子库
完成建库的各项检测和检定
发酵工艺和小试纯化工艺开发
建立稳定的原料药小试制备和制剂小试工艺
完成样品的制备、初步的稳定性考察项目
完成原料药和制剂中试工艺验证
进行药物稳定性、毒理研究
完成新药临床注册资料的研究
完成临床试验
同时完成生产车间的建设
申报生产

注射用索马鲁肽(商品名为OZEMPIC®、Rybelsus等)原研公司为诺和诺德,规格为1.5ml(相当于2mg索马鲁肽)。2017年12月5日,注射形式的索马鲁肽获得美国药监局FDA批准,用于辅助饮食控制和运动以有效控制2型糖尿病患者的血糖。2019年9月20日,美国药监局FDA批准口服形式的索马鲁肽正式上市,其适应症和注射形式的索马鲁肽是一致的,都是用于控制2型糖尿病患者的血糖。
①工程菌构建和筛选:
所用工程菌:芽孢杆菌HTBV-02
载体:pHTN3-1
融合基因:融合蛋白+索马鲁肽(SG)主链
通过转化筛选到多个阳性转化子,选择其中产量较高的一个作为生产菌株保存,己建立种子库,正在进行传代稳定性考察。
②融合蛋白发酵产量检测:
目前摇瓶发酵产量一般在0.5g/L左右。
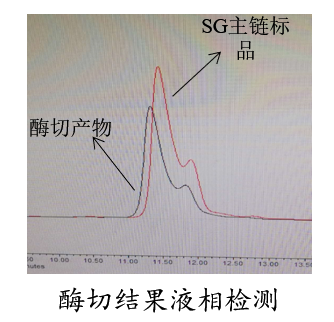
③酶切结果检测:
融合蛋白酶切后进行Tris-Tricine-SDS-PAGE检测和液相检测,液相检测显示酶切产物与SG主链标品在同一位置出峰。
④项目周期:
构建工程菌株
筛选高表达工程菌株
建立菌株种子库
完成建库的各项检测和检定
发酵工艺和小试纯化工艺开发
建立稳定的原料药小试制备和制剂小试工艺
完成样品的制备、初步的稳定性考察项目
完成原料药和制剂中试工艺验证
进行药物稳定性、毒理研究
完成新药临床注册资料的研究
完成临床试验
同时完成生产车间的建设
申报生产
我们综合考虑了现有重组多肽表达平台的优劣,创新性地发展了比原研厂家更为优秀的第三代基于合成生物学的小分子多肽生物合成平台。
我们利用最先进的生物学技术对工程菌株的代谢途径进行了合理的优化,该表达体系只需要无机盐培养基就可以实现GLP-1类化合物的分泌表达。
由于培养基不含诸如蛋白胨等有机物成分,使得我们的最终产品易于纯化且杂质含量极低,不含内毒素,其质量甚至超过了原研厂家的水平。
利用该平台,我们不仅进行了诸如利拉鲁肽、索马鲁肽等仿制药的开发,而且进行了多种创新药物的研发。
我们的一系列产品从仿制药到创新药,从保健品到药物开发;布局合理,形成了中端到高端的梯队。
相信随着我们这次的技术重大突破,我们首先会迅速完成几个重磅GLP-1仿制药的申报,并迅速完成一类创新药的开发布局,成为第一个完成GLP-1国产化并完成me-too而且me-better的医药研发公司。
李燕:13681171770(微信同号)

识别二维码添加微信好友

1.
2.
3.
4.
5.
6.
7.
8.





 点击“阅读原文”查看2020年线下会议安排!
点击“阅读原文”查看2020年线下会议安排!



 个人中心
个人中心
 我是园区
我是园区




