▎药明康德内容团队编辑
今日,CRISPR Therapeutics公司宣布,利用CRISPR基因编辑技术改造的同种异体CAR-T细胞疗法CTX110,在治疗CD19阳性B细胞癌症的1期临床试验中获得积极安全性和疗效结果。初步结果显示,在大B细胞淋巴瘤患者中,较高剂量的CTX110单剂治疗达到58%的总缓解率和38%的完全缓解率。

CTX110是一款利用CRISPR基因编辑技术制造的同种异体CAR-T细胞疗法
。它将靶向CD19抗原的嵌合抗原受体(CAR)定位敲入细胞的天然T细胞受体位点,在引入CAR的同时防止内源性TCR的表达,从而防止移植物抗宿主病(GvHD)的产生。
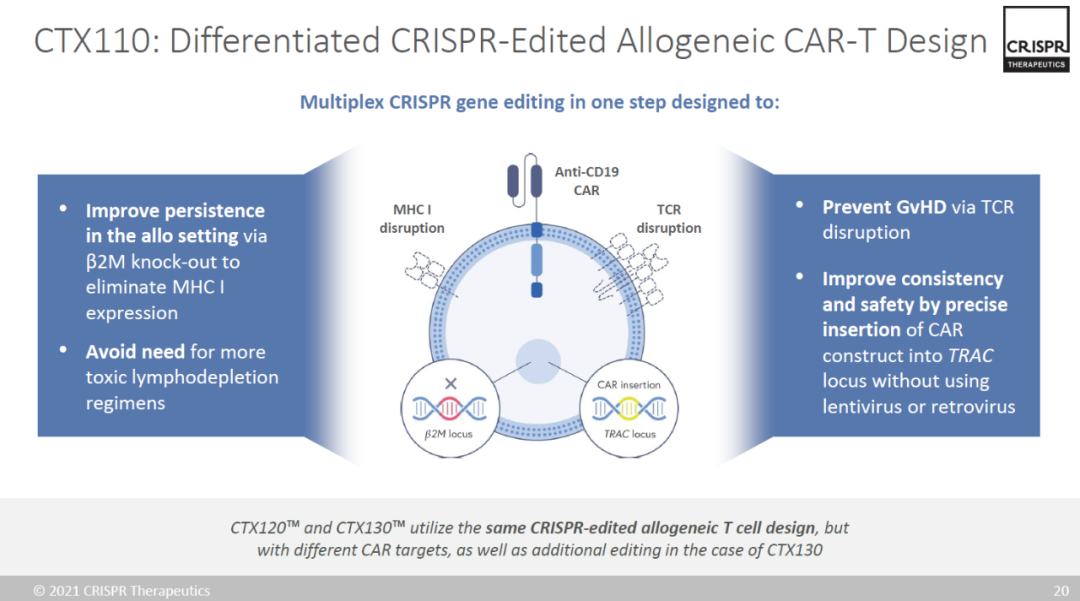
▲CTX110简介(图片来源:CRISPR Therapeutics)
在这项临床试验中,总计26名大B细胞淋巴瘤患者接受了CTX110的治疗并且随访时间至少28天。试验结果显示,在接受剂量超过10^8个细胞的CTX110治疗的患者中,基于意向治疗分析的总缓解率为58%,完全缓解率为38%。各个不同剂量的详细缓解信息请见下图。
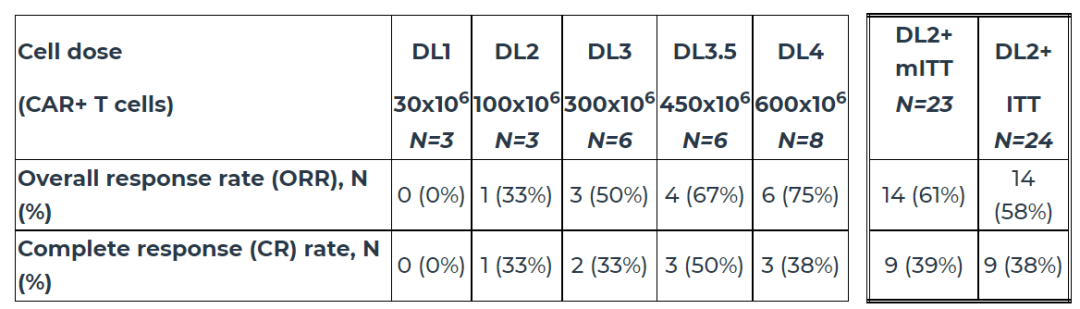
▲CTX110的1期临床试验疗效数据(图片来源:参考资料[1])
在接受治疗6个月后,完全缓解率为21%,最长的缓解持续时间超过18个月,显示了CTX110带来持续缓解的潜力。
在安全性方面,CTX110表现出差异化的积极安全性特征。没有出现移植物抗宿主病,所有的细胞因子释放综合征(CRS)均为1级或2级。在接受CTX110再次给药的患者中,CRS的频率和严重程度都没有增加。
只有一例同时患有HHV-6脑炎的患者出现3级以上的免疫效应细胞相关神经毒性综合征(ICANS)。具体安全性特征如下:
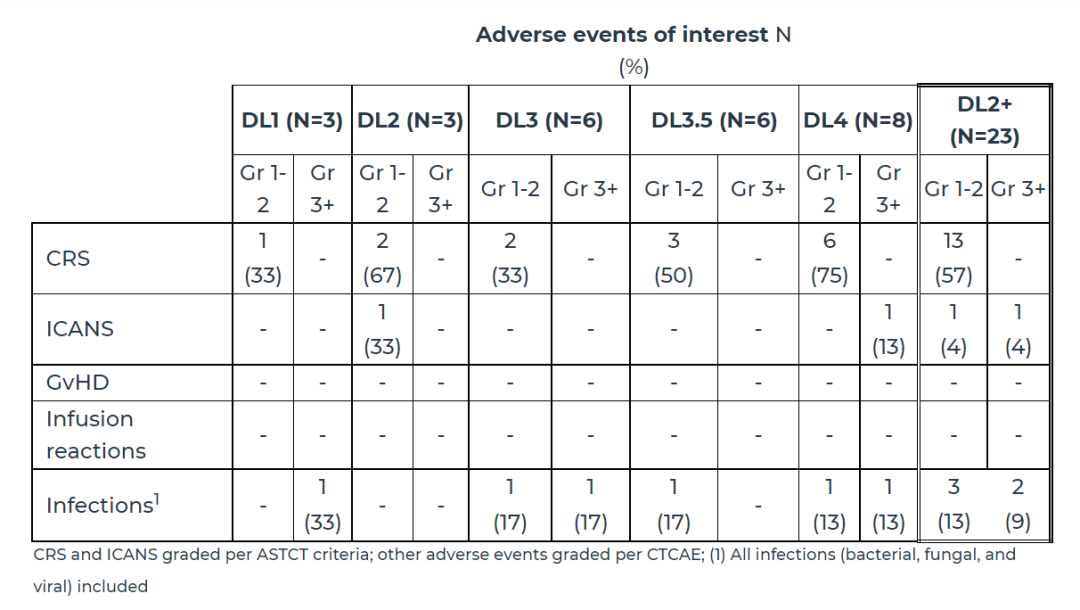
“我们很高兴分享这一临床试验的积极结果,它显示CTX110可以给大B细胞淋巴瘤患者提供一种可以立即使用的‘即用型’疗法,它的疗效与自体疗法相当,并且具有差异化的安全性特征。” CRISPR Therapeutics公司首席执行官Samarth Kulkarni博士说,“而且,利用巩固给药,我们具有进一步改善疗效的潜力。基于这些结果,我们计划在2022年展开注册性临床试验。”
参考资料:
[1] CRISPR Therapeutics Reports Positive Results from its Phase 1 CARBON Trial of CTX110™ in Relapsed or Refractory CD19+ B-cell malignancies. Retrieved October 12, 2021, from https://www.globenewswire.com/news-release/2021/10/12/2312955/0/en/CRISPR-Therapeutics-Reports-Positive-Results-from-its-Phase-1-CARBON-Trial-of-CTX110-in-Relapsed-or-Refractory-CD19-B-cell-malignancies.html
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。









 个人中心
个人中心
 我是园区
我是园区




