您还不是认证园区!
赶快前去认证园区吧!


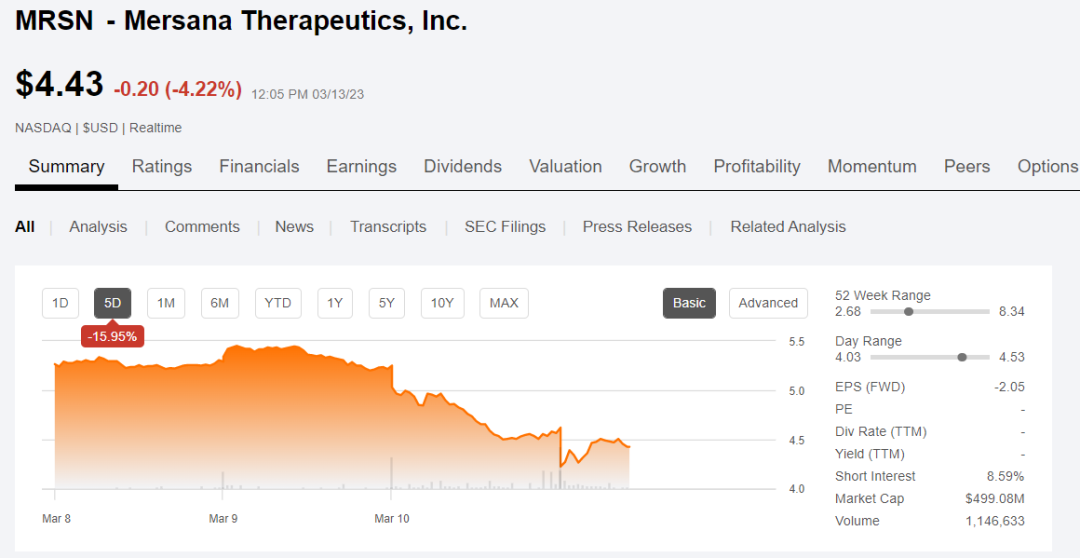
受此消息影响,该公司股价下跌约20%。
XMT-2056是一种STING激动剂ADC候选产品,可以通过STING信号激活先天免疫系统。2022年8月,GSK与Mersana Therapeutics达成近14.6亿美元的合作协议。根据协议条款,Mersana将获得1亿美元的预付款,以及高达13.6亿美元的里程碑付款。
Copyright © 2023 PHARMCUBE. All Rights Reserved.
欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;如需转载,请给微信公众号后台留言或发送消息,并注明公众号名称及ID。

医药魔方读者调研问卷
感谢陪伴 期待反馈
扫描二维码 提供宝贵建议




 个人中心
个人中心
 我是园区
我是园区




