您还不是认证园区!
赶快前去认证园区吧!

目前已有 2 种同类药物被 FDA 和欧洲药品管理局批准用于治疗 2 型糖尿病,分别是诺和诺德公司的 Xultophy 100/3.6 和赛诺菲公司的 Soliqua 100/33。
诺和诺德的 Xultophy 是德谷胰岛素/利拉鲁肽的固定比例复方制剂,最早于 2014 年在欧盟获批,2016 年获 FDA 批准在美上市。2020 年,Xultophy 全球销售额已达到 3.76 亿美元。在国内,诺和诺德在 2020 年 9 月递交上市申请并获受理(受理号:JXSS2000036/7),目前处于第一轮补充资料任务。
Xultophy 历年销售数据
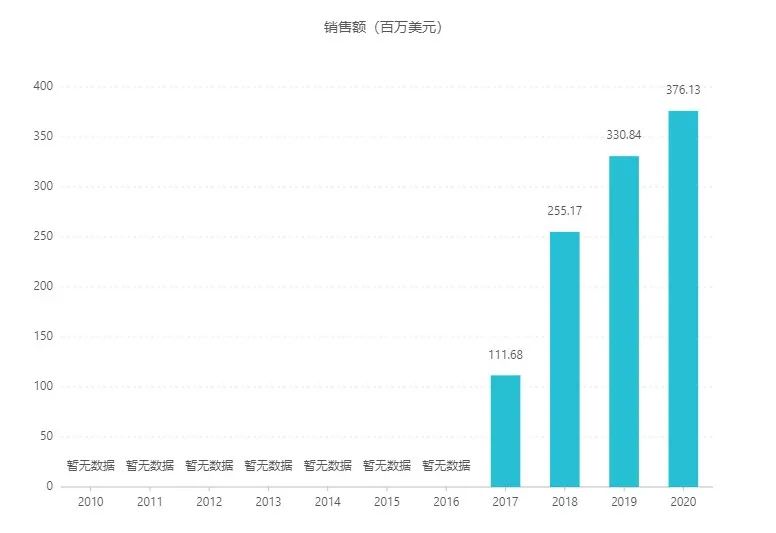
赛诺菲的 Soliqua 是利司那肽/甘精胰岛素固定比例复方制剂,与 Xultophy 同日获 FDA 批准上市,2020 年其全球销售额约为 1.84 亿美元。根据 Insight 数据库,赛诺菲已于 2019 年 2 月在国内启动 Soliqua 的 III 期临床。
根据 Insight 数据库,恒瑞目前共有 6 个糖尿病创新药在研,包括 SGLT2 抑制剂恒格列净、DPP4 抑制剂瑞格列汀、GLP-1 类似物诺利糖肽、长效胰岛素 INS068 等(详见下图)。HR17031 作为恒瑞自主研发的复方药,可能为诺利糖肽和 INS068 的复方制剂。
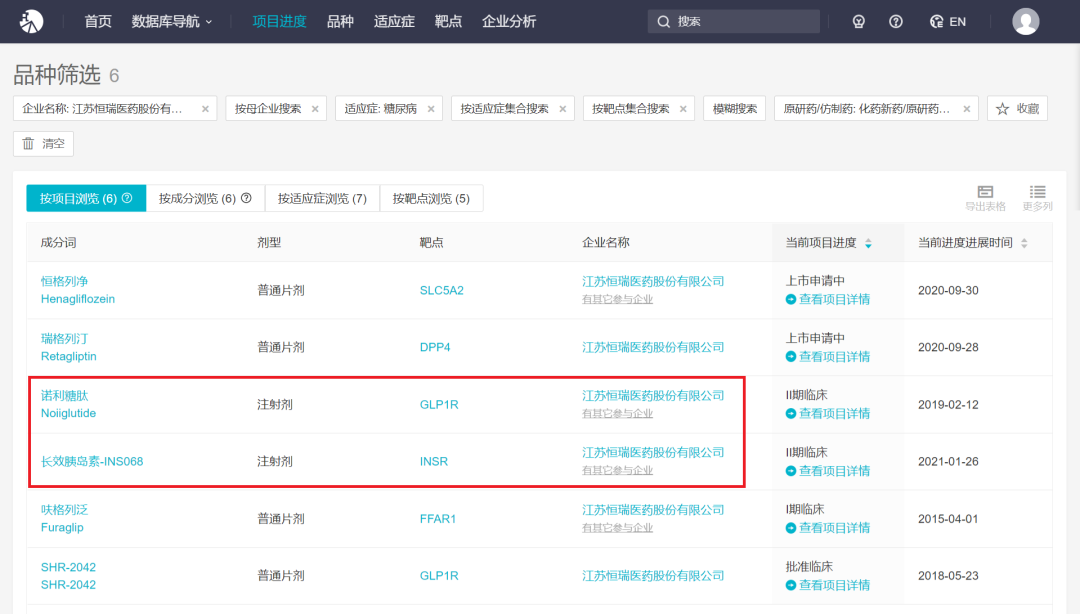
来自 Insight 数据库
 识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!
识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!
请注明:姓名+研究方向!


本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。




 个人中心
个人中心
 我是园区
我是园区




