
随着新冠疫情的发展,在新冠疫苗的研发中,疫苗接种机体后能否有效避免无症状感染和抑制病毒的再传播逐渐受到重视,其中的一个关键就是能否有效激活CD8+T细胞反应,实现细胞免疫应答,清除被病毒感染的细胞。尤其是在病毒不断变异的情况下,细胞免疫的识别序列保守性以及长期的记忆性特点有希望实现广谱的抗感染效果。因此,新冠刺突蛋白(S)的保守CD8+T表位一直是科学家和疫苗研发人员的寻找目标。
近日,艾棣维欣生物制药团队及复旦大学等合作单位在该领域有了重要的研究发现,相关发现为评估疫苗免疫后由CD8+ T细胞介导的免疫反应提供了工具,也为研发出更加有效和广谱的新冠疫苗提供了新的靶点和思路。经过进一步的深入分析发现,该表位肽序列不仅在已知野生型、VOC和VOI的突变株中高度保守,在目前新出现的Omicron变异株中仍然高度保守。
在线期刊《BioRxiv》发表的名为Identification ofa promiscuous conserved CTL epitope within the SARS-CoV-2 spike protein的文章,详细展示了相关的研究发现:
覆盖新冠病毒Spike蛋白中NTD和RBD区域的重叠氨基酸多肽库(Pool 1)具有较强的CTL表位活性;
在重叠氨基酸多肽库(Pool 1)中,发现一段具有较强CTL表位功能的多肽(Peptide 2),这段多肽在目前SARS-CoV-2各种流行变异株中高度保守,与世界上大多数人群的HLA等位基因相兼容。
多肽库Pool 1中存在具有较强CD8+ CTL表位活性的多肽

研究利用BALB/c小鼠动物模型,经过可在体内表达SARS-CoV-2刺突蛋白的pGX9501新冠DNA疫苗两剂次免疫,通过ELIspot实验发现:相较于对照组S2蛋白的重叠氨基酸多肽库(Pool2),使用Pool 1刺激淋巴细胞后新冠抗原特异性IFN-γ的表达量显著升高(图1)。同时,体内CTL实验显示,Pool 1在体内能够激发强烈的CTL细胞反应(图2)。这些结果表明,在多肽库Pool 1中存在着MHC I表位。
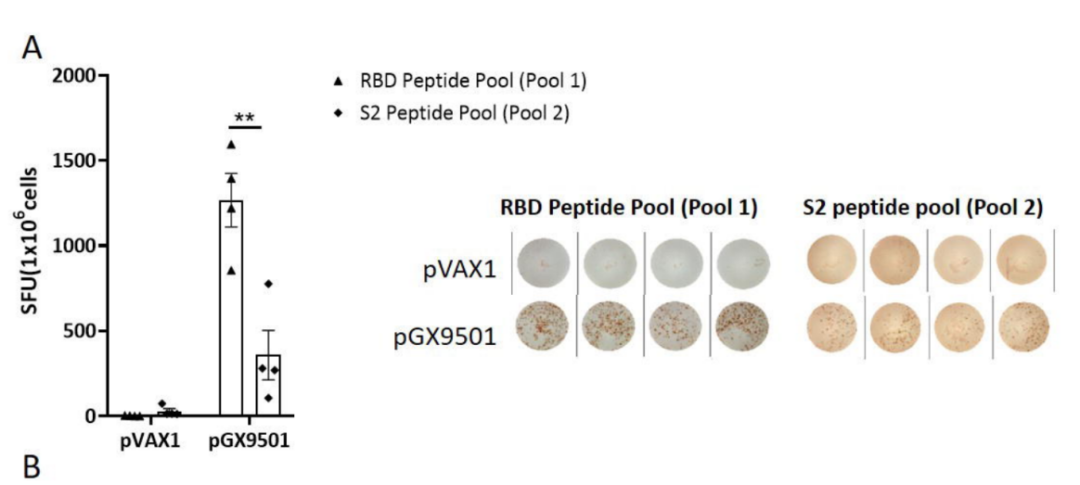
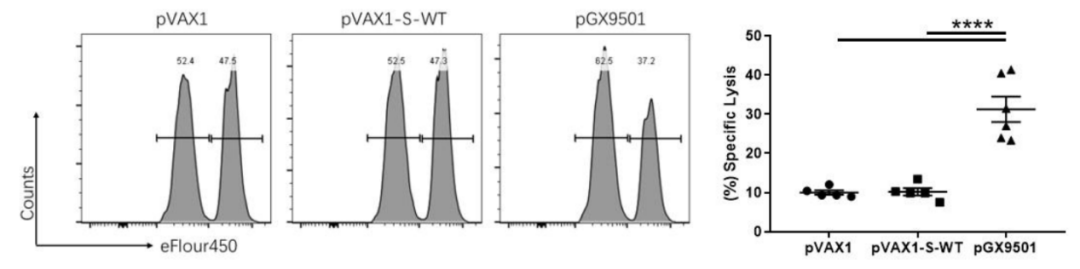
图2:体内CTL杀伤实验,相对于对照空载体pVAX1和野生型pVAX1-S-WT DNA疫苗免疫组,Pool 1检测出pGX9501免疫的小鼠显著的抗原特异性CTL反应
鉴定出多肽库Pool 1中存在的一段具有较强MHC-I表位功能的多肽Peptide2

通过IEBD表位在线分析,研究团队对肽库Pool 1中的氨基酸序列进行分析。同时,为提高预测的准确性,分析过程还采用了H-2d MHC-I等位基因的MHC I亲和力预测、MHC-I免疫原性预测以及MHC分子天然加工(MHC-NP)预测这三种方法。根据不同等位基因条件下各种预测方案下的得分,找出了Peptide2、11、12这三个多肽可能具有较强的MHC-I表位功能(如图3及原文数据)。
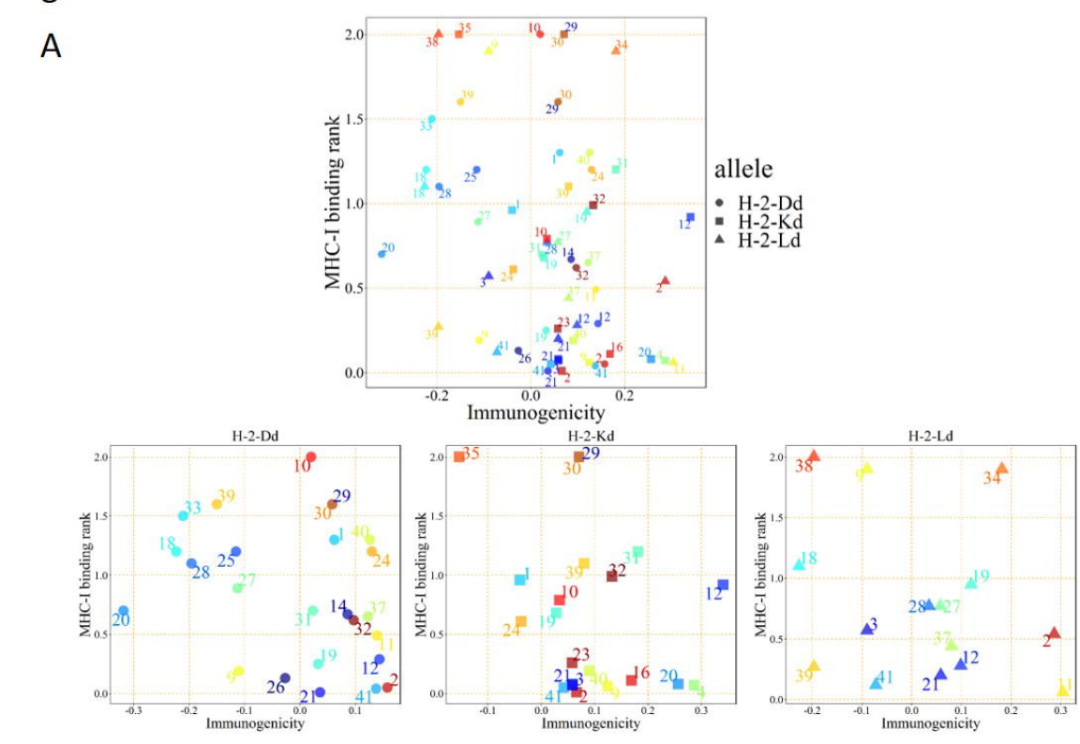
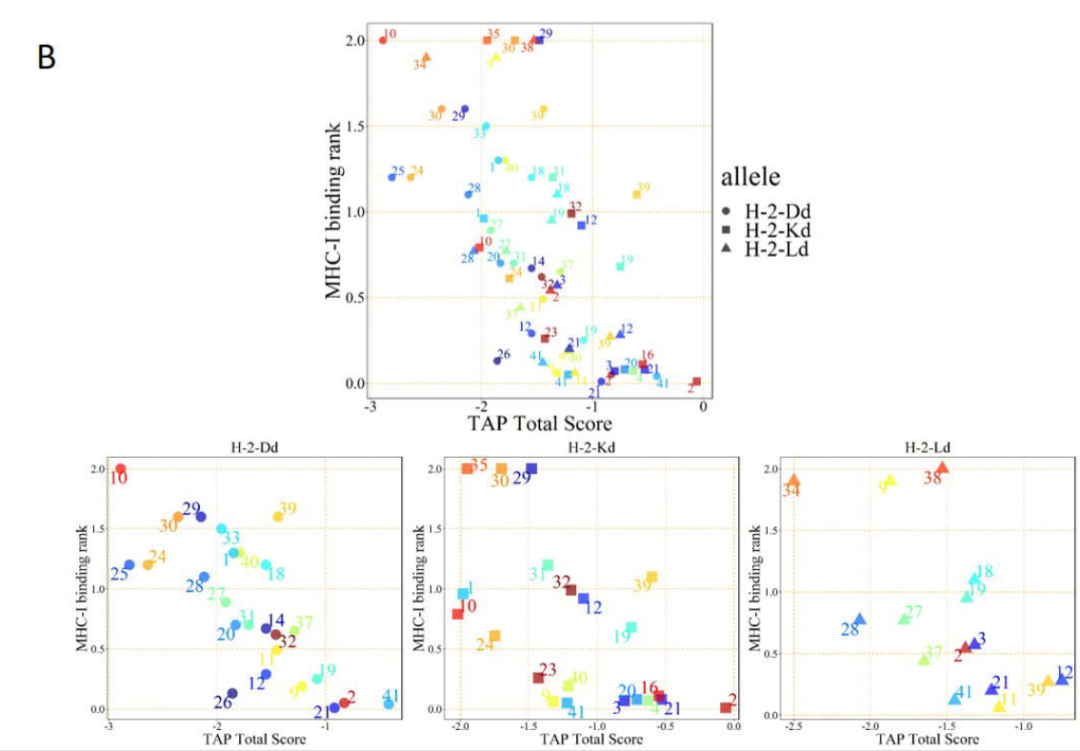
图3:IEBD表位在线分析预测结果,A为免疫原性评分,B为TAP结合功能评分
通过ELIspot实验,对IEBD预测评分高的多肽是否具有强MHC表位功能进行验证。结果表明Peptide2相较于其他两种多肽,能够刺激出更高的IFN-γ产生(图4A)。进一步研究发现Peptide 2激活的是CD8+ T细胞而非CD4+ T细胞(图4B)。根据H-2d MHC-I等位基因的偏好性预测Peptide2中的锚定氨基酸位点,然后将这些位点进行突变,验证结果表明不仅IEDB分析的亲和力分值显著下降(表1),且刺激CD8+T细胞分泌IFN-γ的水平也显著降低(图5)。
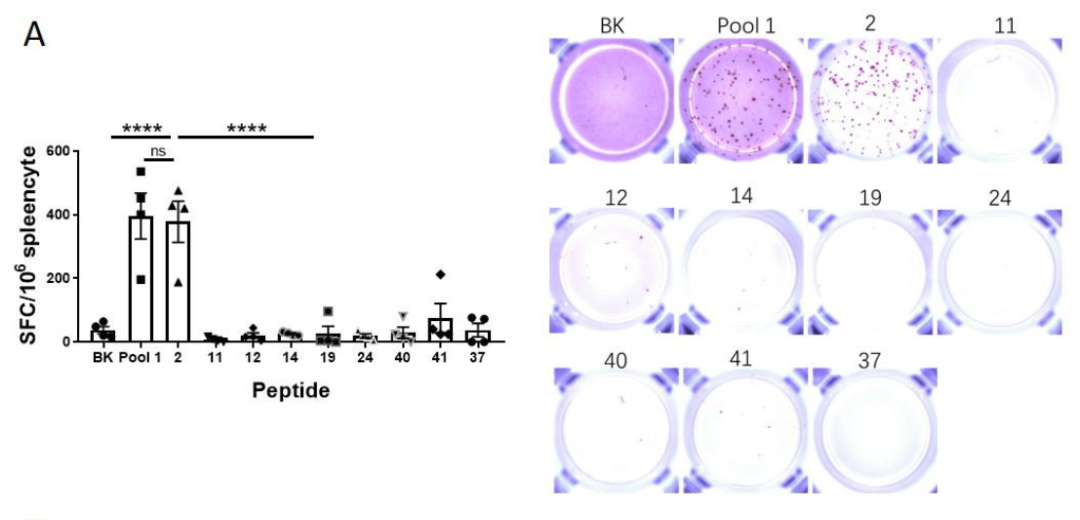
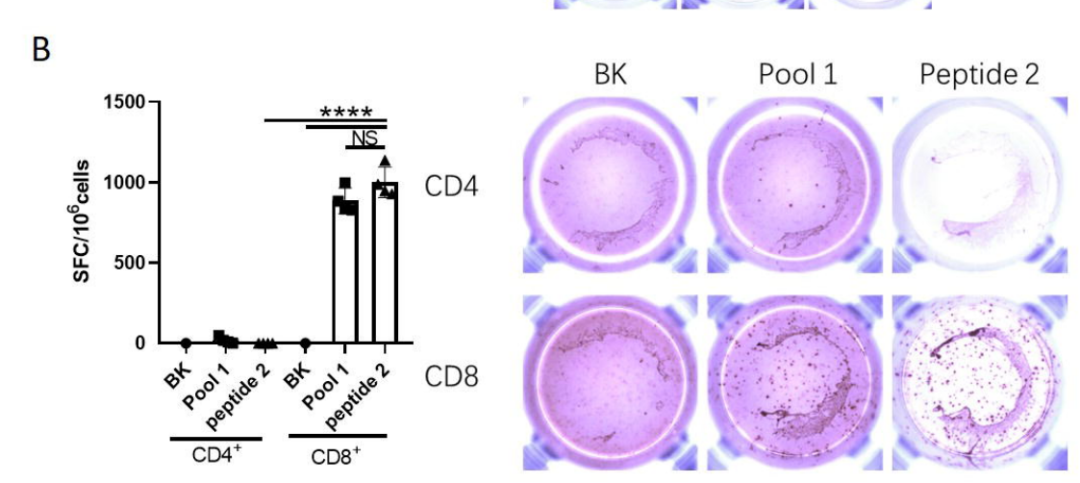
图4:ELISpot实验评价候选多肽的功能。图A比较了Pool1中不同的多肽片段体外刺激IFN-γ分泌的情况;图B验证了多肽分别刺激CD4+T细胞和CD8+T细胞分泌IFN-γ的水平
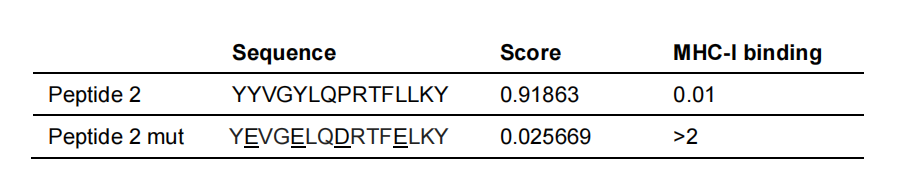
表1:IEBD比较Peptide2及氨基酸序列突变后的Peptide2与MHC-I分子的亲和性
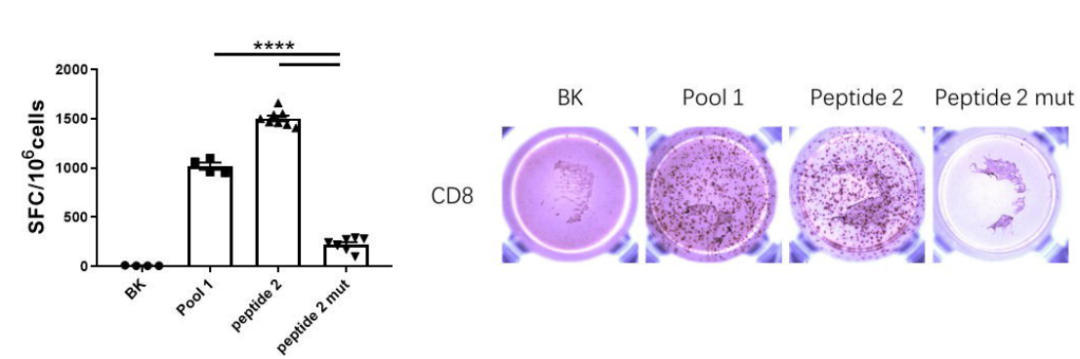
图5:ELISpot实验比较Peptide2及氨基酸序列突变后的Peptide2体外刺激淋巴细胞分泌IFN-γ的水平
Peptide 2序列高度保守,且与世界上大多数人群HLA等位基因相兼容

研究比对了Peptide 2氨基酸序列与WHO公布的SARS-CoV-2多种突变株,包括关切变异株(VOC)和关注变异株(VOI)在内的多种突变毒株序列,均发现Peptide 2序列高度保守(如图6A),位于刺突蛋白NTD区域末端及RBD上游(图6B)。这种高度保守的表位序列为评估疫苗免疫后CD8+介导的免疫反应提供了重要的工具。
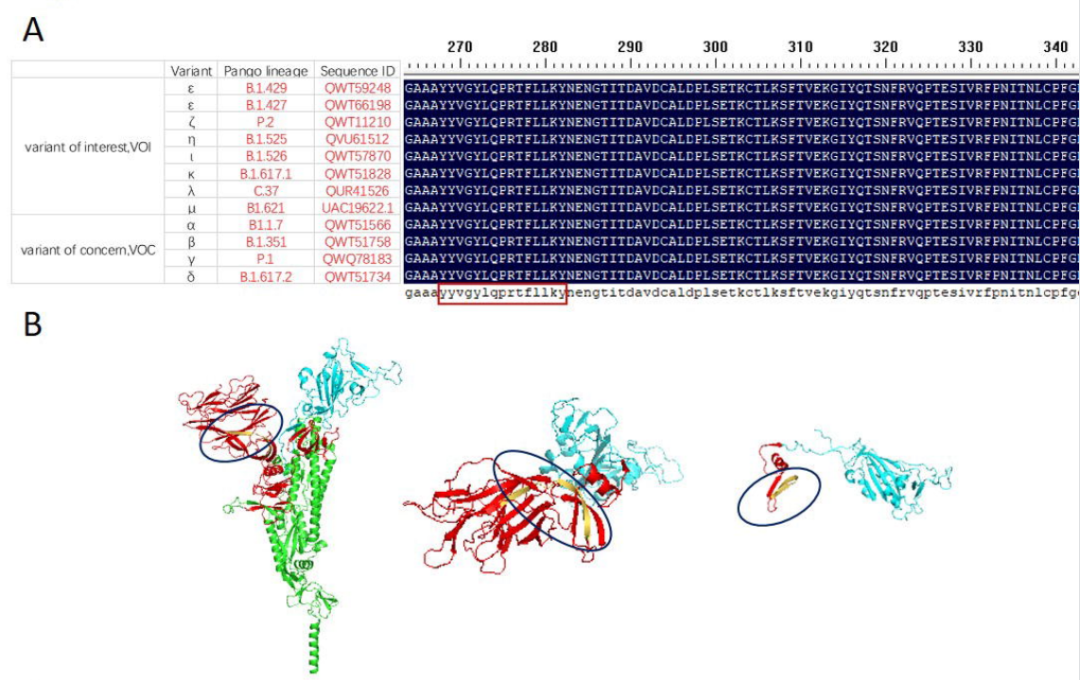
图6:A图显示Peptide 2 (黄色)与突变株序列比对;B图显示Peptide 2(黄色)在刺突蛋白结构中的位置
由于MHC-I基因在全球范围不同人群中存在遗传学上的差异和多样性特点,同一抗原多肽表位序列可能被某地区的人群MHC-1分子识别,但无法被其他群体识别或者识别能力很低,从而限制了其表位的广谱性的应用。为分析Peptide 2是否可以被世界范围内大多数群体识别,该研究对不同区域人群中27个主流的MHC-1型分子等位基因(Human Leukocyte Antigen, HLA)进行分析(图表见原文)。经过对Peptide 2与这些分子相互作用的评估,针对其与HLA亲和力、免疫原性以及TAP潜力的预测评分,结果显示Peptide 2表位可以被 HLA-A*02:01 (欧美地区), HLA-B*08:01(欧洲及澳大利亚地区),HLA-A*23:01(北非和撒哈拉以南的非洲,HLA-A*02:03(东南亚地区),HLA-A*24:02(大洋洲),HLA-A*02:06 (北非、东南亚及大洋洲),HLA-A*33:01 (中国和巴基斯坦),HLA- B*35:01(大洋洲)以及HLA-A*03:01 (欧洲)识别,显示出了Peptide 2的广谱兼容性。
可以看出,在SARS-CoV-2病毒刺突蛋白中涵盖NTD和RBD区域的重叠多肽库中发现的这种具有与MHC-I高亲和且序列保守,同时兼容世界上大多数人群HLA等位基因的表位序列(Peptide 2),该表位有望成为评估疫苗免疫后CD8+ T细胞介导的免疫反应的重要工具,以及有望成为开发更有效广谱的新冠疫苗候选产品的潜在靶标。

温馨提示
医药魔方记录行业发展,揭示产业趋势,持续输出具有行业理解和深刻洞见的内容,包括药品市场格局变化、医药行业趋势演变、政策解读、代表性公司业务分析、医药行业标杆人物专访、重磅事件解读等,帮助用户理解医药行业生态和演变,辅助行业用户决策。
星标⭐医药魔方,这样就不会错过我们的推送啦~

操作步骤见上图:1)点击标题下方“医药魔方”,2)至右上角“…”,3)设为星标



 个人中心
个人中心
 我是园区
我是园区




