您还不是认证园区!
赶快前去认证园区吧!
3 月 30 日,康方生物、中国生物制药共同宣布合作开发的 PD-1 单抗派安普利单抗获 FDA 突破性疗法认定,用于三线治疗转移性鼻咽癌。这是继 FDA 授予派安普利单抗三线治疗转移性鼻咽癌快速审批通道和孤儿药资格后,派安普利在美国取得的又一重要进展。


派安普利单抗(AK105,PD-1 单抗)由康方生物与正大天晴所设立的合营企业共同开发及商业化。派安普利的 Fc 受体和补体介导效用功能通过 Fc 区突变而完全去除,同时与国外已上市 PD-1 抗体相比抗原结合解离速率较慢。这些特点使得派安普利具有更有效地阻断 PD-1 通路的活性,并维持更强的 T 细胞抗肿瘤活性,有可能成为临床获益更好的抗 PD-1 药物。
NMPA 已于 2020 年 5 月受理派安普利单抗用于治疗至少经过二线系统化疗复发或难治性经典型霍奇金淋巴瘤 (r/r cHL) 的新药上市申请。其三线治疗转移性鼻咽癌注册性临床试验亦已达到主要终点,或将在近期递交上市申请。目前,根据 Insight 数据库,派安普利单抗的主要适应症包括肝癌、胃癌、肺癌、霍奇金淋巴瘤、鼻咽癌等疾病。
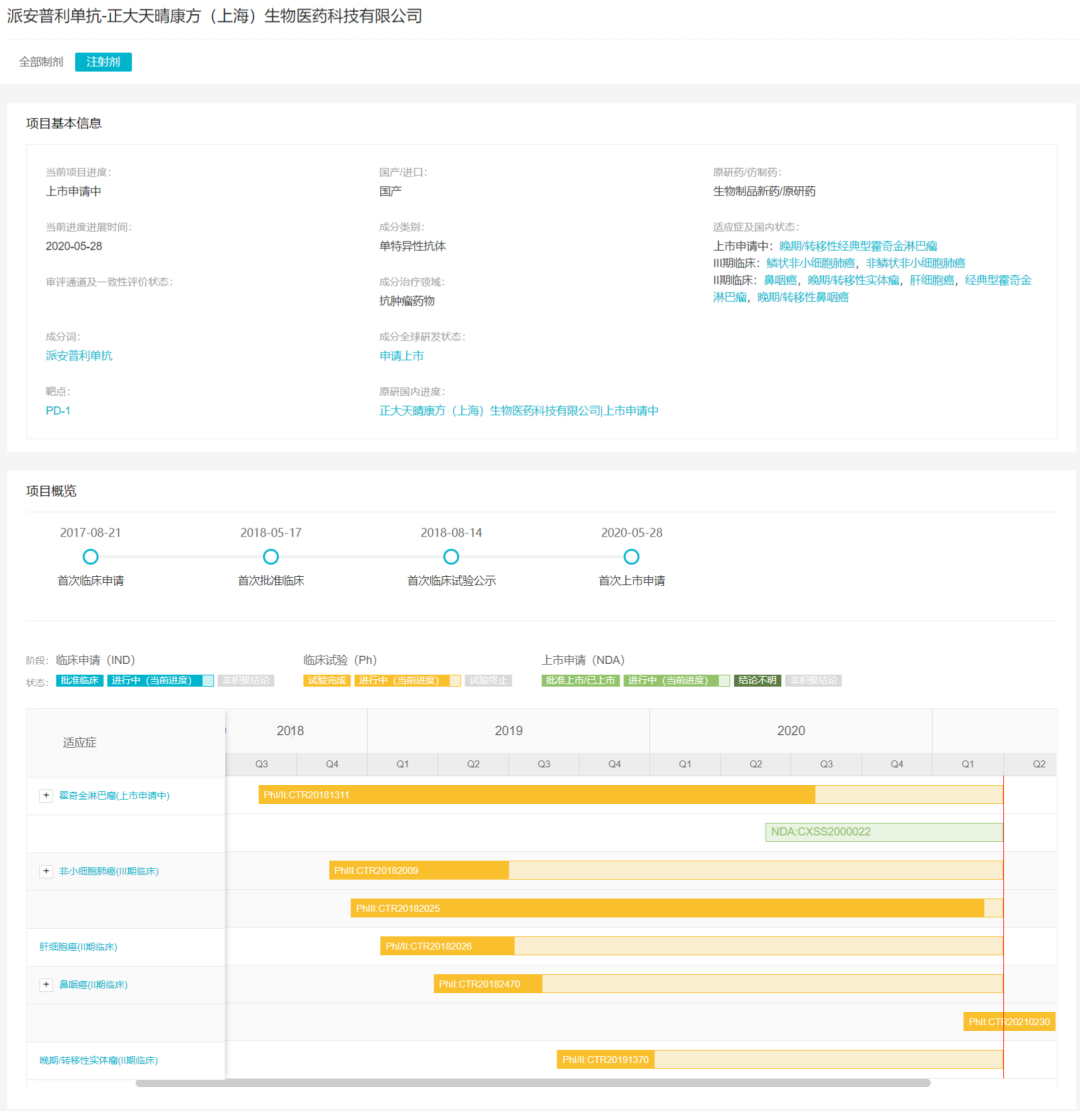
本次派安普利单抗三线治疗转移性鼻咽癌获得 FDA 授予突破性疗法认定,有望显著加速派安普利单抗在美国的商业拓展计划。
此前,君实的 PD-1 特瑞普利单抗的鼻咽癌适应症也曾于 2020 年 9 月获 FDA 突破性疗法认定,并在今年 3 月 4 日向 FDA 滚动提交特瑞普利单抗用于治疗复发/转移性鼻咽癌的 BLA,成为首个在 FDA 报产的国产 PD-1。



 个人中心
个人中心
 我是园区
我是园区




