您还不是认证园区!
赶快前去认证园区吧!

来自:海思科公告
HSK29116 是海思科自主研发的靶向 BTK 的口服 PROTAC 小分子抗肿瘤药物,用于治疗复发难治 B 细胞淋巴瘤,是国内首款、全球第二款进入临床研究的 BTK-PROTAC 药物。该品种已于 2021 年 4 月获得国家药品监督管理局(NMPA)批准开展临床,目前国内和澳大利亚的临床剂量爬坡试验正在快速推进中,已开展到第四个剂量组,进展良好。美国临床将作为 HSK29116 全球多中心研究的重要组成部分,即将正式启动 I 期临床试验。
HSK29116 是基于海思科领先的 Protac 研发平台筛选出的首个申报临床的口服 BTK-Protac 小分子抗肿瘤药物,具有选择性阻断 BTK 激酶活性和蛋白酶体降解双重抗肿瘤活性,通过调节信号通路干预 B 细胞发育,控制各种 B 细胞恶性肿瘤的进展。HSK29116 对野生型 BTK 具有更好的药效,同时可克服 BTK 抑制剂常见的耐药突变问题。若其成功上市,可为 B 细胞恶性肿瘤患者带来更好的临床获益和更多的药物选择。
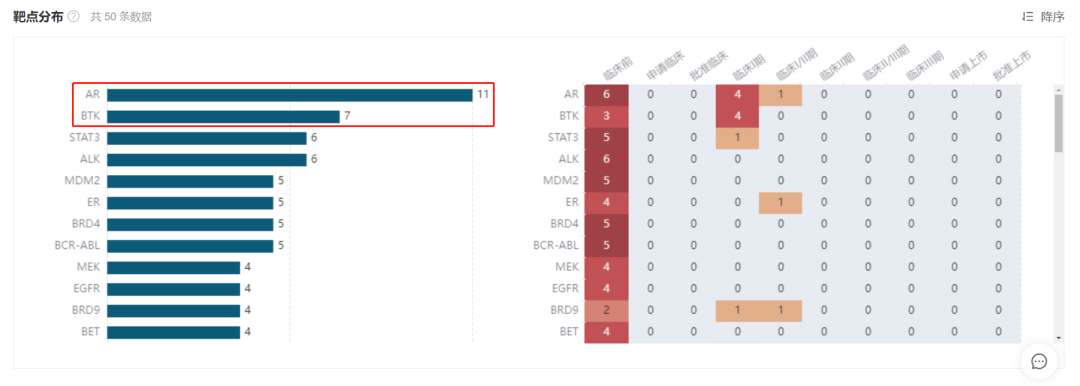
目前 ,据 Insight 数据库显示 , 全 球 PROTAC 在研项目主要 还扎堆在 AR 和 BTK 这两个已成药靶点,详见下图 。 尽管 PR OTAC 药 物的研发 有望 克服已有药物 耐 药现象 ,但其核心优势之一还在于针对不可成药靶点 的蛋白降解,因此,从临床前项目来看还有一些聚焦于 STAT3、c-Myc、KRAS 等靶点,尤其 STAT3 靶点已有 1 款进入临床开发阶段。期待更多新靶点 First-in-class PROTAC 药物的出现,为临床上尚存在未满足需求的疾病增添治疗新机制。



 个人中心
个人中心
 我是园区
我是园区




