速递!儿童多动症新药上市申请拟纳入优先审评
收藏
关键词:
上市新药优先审评药上市申请
资讯来源:医药观澜 + 订阅账号
发布时间:
2022-07-19
▎药明康德内容团队报道
今日(7月19日),中国国家药监局药品审评中心(CDE)官网公示,祐儿医药和Tris Pharma公司联合申报的盐酸哌甲酯缓释咀嚼片上市申请拟被纳入优先审评。公开资料显示,该药是一种中枢神经系统(CNS)兴奋剂,主要用于治疗注意缺陷多动障碍(ADHD,俗称多动症),已在海外获批上市。
祐儿医药是一家专注于儿科领域的公司,由斯道资本、F-Prime Capital和泓元资本共同创办,公司首席执行官(CEO)为张诚先生。该公司致力于通过研发和引进有效且经临床验证的儿童药物,并打造一个专门的儿科生态系统,以满足中国儿童患者的未满足临床需求。2021年4月,祐儿医药完成了A轮融资。
今年7月,祐儿医药和Tris Pharma公司联合申报的盐酸哌甲酯缓释咀嚼片上市申请获得CDE受理,并于今日被纳入拟优先审评公示名单。根据优先审评公示信息,该药因“符合儿童生理特征的儿童用药品新品种、剂型和规格”拟被纳入优先审评,针对的适应症为注意缺陷多动障碍。
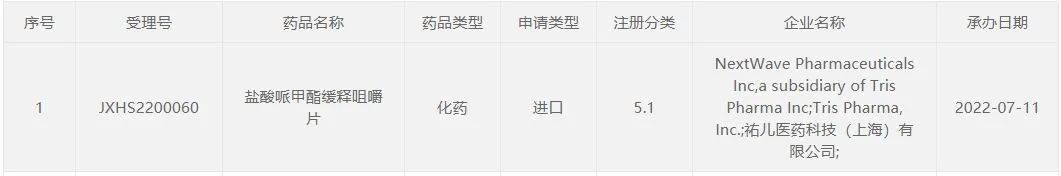
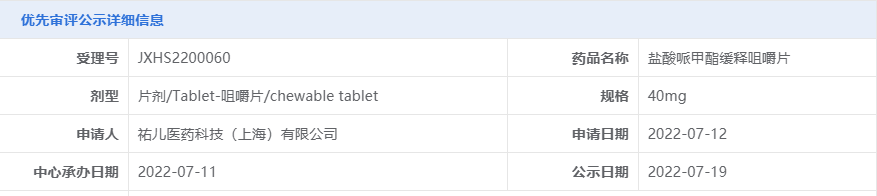
根据Tris Pharma官网资料,盐酸哌甲酯缓释咀嚼片已在海外获批上市治疗ADHD,商品名为QuilliChew ER。研究显示,QuilliChew ER可以在45分钟内起效,有效控制多动症症状。在一项临床研究中,QuilliChew ER显著改善了6至12岁多动症儿童患者的注意力和行为。
ADHD俗称多动症,是一种慢性大脑疾病,表现为注意力无法集中,多动,容易冲动。ADHD症状可能在儿童3-6岁时开始出现,可以持续到青少年和成年期。ADHD是儿童期最常见的精神疾病,影响8%至9%的学龄儿童。
希望这款盐酸哌甲酯缓释咀嚼片早日在中国获批,为患者带来新的治疗选择。
[1]中国国家药监局药品审评中心(CDE)官网. Retrieved July 19,2022, From https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d
[2] Tris Pharma Expands ADHD Portfolio with Acquisition of NextWave Pharmaceuticals. Retrieved Sep 24,2018, from https://www.trispharma.com/who-we-are/news-and-media/tris-pharma-expands-adhd-portfolio-with-acquisition-of-nextwave-pharmaceuticals/
[3] Tris Pharma. From https://www.trisadhd.com/quillichew-er/
本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。








 个人中心
个人中心
 我是园区
我是园区




