全球范围内,肺癌是最常见的癌症类型,也是癌症死亡的首要原因。MET信号通路改变(包括MET第14号外显子跳跃突变和MET扩增)已在多种类型癌症中被发现,包括非小细胞肺癌(NSCLC),这与肿瘤的侵袭行为和不良的临床预后相关。据统计MET信号通路改变发生在3-5%的NSCLC患者中。
Tepotinib是默克发现的一种口服MET激酶抑制剂,可强效、高度选择性抑制由MET基因改变(包括MET第14号外显子跳跃突变和MET扩增)引起的致癌信号,具有改善携带这些特定MET改变的侵袭性肿瘤患者治疗预后的潜力。
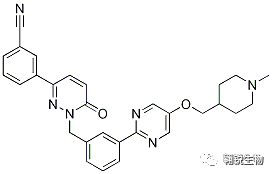
tepotinib分子结构式(图片来源:chemicalbook.com)
今年3月,Tepotinib在日本获得批准,成为全球第一个口服MET抑制剂,适应症为:治疗不可切除性、晚期或复发性、携带METex14跳跃改变的非小细胞肺癌(NSCLC)患者。目前,tepotinib已被授予突破性药物资格(BTD),正在接受美国FDA的优先审查。
近日关于Tepotinib治疗非小细胞肺癌(NSCLC)的关键单臂II期VISION研究(NCT02864992)的阳性结果发表于NEJM。研究评估了Tepotinib在MET基因第14号外显子跳跃(METex14)的转移性NSCLC患者群体中的疗效和安全性。研究中经确认携带METex14跳跃改变的晚期或转移性NSCLC患者接受了tepotinib单药治疗(每日一次,500mg),主要终点是经过独立审查接受至少9个月随访的患者中的客观缓解率(ORR),根据液体活检(LBx)或组织活检(TBx)是否检出METex14跳跃改变来分析缓解率。截止2020年1月1日,共计152例患者接受了tepotinib治疗,99例接受了至少9个月随访。在合并活检组(LBx或TBx),独立审查评估确定的ORR为46%(95%CI:36-57)、中位缓解持续时间(DOR)为11.1个月(95%CI:7.2-NE)。在LBx活检组66例患者中,ORR48%(95%CI:36-61)、在TBx活检组60例患者中,ORR为50%(95%CI:37-63),有27例患者根据2种活检方法取得了阳性结果。研究调查员评估确定的ORR为56%(95%CI:45-66),且无论之前针对晚期或转移性肺癌接受过何种治疗方案,缓解率均相似。该研究中,研究调查员认为与Tepotinib治疗相关的≥3级不良事件发生率为28%,包括外周水肿(7%),不良事件导致11%的患者永久停药Tepotinib。
无独有偶,今年5月诺华MET抑制剂Tabrecta(capmatinib)获得美国FDA加速批准,用于治疗携带METex14跳跃突变的转移性NSCLC患者,包括一线治疗患者和先前接受过治疗的患者。在临床试验中,Tabrecta治疗初治和经治METex14突变患者的总缓解率(ORR)分别为68%和41%。成为第一个被美国FDA批准专门针对METex14突变转移性NSCLC的疗法。
今年7月底,和黄医药MET抑制剂沃利替尼(savolitinib)被国家药监局纳入优先审评,该药用于治疗携带METex14跳跃改变的NSCLC患者。在2020年ASCO年会上公布的II期临床研究(NCT02897479)数据显示,沃利替尼治疗METex14跳跃突变NSCLC疗效可评估的患者中,客观缓解率(ORR)为49.2%、疾病控制率(DCR)为93.4%、缓解持续时间(DOR)为9.6个月。




 个人中心
个人中心
 我是园区
我是园区




