恒瑞 2 款单抗启动 III 期临床,分别靶向 PCSK9 和 IL17A
收藏
关键词:
临床靶向期临床单抗恒瑞
资讯来源:易企说17Talk + 订阅账号
发布时间:
2021-04-15
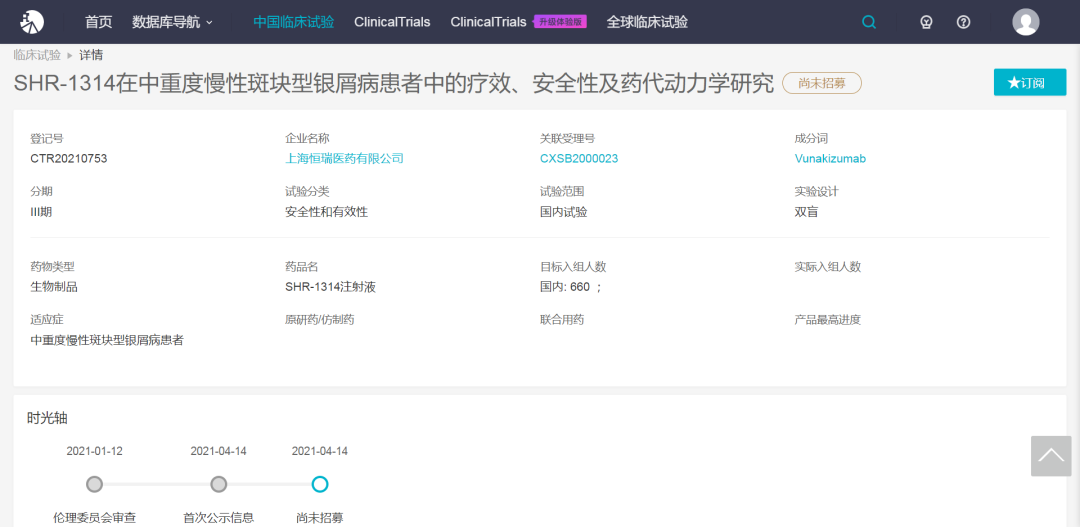
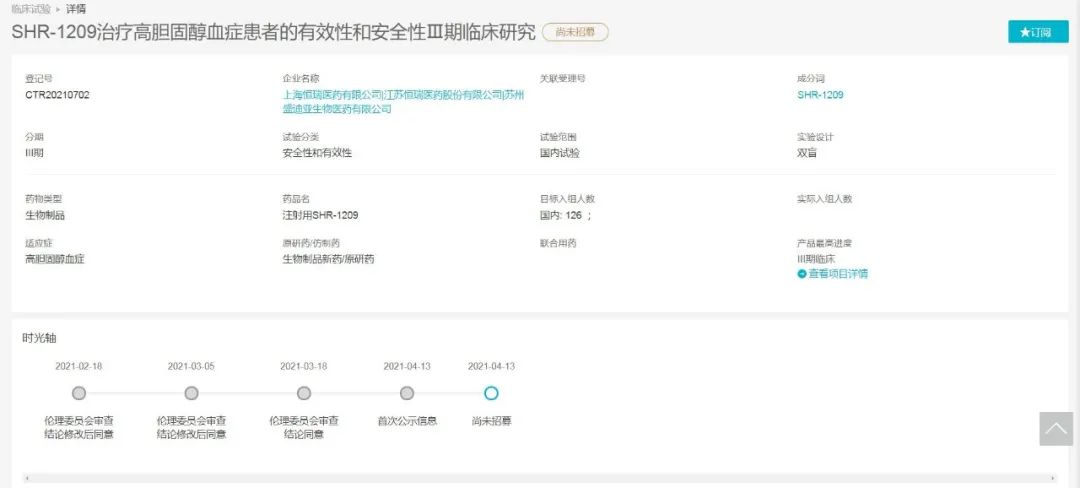
近日,据 Insight 数据库显示,恒瑞有 2 款新药启动 III 期临床,分别为靶向 PCSK9 的注射用 SHR-1209,用于高胆固醇血症;另一款为靶向 IL-17A 的 SHR-1314 注射液,用于中重度慢性斑块型银屑病。
图片来源:Insight 数据库(https://db.dxy.cn/v5/home)
PCSK9 单抗,恒瑞、信达、君实均进入 III 期临床
PCSK9 是他汀类药物之后公认的最有效的降脂靶点,人源化抗 PCSK9 单克隆抗体(SHR-1209)是恒瑞研发的治疗用生物制品 1 类新药,它通过降低 PCSK9 循环水平,使细胞表面 LDLR(低密度脂蛋白受体)表达升高,LDL-C(低密度脂蛋白胆固醇)清除增加,从而降低循环中 LDL-C 水平。
目前全球共有两款 PCSK9 单抗药物获批,分别是安进的依洛尤单抗(Evolocumab,商品名 Repatha) 和赛诺菲和再生元联合研发阿利珠单抗(Alirocumab,商品名:Praluent),目前两款新药均已在国内获批。
据 Insight 数据库显示,目前恒瑞已完成 SHR-1209 用于高胆固醇血症的 2 期临床研究,本次新开展的 3 期临床也是该产品首个进入 3 期临床的适应症。国内该靶点布局企业比较多,目前来看国内企业中,除了恒瑞外信达和君实生物的 PCSK9 单抗也已进入 3 期临床。
图片来源:Insight 数据库(https://db.dxy.cn/v5/home)
SHR-1314 注射液,即 Vunakizumab,是一款靶向人 IL-17A 的重组人源化单克隆抗体,该药最早于 2016 年 6 月该药首次获批临床。目前,恒瑞已针对该药展开 9 项临床,本次是首次进入 III 期。在既往的研究中表明,SHR-1314 注射液不仅可以用于治疗成年中重度斑块状银屑病,还可以用于改善强直性脊柱炎的疾病活动性,且起效迅速,疗效持续,安全性良好。
目前全球已有 2 个 IL-17A 抗体获批上市。诺华公司的 secukinumab(商品名 Cosentyx)于 2015 年在美国和欧洲获批上市,2019 年其销售额为 35.51 亿美元;礼来公司的 ixekizumab(商品名 Taltz)于 2016 年在美国和欧洲获批上市,2019 年其销售额为 13.66 亿美元。Secukinumab 和 ixekizumab 分别于 2019 年 4 月和 9 月作为第一批临床急需境外新药在中国获批上市。
图片来源:Insight 数据库(https://db.dxy.cn/v5/home)
BIO100+旨在打造中国BIO领域的企业服务平台,为企业提供线上+线下的整体发展解决方案。平台上汇聚中国生物产业领先的100+创新技术企业,共建全产业链交流合作平台。
江苏恒瑞医药股份有限公司是一家从事医药创新和高品质药品研发、生产及推广的医药健康企业,创建于1970年,2000年在上海证券交易所上市。目前共有全球员工24000余名,是国内知名的抗肿瘤药、手术用药和造影剂的供应商,也是国家抗肿瘤药技术创新产学研联盟牵头单位,建有国家靶向药物工程技术研究中心、博士后科研工作站。
2020 年恒瑞医药入选全球 1000 强药企榜单,位列第 21 位。2019年,公司实现营业收入232.9亿元,税收26.8亿元。
在市场竞争的实践中,恒瑞医药坚持以创新为动力,打造核心竞争力。公司每年投入销售额10%以上的研发资金,在美国、欧洲、日本和中国多地建有研发中心或分支机构。目前公司的研发团队已有3400多人,其中包括2000多名博士、硕士及200多名海归人士。近年来,公司先后承担了国家重大专项课题44项,已有6个创新药艾瑞昔布、阿帕替尼、硫培非格司亭、吡咯替尼、卡瑞利珠单抗及瑞马唑仑获批上市,一批创新药正在临床开发,并有多个创新药在美国开展临床。截止2020年10月,公司累计申请发明专利1000余项,拥有国内授权专利238项,欧美日等国外授权专利347项,先后荣获中国发明专利金奖1项、中国发明专利优秀奖2项,核心技术获得国家科技进步二等奖2项、省科技进步奖10项。
恒瑞医药本着“诚实守信、质量第一”的经营原则,抗肿瘤药、手术麻醉类用药、特色输液、造影剂市场份额在国内市场名列前茅。目前公司有注射剂、口服制剂和吸入性麻醉剂等19个制剂产品在欧美日上市,实现了国产注射剂在欧美日市场的规模化销售。
恒心致远,瑞颐人生。恒瑞医药一直秉承“科研为本,创造健康生活”的理念,以建设中国人的跨国制药集团为总体目标,拼搏进取、勇于创新,不断实现企业发展的新跨越和新突破。




 药选址
药选址