罗氏「托珠单抗」皮下注射剂型在华递交新适应症上市申请
收藏
关键词:
单抗注射上市上市申请罗氏适应症
资讯来源:医药观澜 + 订阅账号
发布时间:
2022-11-22
▎药明康德内容团队报道
11月21日,中国国家药监局药品审评中心(CDE)官网公示显示,罗氏(Roche)递交了一项托珠单抗注射液(皮下注射)的新适应症上市申请,并获得受理。开资料显示,托珠单抗(tocilizumab)是一款抗IL-6R重组人源化单抗。今年4月,托珠单抗皮下注射剂型首次在华获批,用于治疗特定的中到重度活动性类风湿关节炎成年患者。
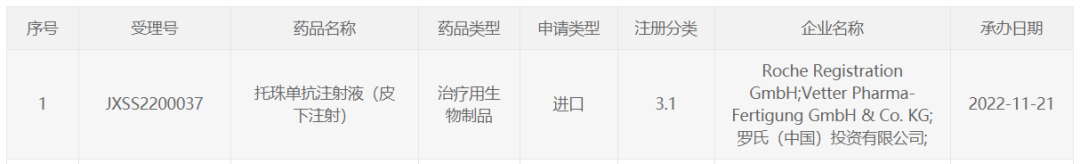
截图来源:CDE官网
公开资料显示,托珠单抗是采用哺乳动物细胞(CHO)表达的一种重组人源化抗人白介素6(IL-6)受体单克隆抗体,通过抑制IL-6受体的活性而发挥作用。IL-6是一种促炎性细胞因子,它的释放可以促发一系列下游的促炎症反应。托珠单抗通过阻断IL-6与可溶性及膜结合的IL-6受体结合,抑制IL-6的信号转导,从而减少病理性炎症反应。
在中国,托珠单抗的静脉注射剂型已获批多种适应症,包括类风湿关节炎、全身型幼年特发性关节炎、成年和2岁及以上儿童患者由CAR-T细胞引起的重度或危及生命的细胞因子释放综合征等等。
2022年4月,罗氏宣布托珠单抗注射液(皮下注射)剂型在中国正式获批,用于治疗对改善病情的抗风湿药物(DMARDs)治疗应答不足的中到重度活动性类风湿关节炎的成年患者。
根据
罗氏早前发布的新闻稿,相较于静脉注射,托珠单抗皮下注射不仅缩短了单次的治疗时间,也省去了患者来回医院、办理住院手续的时间,可满足患者长期慢病用药管理的需求,提高患者用药的便捷性和可及性。
本次托珠单抗注
射液(皮下注射)剂型又一项上市申请获受理意味着,它将有望给患者带来更多的治疗选择。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网. Retrieved Nov 21,2022, From https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d
[2]罗氏抗疫药物托珠单抗皮下注射剂型在华获批,开启双剂型时代. Retrieved Apr 13,2022, From https://mp.weixin.qq.com/s/SJB67iqnP9Fb--X0cIrbgg

本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈。转发授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。







 个人中心
个人中心
 我是园区
我是园区





