作者:饮乐多
3月31日,国家药品监督管理局发布公告,两款用于胃肠道间质瘤(GIST)的靶向治疗药物阿泊替尼片(avapritinib)和瑞派替尼片(ripretinib)同一天获得进口药品注册许可。
阿泊替尼是基石药业从Blueprint Medicines授权获得的KIT/PDGFRα激酶抑制剂。2018年6月,该公司与Blueprint Medicines达成独家合作及授权协议,获得了包括阿泊替尼在内的三款候选药物在大中华区的开发与商业化权利。2020年1月,阿泊替尼首先获得美国FDA批准,用于治疗PDGFRA外显子18突变(包括PDGFRα D842V突变)不可切除或转移性GIST成人患者。
瑞派替尼为再鼎医药从美国Deciphera公司授权获得的一种酪氨酸激酶开关控制抑制剂,通过独特的双重作用机制来调节激酶开关和活化环,从而广泛抑制KIT和PDGFRα突变激酶。2020年5月,瑞派替尼首先获得美国FDA批准,用于治疗既往接受过包括伊马替尼在内的3种或更多种激酶抑制剂治疗的晚期GIST成年患者。
GIST是一类起源于胃肠道间叶组织的肿瘤,约占胃肠道恶性肿瘤的1~3%,估计年发病率约为10~20/100万,在我国每年约有2~3万例新诊断GIST患者。超过85%的GIST患者携带KIT或PDGFRα突变,其中KIT突变最常见,达80%,PDGFRα突变达10%,此外还有10%的患者缺少KIT或PDGFRα突变,此类患者可能携带琥珀酸脱氢酶(SDH)复合物突变、BRAF突变、KRAS突变或NRAS突变。
GIST对放化疗均不敏感,对于无法手术切除或者术后出现复发或转移的GIST患者,靶向治疗是主要的治疗手段。伊马替尼于2002年被批准用于GIST的治疗,取得了巨大的成功。然而,约15%的患者对伊马替尼表现出原发耐药性,另有42%的患者会在两年内对伊马替尼发展出继发性耐药,虽然舒尼替尼和瑞戈非尼先后获批用于伊马替尼治疗失败后的GIST二线和三线的治疗,但靶向治疗后的耐药问题依然成为GIST治疗面临的主要困境。
阿泊替尼的获批上市,为伊马替尼治疗效果不佳的PDGFRα外显子18突变(包括PDGFRα D842V突变)GIST患者带去了福音。国际多中心临床试验结果显示,既往至少接受过 2 种激酶抑制剂(包含伊马替尼)治疗进展的无法切除PDGFRα 基因 D842V 突变GIST 成年患者,应用阿泊替尼治疗总体缓解率(ORR)达86%,临床获益率(CBR)达到95.3%。在中国进行的桥接试验结果也显示相近疗效,携带PDGFRα D842V突变患者接受阿泊替尼治疗后,所有患者靶病灶均有缩小,ORR为62.5%,且安全性和耐受性良好。
而瑞派替尼则为晚期GIST四线治疗带来新的标准方案,关键获批临床试验结果显示,对既往接受过包括伊马替尼、舒尼替尼和瑞戈非尼在内多种激酶抑制剂治疗后进展的晚期GIST患者,瑞普替尼皆有较好的疗效。与安慰剂相比,瑞派替尼治疗组患者无进展生存期显著延长(6.3个月vs 1.0个月),疾病进展或死亡的风险显著降低了85%。中位总生存期为15.1个月(安慰剂组为6.6个月)。
赛道:谁是下一个变局者?
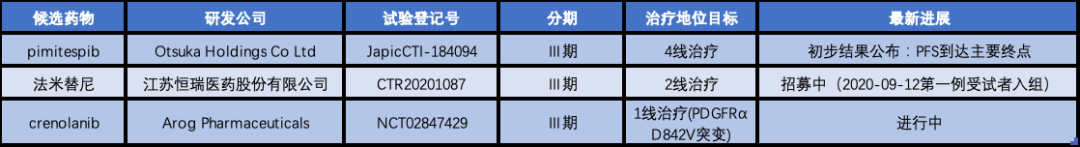
作为实体瘤中靶向治疗相对成功的肿瘤类型,GIST自然成为众多候选靶向治疗药物的研究重点领域。根据CPM数据库的监测数据,目前全球针对GIST的临床试验已超过300个,其中处于进行中的超过110个。其中,将有可能改变GIST市场格局带来新玩家的临床试验主要有3个(表1),涉及到在研候选药物Pimitespib、法米替尼和Crenolanib。
Pimitespib(TAS-116)是Otsuka Holdings Co Ltd旗下Taiho Pharmaceutical Co Ltd正在开发的口服HSP90抑制剂。JapicCTI-184094临床试验主要评估Pimitespib对既往接受过一、二、三线激酶抑制剂治疗的晚期GIST患者的安全性及有效性,目前初步结果已公布。Taiho于2021年2月22日在官网发布的消息显示,该代号为CHAPTER-GIST-301的关键Ⅲ期临床试验达到了延长无进展生存期(PFS)的主要终点。Taiho表示将继续推动Pimitespib上市进程,争取尽快获得批准。
法米替尼是江苏恒瑞医药股份有限公司开发的一种口服多靶点受体酪氨酸激酶抑制剂,具有抗增殖和抑制血管生成的双重抗肿瘤作用。CPM数据库监测数据显示,2020年6月,江苏恒瑞将法米替尼单药用于治疗经过伊马替尼治疗失败的晚期胃肠道间质瘤的临床申请获得默示许可,同年9月12日第一例受试者入组。目前,该Ⅲ期临床试验仍处于患者招募状态。
Crenolanib是Arog Pharmaceuticals公司开发的PDGFRα D842V 突变特异性抑制剂,先前的剂量爬坡试验结果表明,crenolanib治疗PDGFRα D842V突变晚期GIST患者有31%获得临床益处。在总共接受治疗的16例患者当中,2例患者达到了PR,3例患者达到了SD。基于以上研究成果,crenolanib治疗PDGFRα D842V突变GIST患者开启了Ⅲ期临床试验。目前,该临床试验患者招募已完成,预计试验结束时间是2021年8月。






 个人中心
个人中心
 我是园区
我是园区




