

 长按二维码报名参加!
长按二维码报名参加!

在相当长的时间内,两性生物的繁衍都离不开生殖细胞以及生殖系统。对于人类,精子和卵子的结合是生命的起点,随后受精卵进行迁移进入子宫后,生命开始被孕育。随着技术的发展,这种自然的生殖体系被打破,这项新的技术就是经常被提起的干细胞技术。
在受精卵开始发育的时候,其中任何一个细胞都具有发育成完整个体的潜力,这些细胞被我们称之为胚胎干细胞(全能干细胞的一种)。在适当的条件下,这些细胞可以分化成人类所需要的任何一种细胞。
“不用精子卵子子宫科学家培育出胚胎”冲上了热搜,这实际上是近期发表在国际顶级期刊《细胞》上的一项新研究:科学家通过小鼠胚胎中获取的胚胎干细胞,经过诱导分化后可以形成不同的胚胎细胞系,随后放到一起时可以有效结合,并在人造子宫中发育出大脑、心脏以及消化系统,最终形成具有活力的新的小鼠胚胎。这一新的重磅进展有望为多种疾病带来新的治疗希望。

该文章封面 | 图片来源:《细胞》杂志官网
在这项研究中,研究人员首先从小鼠的胚胎中获取了胚胎干细胞,随后通过干细胞诱导技术使其分化成具有不同分化方向的细胞,在培养5天后,这些细胞已经发育到足够合成胚胎的情形(不过相对来说,适合用于移植的培养的细胞概率为千分之五—)。
随后这些细胞被移植到一个新搭建起来的电子设备平台,用作给自然胚胎宫外生长提供发育所需的理想条件,在这里小鼠的原肠胚可以生成全胚胎模型,包括胚胎和胚胎外隔室。在人工搭建的“电子子宫”中,这些细胞可以继续发育。
3天后,这些细胞达到了一个发育的里程碑时间点,包括大脑、心脏以及消化系统已经发育,同时通过相应的基因表达数据进行分析后发现,这些合成的胚胎和天然的胚胎有着高度的相似性,可以表达生长发育中表达的重要生物标志物,并且和正常发育年龄表达的标志物相同。
这意味着胚胎干细胞在合适的人工子宫条件下可以形成自我组织并重建和模拟整个哺乳动物胚胎的潜力。
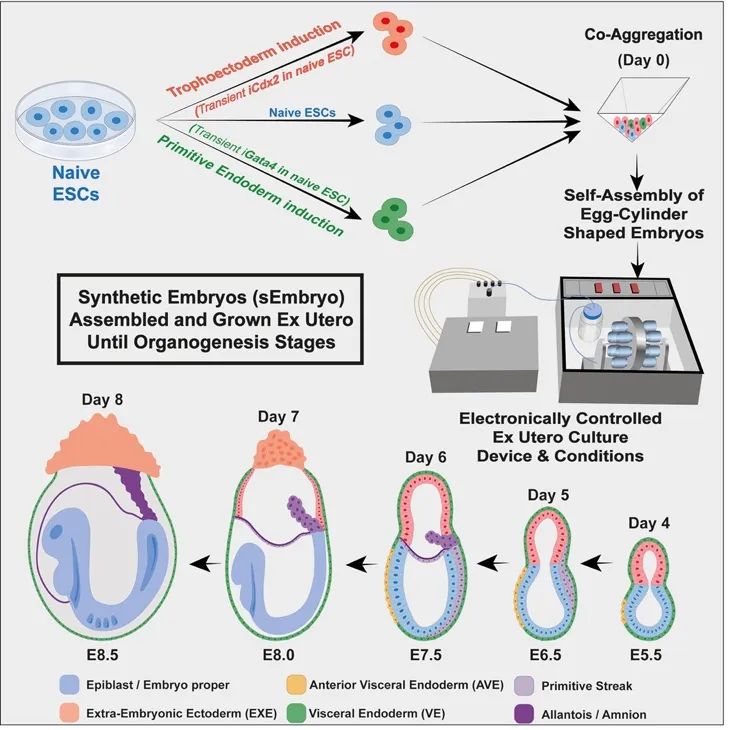
实验的整个过程,在人工子宫中具有不同分化倾向的细胞可以重新组合并发育成完整的胚胎 | 图片来源:Post-Gastrulation Synthetic Embryos Generated Ex Utero from Mouse Naïve ESCs
从研究胚胎构建的角度看,可以有助于了解人类是如何发育并最终发育成现在的历程;同时,这项技术展示了一个新的可能性:可以通过将人类的皮肤或者其他组织的细胞转化成干细胞,而后通过这项技术将细胞培养和分化成任何我们需要的细胞或者器官,这不仅可以用于器官移植,还可以用于多种疾病治疗(比如需要进行骨髓移植的血液肿瘤患者)。
尽管这项技术看起来非常好,但是不可否认的是:这项新进展对当前的伦理提出了巨大的挑战。
一方面,当干细胞衍生胚胎有着进一步的发育能力,是否会有越来越多的合成胚胎和天然胚胎的出现?而合成胚胎和融合胚胎对后续的发育和社会地位存在怎样的影响?
另一方面,通过干细胞技术我们是否可以直接合成一个生物,本次的研究已经展现出了这样的潜力,人类是否会把自己塑造成另一个上帝?
目前,暂时没有法律或者约定俗成的事情来进行规定,因此这些灰色地带需要科学家和社会团结起来共同确定界限在哪里。
很多技术的发展初衷是为了人类可以生活得更好,但是技术进展同样也会带来很多的问题,只有解决了技术带来的问题和人类社伦理会层面的冲突,才能让技术更好地为人类服务,而不是给人类带来生存的灾难。
作者:CellPlus
审校:Coco

推荐阅读
-
半年营收超10亿,复宏汉霖半年报业绩亮眼,彰显Biopharma实力 -
国外「三足鼎立」,国内「遍地开花」,拥挤的CD47赛道,有人坚守,有人退出,风口过后,未来将何去何从?
-
中国需要自己的Flagship,多玛医药能做到吗?——专访多玛医药首席运营官黄蕤博士 -
手握创新药项目的你,需要帮助吗?诺和诺德携手ATLATL为你点亮「星起点」...
-
在雷尼替丁的相关争议中,GSK放弃与Ideaya的一项实体瘤合作 -
Seagen终审败诉,默沙东恐成赢家? -
FDA对中国药企的要求合理吗?过分吗?先来看看FDA自己发布的统计数据 | 欢迎投票发声!| 药时代出海系列
-
“最贵药物”Zolgensma出现两名儿童死亡,基因疗法面临新挑战
-
又一个首款!FDA加快批准Enhertu(DS-8201)治疗HER2突变非小细胞肺癌患者 -
药企们的「过冬」策略,裁员不尽兴,他还要收租... -
Aβ假说“被锤”后,离开4年的默沙东又被勾回来,买了一个连靶点都不知道的产品...
-
54亿美金,买!歇了不到3个月的辉瑞,又开始溢价收购了... -
104家中国新药企业扬帆出海!ADC赛道喜讯频传!科伦博泰势头赶超老大哥石药 | 药时代出海系列 -
对话RNA靶向新兴企业施能康(SynerK):从Alnylam公司APOLLO-B的成功看RNAi药物的研发
 点击这里,报名参加第三届中国新药CMC高峰论坛!
点击这里,报名参加第三届中国新药CMC高峰论坛!



 个人中心
个人中心
 我是园区
我是园区





