8月23日,Foghorn Therapeutics宣布,FDA已全面暂停BRG1/BRM抑制剂FHD-286在复发和/或难治急性髓细胞白血病(AML)和骨髓增生异常综合征(MDS)中的I期剂量递增研究。Foghorn的股价周一收于14.59美元,但在盘前交易中下跌超过30%,至10.27美元。

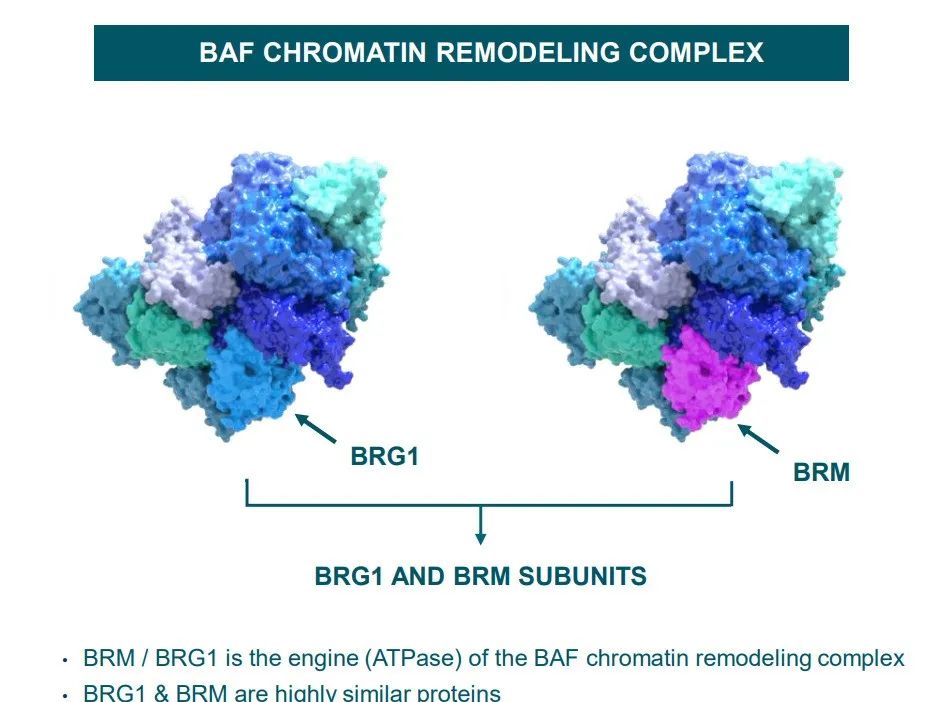
FHD-286是一款口服有效、选择性的BAF复合体BRG1/BRM亚基的变构小分子抑制剂。BAF是一种研究透彻的染色质重塑复合物。BRG1和BRM是高度相似的蛋白质,这两种蛋白质是BAF染色质重塑复合物的ATP酶,是染色体调节系统的关键调节剂之一。
在临床前研究中,FHD-286已表现出抗肿瘤活性。

今年5月,Foghorn报告了一例潜在分化综合征患者死亡事件,FDA因此部分暂停了FHD-286在AML和MDS中的I期研究。此次FDA全面暂停这项研究,是因为出现了其他疑似致命分化综合征病例。
分化综合征是由于癌症治疗影响的白细胞快速释放大量细胞因子引起的。临床表现为发热、体重增加、呼吸窘迫、心包积液、皮肤水肿、血压低、急性肾衰竭甚至死亡。Foghorn表示,分化综合征与诱导分化的AML/MDS治疗相关,被认为是FHD-286的靶向机制。
FDA要求对数据进行全面分析,然后才能解除暂停,并允许剂量递增研究继续进行。该公司最初计划在2022年底之前提供这项研究的数据。然而,随着临床的完全暂停,不太可能实现这项计划。
Foghorn首席执行官Adrian Gottschalk表示:“我们致力于患者的安全,并将与FDA合作,解决该机构的问题,并提供进一步的分析,以尽快解决临床暂停问题。
虽然FHD-286在AML和MDS的研究被暂停了,但Foghorn指出,FHD-286在另一项适应症转移性葡萄膜黑色素瘤(一种罕见的眼癌)中的剂量递增研究将继续按照方案进行。在美国,每年约有2000名成年人被诊断出葡萄膜黑色素瘤。该疾病在大约50%的病例中发生转移,导致预后非常差。I期研究的数据预计将于2023年上半年公布。




 个人中心
个人中心
 我是园区
我是园区




