美国 FDA 于 10 月 5 日在《联邦公报》上公布了各类使用者付费项目(UFA)2023 财年(2022年10月1日至2023年9月30日)的费率。
今年情况比较特殊,支持各项 UFA 重新授权的法案在最后关头 9 月 30 日才在国会通过并由总统最终签署成为法律。这直接导致的后果就是 2023 财年已经开始,FDA 才匆匆根据重新授权法案发布本财年的收费标准。正常情况下,FDA 一般在前一财年的 7 月末公布下一财年的费率,以给企业充足的准备时间。因此,FDA 在公布费率的文件中给出了付费时限的说明,“鉴于 2023 至 2027 财年 GDUFA 重新授权的日期较晚,(相关企业)应在通知发布之日起 30 天内支付 2023 财年的场地和项目费。”
下面我们重点来看看仿制药使用者付费重新授权(GDUFA III)的费率。首先,GDUFA III 的收费结构与 GDUFA II 相比大体一致,仅有细微的组成变化,如下表所示, API 场地费从 GDUFA II 占比 7% 下降至 GDUFA III 的占比 6%,ANDA 项目费则从 35% 升至 36%。
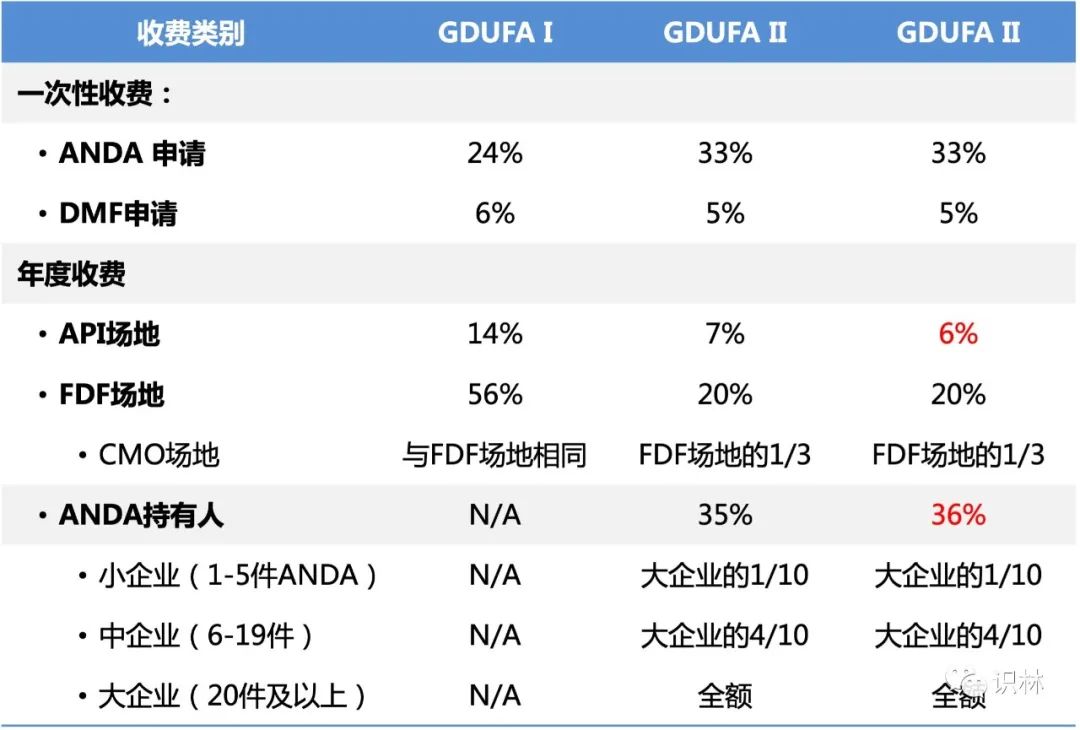
GDUFA 与去年差别显著,申请费、制剂场地费和 ANDA 项目费都有所上涨,但涨幅不大。原料药生产场地由于总占比下降 1%,因此费率也有所下降。
下表列出了 2023 财年新费率于 2020 财年费率的比较。
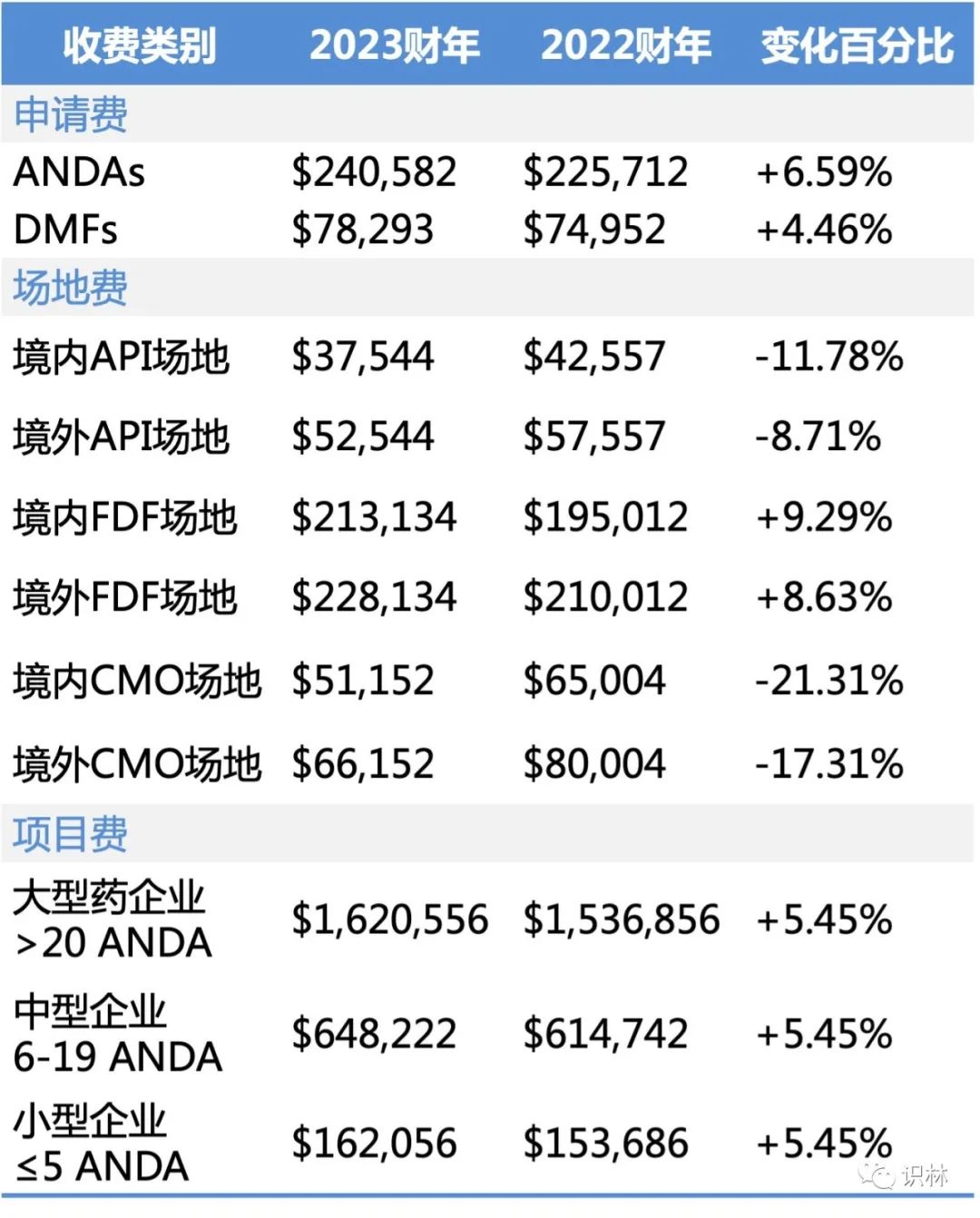
FDA 利用 2020 年 10 月 1 日至 2022 年 4 月 30 日提交的 ANDA 数据来预估将在 2023 财年产生申请费的新院士 ANDA 数量。2023 财年 FDA 预估需要缴费的 ANDA 数量大约为 800 件新原始 ANDA,但并非所有新原始 ANDA 都会被 FDA 接收,一些未被接收的 ANDA 将在同一财年度重新提交,因此 FDA 预计 2023 财年的等效 ANDA 数量未 799 件,这与 2022 财年的预估(789 件)基本持平。
合同生产(CMO)场地的费率有较大幅度的下降,可能是因为 CMO 场地预估数量比 2022 财年相比略有增加。
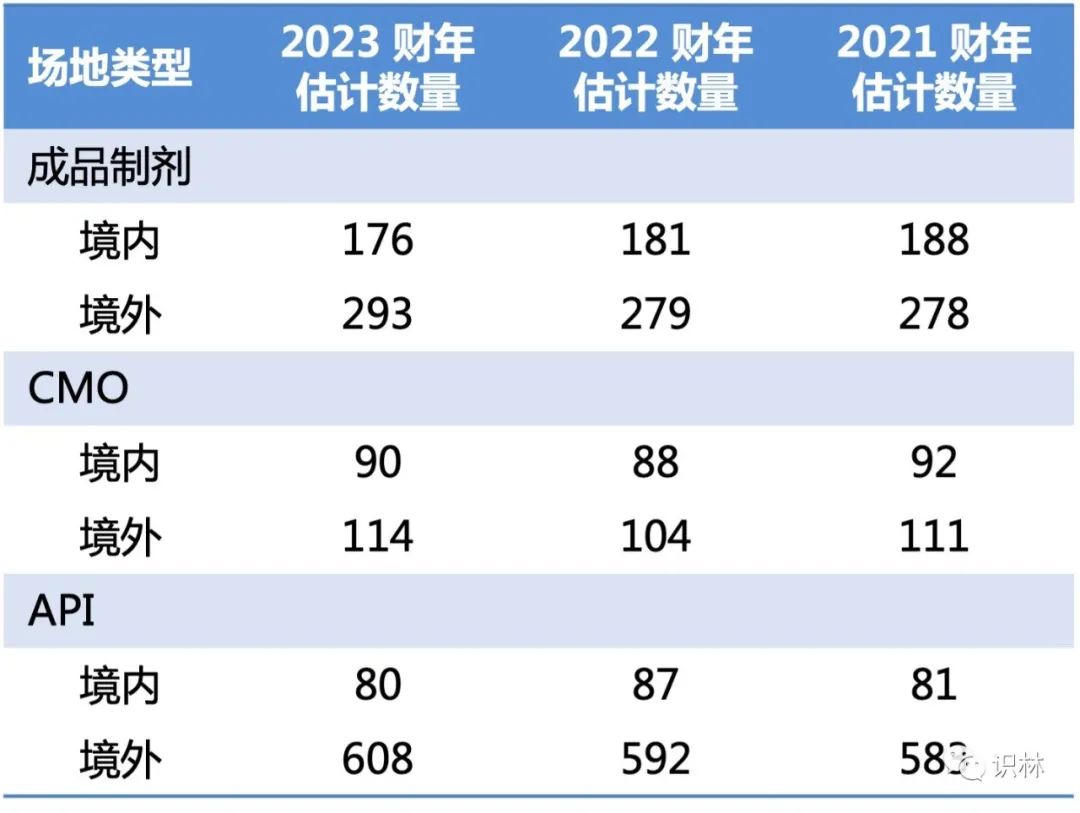
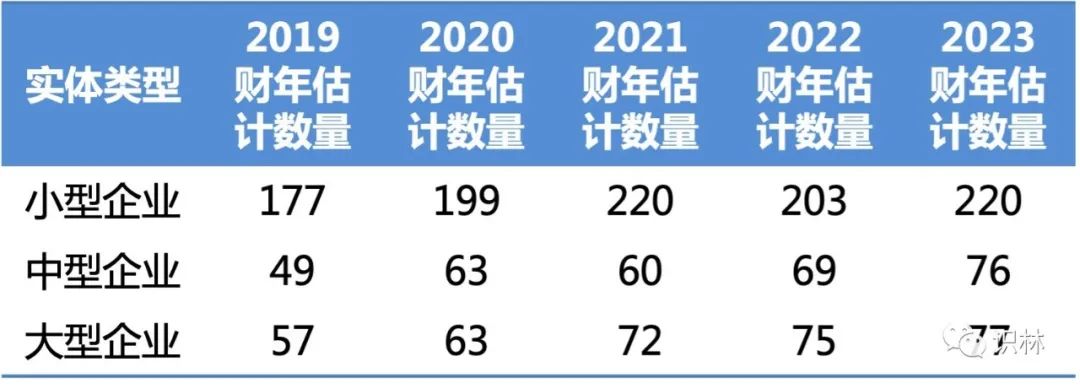
项目费方面,FDA 估计的 2023 财年大中小型企业数量与前一财年相比均有所增加(见下表),但由于项目费占比升高 1%,所以 2023 财年的项目费也略有增加。
作者:识林-椒
点击下方卡片,快速绑定/注册识林小程序
长按下方二维码下载识林®App

识林®版权所有,未经许可不得转载



 个人中心
个人中心
 我是园区
我是园区




