12 月 8 日,根据 CDE 临床试验登记平台,恒瑞医药 SHR-1901 首次启动临床试验。据临床试验方案,这是一款皮下注射 PD-1 单抗,也是恒瑞的第 2 款 PD-1 单抗。临床试验详情
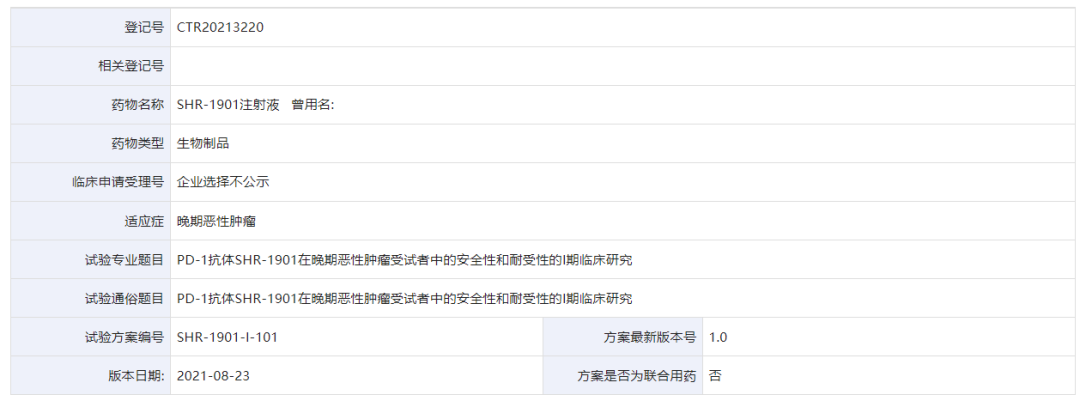
Insight 数据库显示,SHR-1901 在今年 6 月首次申报临床,8 月获批临床。
相较于注射剂,皮下注射制剂独具依从性优势,给药快、便捷性高,可将给药时间从数小时缩短到 3 至 5 分钟,甚至以秒计。11 月 25 日,康宁杰瑞/思路迪/先声药业的全球首款皮下注射 PD-L1 才刚刚获批上市,今日首批处方刚刚落地。据企业新闻稿,恩维达®可在 30 秒完成给药,还可应用于静脉注射不耐受的患者。
罗氏也曾在曲妥珠单抗皮下制剂的开发中做过患者偏好性试验 PrefHER,240 名患者接受辅助 Herceptin Hylecta 治疗、随后接受静脉曲妥珠单抗治疗,或者以相反顺序。结果显示,86% 的试验患者首选皮下方案。
恒瑞的卡瑞利珠单抗仍是国内 PD-1 单抗中销售额领先的产品,不过 2021 年屡遭挫折,先是因医保降价、进院难等因素导致销售额环比下滑,后在 2021 最新医保谈判中又未将新适应症谈进医保。开发第二款 PD-1 单抗一方面可以借助恒瑞优秀的医学团队以及过往开发 PD-1 积累的经验而实现快速推进;另一方面,通过皮下注射制剂的方式杀出重围不失为一种破局之策。
目前,国内尚无其他企业将 PD-1 皮下注射剂推入临床。而从全球维度来看,辉瑞同样也开发了一款皮下注射 PD-1 单抗 sasanlimab (PF-06801591),已经进入到 3 期临床,联合卡介苗治疗高危非肌层浸润性膀胱癌。这项临床试验今年 7 月也已经在国内启动(点此跳转临床试验详情)。
辉瑞最新肿瘤管线
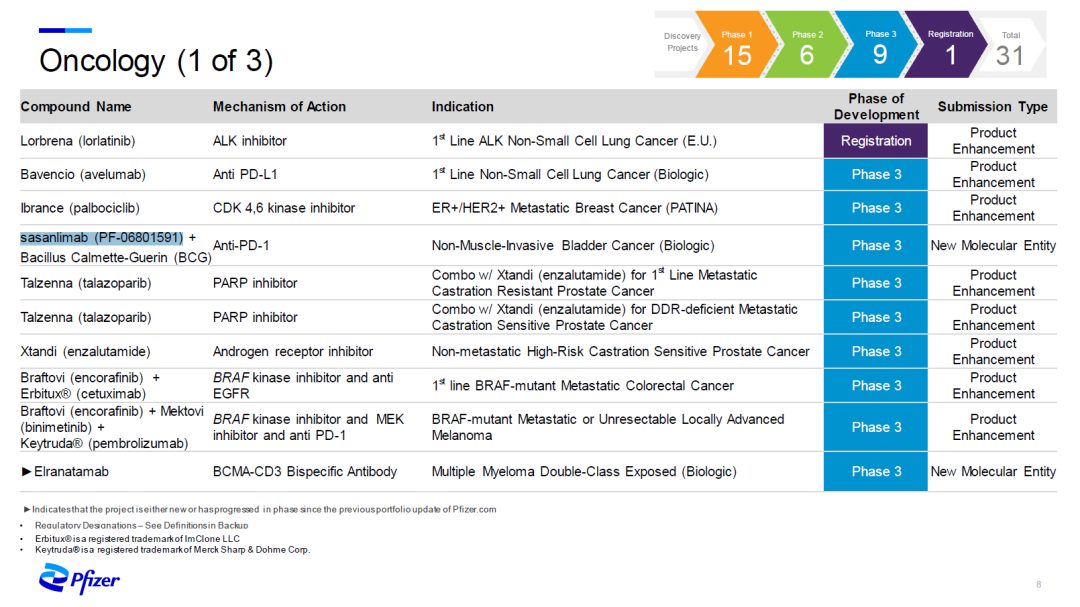
来自:辉瑞 Q3 管线更新 PPT,公众号回复「辉瑞2021Q3」即可下载
Sasanlimab 目前已经公布了 1 期临床数据。在 2020 ESMO 会议上,辉瑞更新了在非小细胞肺癌(NSCLC)及尿路上皮癌(UC)患者中的 1 期首次人体临床研究数据(NCT02573259)。
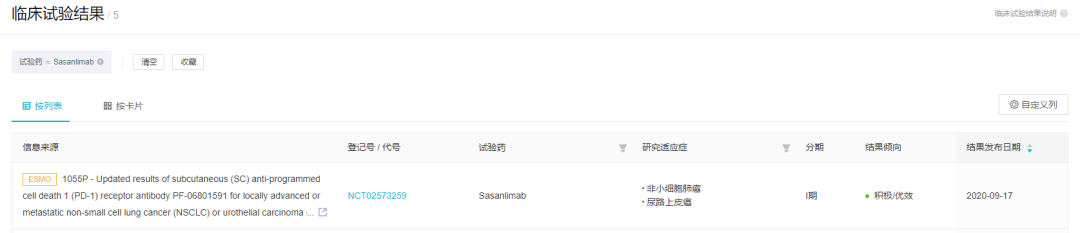
来自:Insight 临床结果库(http://db.dxy.cn/v5/home/)
截至 2019 年 11 月 1 日,在 106 位入组患者中(NSCLC=68,UC=38)中,中位治疗持续时间为 113.0 天。疗效数据来看,在 mITT NSCLC 人群中 20.9% 达到 PR、35.8% SD,ORR 为 20.9%(95%CI: 11.9-32.6);在 PD-L1 表达 ≥1% 和 ≥ 50% 的患者中 ORR 分别为 32.1% 和 45.5%。在 mITT UC 人群中 21.1% 达到 PR(中位持续时间:183.0 天),31.6% SD(中位持续时间:118.5 天),ORR 为 21.1%(95%CI: 9.6-37.3%),而在 PD-L1 表达 ≥1% 和 ≥ 50% 的患者中 ORR 则分别为 40.0% 和 50.0%。
在开发 Sasanlimab 之前,辉瑞也已经有一款与默克合作的 PD-L1 单抗阿维鲁单抗(avelumab),2017 年已经获 FDA 批准上市,商品名为 Bavencio®。这款产品陆续在肾细胞癌、尿路上皮癌、Merkel 细胞癌 3 个癌种上获得了批准。不过作为市场后来者,PD-L1 领域还是主要被罗氏(阿替利珠单抗)和阿斯利康(度伐利尤单抗)所占据。
免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
编辑:加一
PR 稿对接:微信 insightxb
投稿:微信 insightxb;邮箱 insight@dxy.cn
点击卡片进入 Insight 小程序
药品申报、临床、上市、一致性评价…
随时随地查!
↓↓ 点击解锁更多新功能



 个人中心
个人中心
 我是园区
我是园区




