▲点击上方的蓝色“医谷”关注我们

近日,苏州新芽基因生物技术有限公司(以下简称“新芽基因”)宣布,其首个碱基编辑产品GEN6050 向FDA提交pre-IND申请并被受理。
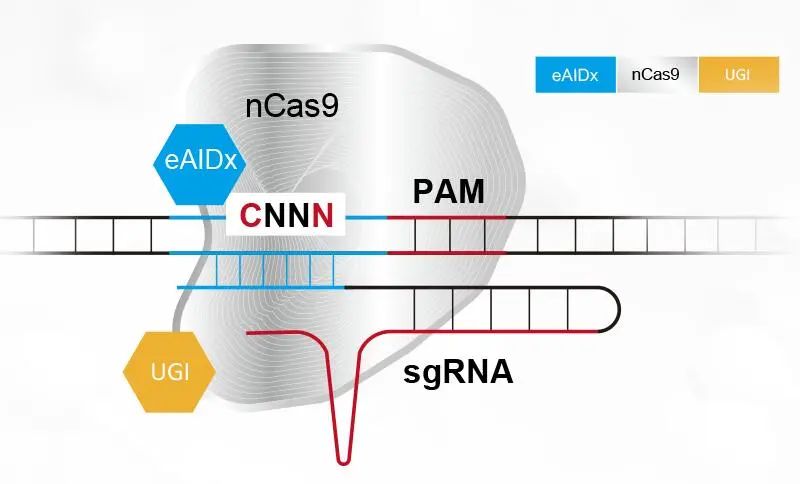
新芽基因成立于2020年7月,致力于基因编辑药物研发,拥有碱基编辑器TAM全球权利,该技术来自于中国科学院营养与健康研究所和西湖大学授权。官网信息显示,其TAM BE (Targeted AID-mediated Mutagenesis Base Editor) 碱基编辑器技术平台是基于活化B细胞中激活诱导的脱氨酶(AID)高活性变体为基础开发而成的胞嘧啶脱氨酶。在sgRNA的引导下,TAM BE能在特定位点实现C>T, G>A的转换。
目前,新芽基因已经建立相应的碱基编辑药物体内外评价系统,正在针对DMD开发一系列的产品。GEN6050是一款针对杜氏肌营养不良(Duchenne muscular dystrophy,DMD)基因外显子50跳跃可治疗的体内碱基编辑药物,旨在通过碱基编辑,达到DMD基因外显子50跳跃,恢复抗肌萎缩蛋白的表达。DMD是发病率较高的罕见病,每4000个新生男婴就一例DMD患者。根据LEIDEN DMD数据显示外显子50跳跃可用于4%的大片段缺失DMD患者治疗。目前针对DMD的上市药物有糖皮质激素和ASO药物。ASO药物针对的外显子跳跃包括45,51,53。目前尚未有针对抗肌萎缩蛋白基因外显子50跳跃的药物在临床。此外,截至目前,全球也尚未有针对其他适应症的体内碱基编辑药物进入临床。
2022年12月,新芽基因宣布完成数千万美元A轮融资,阿斯利康中金医疗产业基金领投,BV百度风投和某知名股权投资机构跟投,老股东红杉中国持续追加投资,泰合资本担任独家财务顾问。融资资金将主要用于推进新芽基因多个碱基编辑技术治疗管线的临床前研究、IND申报和临床试验。
推荐阅读


寻求广告投放、会议合作、企业传播等请联系400-689-7892。



 个人中心
个人中心
 我是园区
我是园区





