晚期肺鳞癌治疗需求尚未满足
免疫治疗出现开启全新治疗时代
肺癌是全球发病率和死亡率最高的恶性肿瘤之一[1]。中国是肺癌大国,发病率和死亡率均居全球之首,疾病负担沉重[1]。NSCLC约占肺癌的80%~85%,肺鳞癌约占NSCLC的25%~30%,是NSCLC的第二大亚型。我国多数NSCLC患者确诊时已为晚期,失去了手术机会,晚期患者5年总生存(OS)率不超过5%[2]。有效的系统治疗成为改善晚期NSCLC患者预后的主要手段和希望。
近20年来,相较于非鳞癌,鳞癌系统治疗进展缓慢,非鳞癌常见的表皮生长因子受体(EGFR)、ALK等驱动基因突变在鳞癌中发生率极低,仅约为5%左右,腺癌则高达68.3%[3]。有效驱动基因靶点的缺乏使肺鳞癌靶向治疗举步维艰。在免疫治疗探索成功以前,晚期肺鳞癌系统治疗仅以含铂化疗为主,方案选择和疗效均十分有限,总体预后差,临床治疗需求亟待满足。鉴于我国肺鳞癌庞大的患者基数,要提高中国肺癌患者总体预后,实现《“健康中国2030”规划纲要》中癌症5年总生存率提升的总体目标,晚期肺鳞癌的治疗突破迫在眉睫。
KEYNOTE-407研究[4-5]奠定了免疫治疗联合化疗在晚期肺鳞癌一线治疗的地位,美国国立综合癌症网络(NCCN)、欧洲肿瘤内科学会(ESMO)及中国临床肿瘤学会(CSCO)等国内外权威指南自2019年起就已将PD-1单抗联合卡铂+紫杉醇/白蛋白紫杉醇作为晚期肺鳞癌一线治疗推荐。但一方面,国内可用的免疫治疗药物种类及可及性仍十分有限,远不能满足广大的临床需求;同时,KEYNOTE-407研究纳入的中国患者数量少,中国的晚期肺鳞癌患者亟需中国研究探索免疫治疗的获益。
基于RATIONALE 307研究的成功,替雷利珠单抗用于晚期肺鳞癌一线治疗新适应症在国内获批,以大样本的中国患者数据和民族品牌药物良好的可及性率先填补了中国肺鳞癌免疫治疗的空白,为中国临床医生再添有力武器,为中国肺鳞癌患者带来了全新治疗选择。
替雷利珠单抗循证医学证据充分
获批上市惠及中国肺癌患者
替雷利珠单抗是目前唯一对Fc段进行了特殊基因工程改造的PD-1单抗,可更大限度减少Fc段与巨噬细胞上FcγR 结合,避免抗体依赖的细胞介导的吞噬作用(ADCP),从而减少活化T细胞消耗、增强抗肿瘤活性,潜在减少耐药发生[6-7]。此外,替雷利珠单抗Fab段具有独特的PD-1结合表位,其较帕博利珠单抗和纳武利尤单抗对PD-1的亲和力更高,解离速率更慢,可更彻底、持久地阻断PD-1与PD-L1结合[6、8]。
RATIONALE 307研究是一项针对晚期肺鳞癌患者一线免疫治疗的随机、开放、多中心大型Ⅲ期注册临床研究,其结果先后亮相于2020年ASCO、ESMO、CSCO及NACLC等多项全球顶级肿瘤学术大会,以大样本中国患者数据确证了替雷利珠单抗联合紫杉醇/白蛋白紫杉醇+卡铂方案显著优于单纯化疗方案的有效性和可靠的安全性,如图1所示。
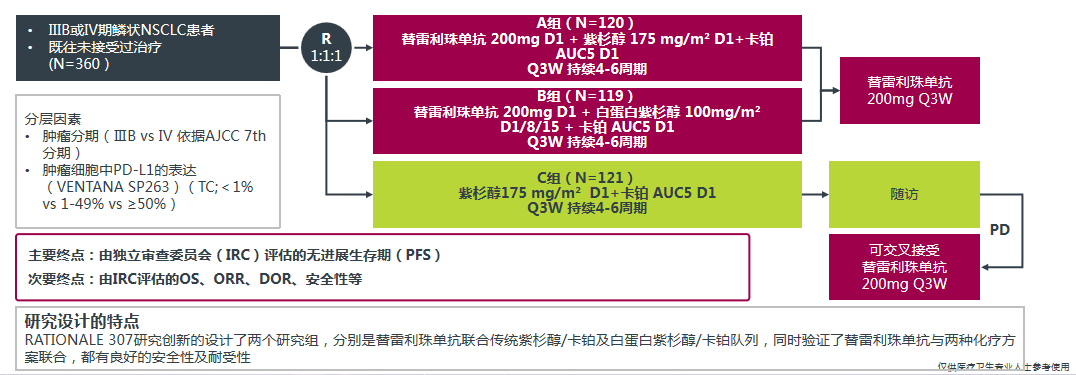
图1 RATIONALE 307研究设计
RATIONALE 307研究共纳入360例ⅢB~Ⅳ期初治肺鳞癌患者,随机分配进入替雷利珠单抗+紫杉醇+卡铂组(A组、120例)、替雷利珠单抗+白蛋白紫杉醇+卡铂组(B组、119例)和紫杉醇+卡铂组(C组、121例)。结果如图2所示,相较于C组,A组和B组在主要终点中位无进展生存期(PFS)上均显著延长[7.6个月对5.5个月,风险比(HR)=0.52,P=0.0001;7.6个月对5.5个月,HR=0.48,P<0.0001],A组和B组分别显著降低患者疾病进展风险48%和52%。次要终点客观缓解率(ORR)的数据尤为惊艳,A组和B组分别达到72.5%和74.8%(C组为49.6%),替雷利珠单抗治疗的缓解比例比肩靶向治疗,让更多患者能够从免疫治疗中获益;中位缓解持续时间(DoR)方面,A组和B组分别为8.2个月和8.6个月,达单用化疗C组4.2个月的两倍左右,可见患者接受替雷利珠单抗治疗能够持续获益。
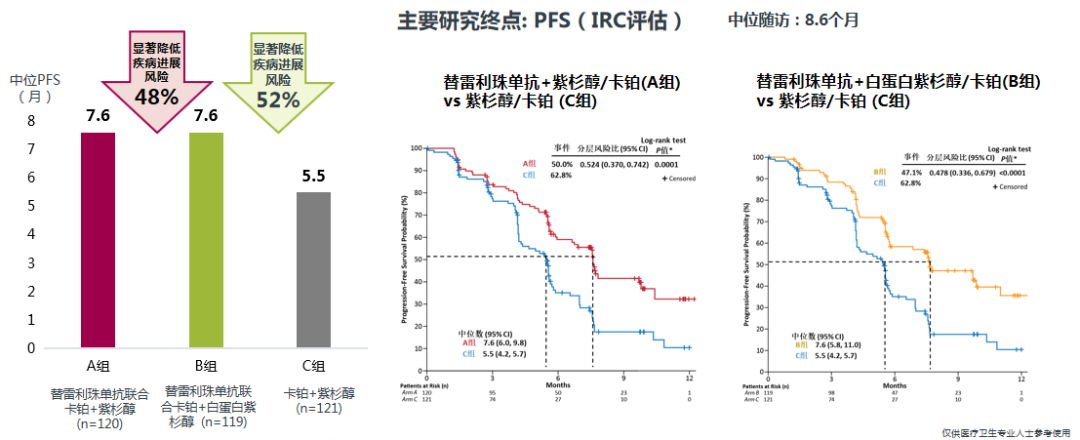
图2 RATIONALE 307研究主要结果
亚组分析数据提示,无论患者年龄、性别、ECOG PS评分、吸烟状态、肿瘤分期、是否伴肝转移及PD-L1表达状态,替雷利珠单抗联合化疗均能显著延长患者PFS。且总体安全性和耐受性均良好,未发现新的安全性信号。患者接受替雷利珠单抗联合化疗方案治疗后,咳嗽、呼吸困难、咯血等症状改善明显,患者生活质量显著提升。
替雷利珠单抗基于结构优化创新的强效抗肿瘤作用在RATIONALE 307研究中得到了充分体现和印证,此项研究更获得了2020年CSCO优秀论文一等奖的荣誉,并在CSCO大会上得到“RATIONALE 307研究建立肺鳞癌中国一线治疗新标准”的高度评价,为获批上市后的广泛临床应用奠定了坚实基础。
除了肺鳞癌领域的突破之外,替雷利珠单抗用于非鳞状NSCLC一线治疗的RATIONALE 304研究也已于去年同期获得了成功,结果同样令人鼓舞!在2020年ESMO大会上公布的中期分析数据显示:替雷利珠单抗联合化疗方案一线治疗晚期非鳞状NSCLC疗效显著、安全性良好:独立影像评估(IRC)的中位PFS达到9.7个月,研究者评估的患者疾病进展风险显著降低44%;57%的患者达到客观缓解,对比化疗组获益患者增加一半以上;患者的中位DoR对比化疗组延长了42%,达到8.5个月。
NMPA也已于2020年6月正式受理了替雷利珠单抗联合化疗用于一线治疗非鳞状NSCLC患者的新适应症上市申请,获批指日可待,替雷利珠单抗也有望成为首个同时获批一线治疗晚期鳞状及非鳞状NSCLC的国内自主研发的PD-1/PD-L1抗体药物。
2020年11月,替雷利珠单抗单药对比多西他赛二/三线治疗局部晚期或转移性NSCLC患者的全球Ⅲ期临床试验——RATIONALE 303研究也取得了成功,在中期分析中取得了OS的阳性结果。从联合治疗到单药治疗,从晚期一线到晚期后线,替雷利珠单抗在肺癌领域披荆斩棘,连下三城。替雷利珠单抗已成为目前国内唯一在肺癌领域取得OS主要终点阳性结果的国内自主研发的PD-1/PD-L1抗体药物,同时更是目前全球唯一取得晚期NSCLC一线联合化疗及二线单药治疗全人群获益的PD-1/PD-L1抗体药物!
除了肺癌领域不断突破之外,替雷利珠单抗前期已获批的经典型霍奇金淋巴瘤和尿路上皮癌相应适应症也已于2020年12月纳入国家医保药品目录,可及性有望进一步提高。同时,替雷利珠单抗在肝癌、食管癌、胃癌、鼻咽癌等领域的多项国际/国内多中心临床研究也在积极开展中,为更广泛的瘤种探索证据,为更广大的中国乃至世界肿瘤病患谋求福祉!
百济神州战略携手诺华
本土抗癌新药再创“出海”里程碑
作为植根中国、面向全球的生物制药企业,百济神州始终坚持循着自主研发的全球化发展道路前行。作为百济神州的第一个重大创新抗肿瘤优秀药物,替雷利珠单抗在中国临床已取得了瞩目成绩,目前替雷利珠单抗共有15项注册性临床试验在全球开展,已在全球入组7700余例患者。
为了将中国的自主研发成果加速推向世界舞台、领跑国际,也为了惠及全球广大的肿瘤患者,2021年1月12日,百济神州与诺华公司正式达成了替雷利珠单抗在多个国家的开发、生产及商业化合作与授权,首付款高达6.5亿美元,总交易金额超过22亿美元,创下目前国内单品种药物授权交易金额最高记录。这是继2019年泽布替尼在美国获得食品药品监督管理局(FDA)批准上市、实现“零的突破”后,百济神州创造的本土抗癌新药“出海”的又一里程碑事件。
全球制药巨头诺华选择与百济神州携手,既是对百济神州坚持走自主研发的全球化发展道路及公司研发实力的巨大认可,也是对替雷利珠单抗作为一款与众不同的全球高品质PD-1单抗的肯定,更为中国制药树立了坚持走全球化创新之路的信心。此次合作是中国本土创新药企崛起与壮大的有力写照,更是中国制药的全球化创新之路已经迈入了新时代的重要里程碑事件!替雷利珠单抗的出海,将让全球的肿瘤患者有望用上高品质的中国创新药物,让中国智慧闪耀全球,中国好药惠泽众生!



 个人中心
个人中心
 我是园区
我是园区




