您还不是认证园区!
赶快前去认证园区吧!

7月14日,Alkeus宣布FDA授予ALK-001(C20-D3-维生素A)突破性疗法称号,用于治疗斯特格氏病。目前,尚无批准的斯特格氏病治疗药物。ALK-001 是唯一获得斯特格氏病突破性疗法认定的药物。
斯特格氏病是一种罕见的遗传性视网膜退行性疾病,会导致视力不可逆的丧失,最终失明。美国国立卫生研究院预计斯特格氏病的患病率为1/8,000至1/10,000,美国和欧洲五国约有62,000-77,000例患者。症状通常开始于儿童期或青春期,出现黄斑椭圆形萎缩区及其周围视网膜的黄色斑点。
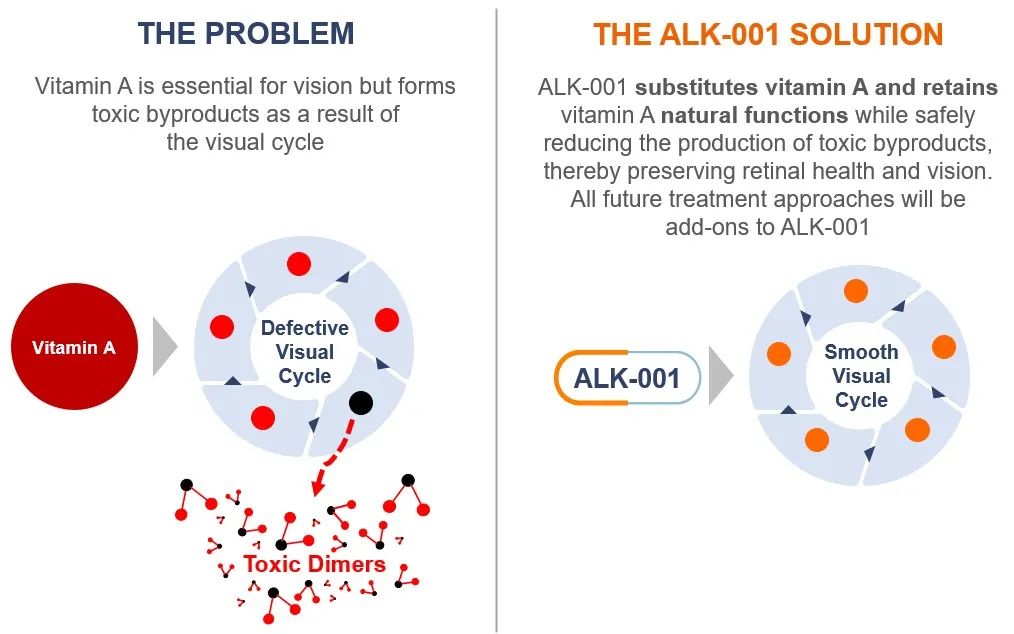
ALK-001是一种维生素A的化学修饰形式,通过替代维生素A并保留其天然功能来减少有毒维生素 A 脂褐素的的产生,每日一次口服给药。临床数据表明,ALK-001可以安全地减缓斯特格氏病的进展,同时保持正常的视觉周期。
Alkeus Pharmaceuticals 首席执行官 Leonide Saad 博士说:“获得突破性疗法认定是斯特格氏病的一个重要里程碑,我们II期试验的结果为 ALK-001治疗斯特格氏病的监管备案和批准提供了强有力的基础。我们期待与 FDA 及其他监管机构合作,以便我们能够尽快将 ALK-001带给患者。”





 个人中心
个人中心
 我是园区
我是园区




