“肾癌文献月评”秉承传递最新医学进展的理念已陪伴大家一年,如今改版归来,再次扬帆起航!中华医学会泌尿外科学分会(CUA)青年委员会点评组将继续围绕肾癌药物、手术、基础研究、诊断学等相关内容,以专业视角,多维度关注、分析肾癌领域学术成果,以期为各位同道带来帮助。本期为肾癌文献月评2021~2022年度第一期。
本期汇总2021年3月~6月发表的肾癌领域文献,精选其中3篇高水平热点研究,包括晚期肾癌的药物治疗临床研究,以及多囊肾向透明细胞肾细胞癌转化方面的研究,由第二军医大学第三附属医院崔心刚教授、北京大学第三医院张树栋教授、中山大学孙逸仙纪念医院董文教授进行点评。
本期导览
(1)仑伐替尼联合帕博利珠单抗或依维莫司一线治疗晚期肾细胞癌;
(2)Belzutifan(HIF-2α)治疗肾细胞癌的Ⅰ期临床研究和生物标志物分析;
(3)SETD2对β-连环蛋白活性的多层次调节,抑制多囊性肾病向透明细胞肾细胞癌转变。
(1)仑伐替尼联合帕博利珠单抗或依维莫司一线治疗晚期肾细胞癌

背景:仑伐替尼联合帕博利珠单抗或依维莫司治疗晚期肾细胞癌,在先前的研究中显示出一定的疗效,但尚不清楚和舒尼替尼治疗方案间的疗效差异。
方法:在这项Ⅲ期试验中,纳入了既往未接受过全身治疗的晚期肾细胞癌患者,按1:1:1的比例随机接受以下三种治疗方案:(1)仑伐替尼(20 mg,口服,每日1次)联合帕博利珠单抗(200 mg,静脉注射,每3周1次);(2)仑伐替尼(18 mg,口服,每日1次)联合依维莫司(5 mg,口服,每日1次);(3)舒尼替尼(50 mg,口服,每日1次,交替4周接受治疗和2周不接受治疗)。主要终点为无进展生存期(PFS),此外还评估了总生存期(OS)和安全性。
结果:共1069例患者随机接受仑伐替尼联合帕博利珠单抗(355例)、仑伐替尼联合依维莫司(357例)或舒尼替尼单药(357例)治疗。
PFS:相较舒尼替尼单药治疗组,仑伐替尼联合帕博利珠单抗治疗组(23.9个月 vs 9.2个月;HR=0.39;95% CI:0.32-0.49;P < 0.001)和仑伐替尼联合依维莫司治疗组(14.7个月 vs 9.2个月;HR=0.65;95% CI:0.53-0.80;P < 0.001)的中位PFS均显著延长(图1)。
OS:相较舒尼替尼单药治疗组,仑伐替尼联合帕博利珠单抗治疗组的OS显著延长(HR=0.66;95% CI:0.49-0.88;P = 0.005),但仑伐替尼联合依维莫司治疗组的OS无统计学差异(HR=1.15;95% CI:0.88-1.50;P = 0.30)(图2)。
安全性:仑伐替尼联合帕博利珠单抗治疗组、仑伐替尼联合依维莫司治疗组和舒尼替尼单药治疗组,分别有82.4%、83.1%和71.8%的患者在治疗期间出现3级及以上不良事件。常见发生率>10%的≥3级不良事件包括高血压、腹泻和脂肪酶水平升高。
结论:与舒尼替尼单药治疗相比,仑伐替尼联合帕博利珠单抗可显著延长晚期肾细胞癌患者的PFS和OS。
董文 教授
中山大学孙逸仙纪念医院
【专家简评】
KEYNOTE-581/CLEAR研究证实,相比舒尼替尼,仑伐替尼联合帕博利珠单抗/依维莫司可以显著改善晚期肾细胞癌患者的PFS及ORR。研究结果公布后,美国食品与药物管理局(FDA)迅速批准仑伐替尼联合帕博利珠单抗用于晚期肾细胞癌的一线治疗。在目前获FDA批准用于晚期肾细胞癌一线治疗的4种“酪氨酸激酶抑制剂(TKI)+免疫治疗(IO)”方案中,仑伐替尼联合帕博利珠单抗方案获得了相对最长的PFS(23.9个月)和相对最高的ORR(71%),完全缓解(CR)率高达16%。这样的结果可能与该研究纳入的中低危受试者比例较高(91.2%)相关,但不可否认的是,该组合方案将晚期肾细胞癌的预后提升到了一个新高度,特别是对于中高危患者,仑伐替尼联合帕博利珠单抗获益更为显著。
今年的美国临床肿瘤学会(ASCO)大会上,KEYNOTE-581/CLEAR研究更新了几项亚组分析数据:(1)该研究进一步探索了患者缓解程度与生存期的相关性,结果显示获得CR的患者2年生存率达到100%,意味着缓解程度越高,患者的生存期可能越长,而仑伐替尼联合帕博利珠单抗的高缓解率意味着患者的生存获益可能会进一步延长,期待未来数据成熟;(2)该研究进一步探索了危险分层与疗效的相关性,结果显示不论是低/中/高危患者,仑伐替尼联合帕博利珠单抗的PFS均显著延长,中高危患者的OS显著延长,但低危患者OS无显著差异,与其他几项“TKI+IO”的研究结论一致。需要注意的是,联合治疗的高疗效伴随的是较高的不良事件发生率,因此在选择治疗方案时需要权衡疗效与风险,为患者制定个体化治疗方案。未来如何在提高疗效的基础上减少、预防不良事件的发生,还需要不断进行临床探索和实践。
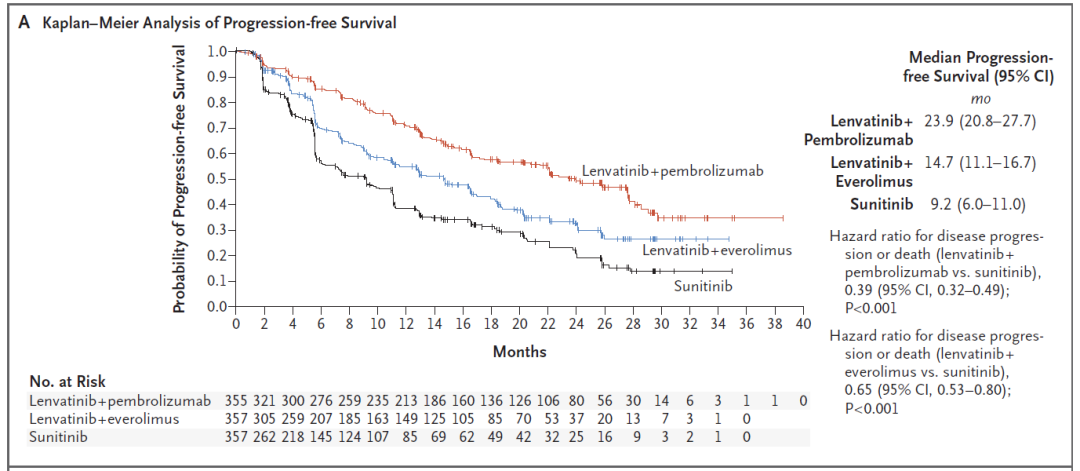
图1 每个治疗组中PFS的Kaplan-Meier曲线
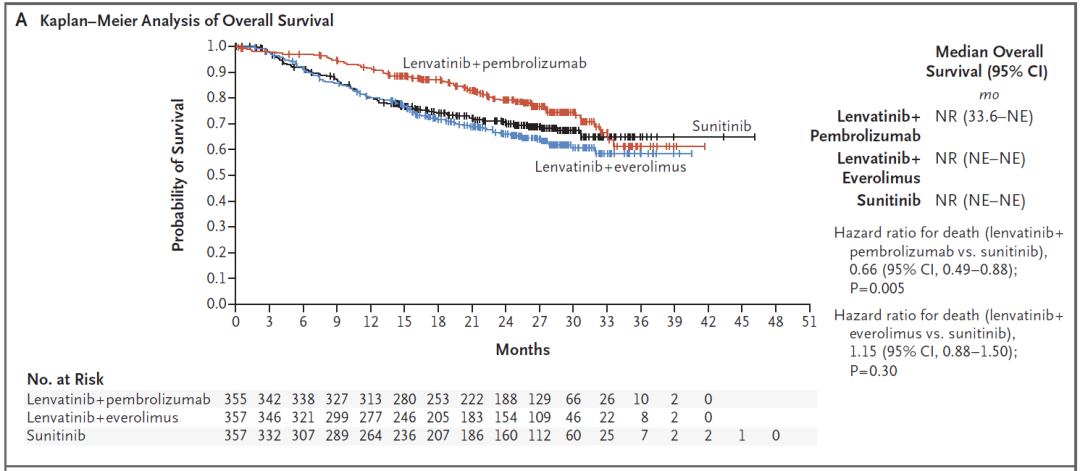
图2 每个治疗组中OS的Kaplan-Meier曲线
(2)Belzutifan(HIF-2α)治疗肾细胞癌的Ⅰ期临床研究和生物标志物分析

摘要:缺氧诱导因子-2α(HIF-2α)是一种在透明细胞肾细胞癌(ccRCC)中关键的转录因子,会导致癌变相关基因的激活。Belzutifan(MK-6482,以前称为PT2977)是一种选择性HIF-2α小分子抑制剂。在这项Ⅰ期研究中(NCT02974738),评价了belzutifan的最大耐受剂量、安全性、药代动力学、药效学和抗肿瘤活性。该研究纳入患有晚期实体瘤(剂量递增队列)或既往接受过治疗的晚期ccRCC(剂量扩展队列)患者,belzutifan口服给药方案采用“3+3剂量递增”设计,随后在ccRCC患者中以推荐的Ⅱ期剂量(RP2D)进行扩展。在剂量递增队列(n=43)中,“160 mg,每日1次”剂量组未发生剂量限制性毒性,未达到最大耐受剂量;RP2D为“120 mg,每日1次”。在所有剂量下均观察到血浆促红细胞生成素降低,且促红细胞生成素浓度与belzutifan的血浆浓度相关。在接受“120 mg,每日1次”剂量的ccRCC患者(n=55)中,确认的ORR为25% [均为部分缓解(PR)],中位PFS为14.5个月。最常见的≥3级不良事件为贫血(27%)和缺氧(16%)。Belzutifan耐受性良好,在强化预处理的患者中表现出初步的抗肿瘤活性,提示HIF-2α抑制剂可能是ccRCC的一种有效治疗方法。
张树栋 教授
北京大学第三医院
【专家简评】
希佩尔·林道(Von Hippel-Lindau,VHL)基因导致的HIF-2α水平异常是ccRCC发病的始动因素之一,HIF-2α靶向药物已成为一种潜在的ccRCC治疗策略。既往的Ⅰ期探索性研究显示,第一代HIF-2α抑制剂MK-3795耐受性良好,具有一定的抗肿瘤活性。然而,由于MK-3795对葡萄糖醛酸代谢产物的代谢广泛,导致其药代动力学受变量和剂量限制,因此研发了第二代高选择性的小分子HIF-2α抑制剂belzutifan。
在本研究中,belzutifan未达到最大耐受剂量,RP2D剂量为“120 mg,每日1次”。最常见的不良事件是贫血,与TKI药物有一定的相似性。促红细胞生成素减少和缺氧是其独特的不良事件,可在临床药物选择时提供一定参考。
本研究同时验证了belzutifan的抗肿瘤活性,在平均随访27.7个月后,中位PFS为14.5个月,ORR为25%,对比目前已获批的后线治疗药物(TKI单药阿替尼:中位PFS为6.7个月,ORR为19%;TKI单药仑伐替尼:中位PFS为7.4个月,ORR为21%;IO单药纳武利尤单抗:中位PFS为4.6个月,ORR为25%),显示出可期的有效性和安全性。对于这些经过多线治疗的晚期转移性肾细胞癌患者,即便与双免联合、靶免联合或TKI联合哺乳动物雷帕霉素靶蛋白(mTOR)抑制剂等联合治疗方案二线12个月左右的中位PFS对比,HIF-2α抑制剂显示出的有效性证据也是不错的,未来扩大样本量、延长随访时间后的数据值得期待。
表1 ccRCC 队列中发生率≥20%的全因不良事件
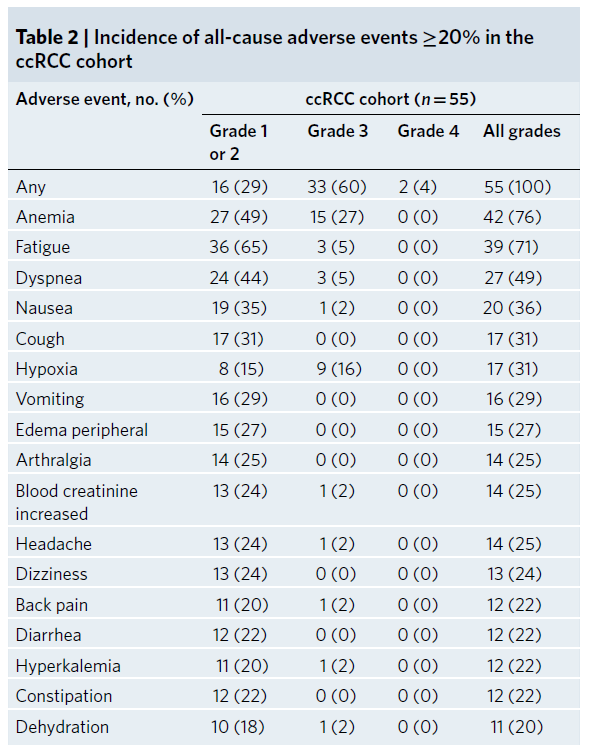
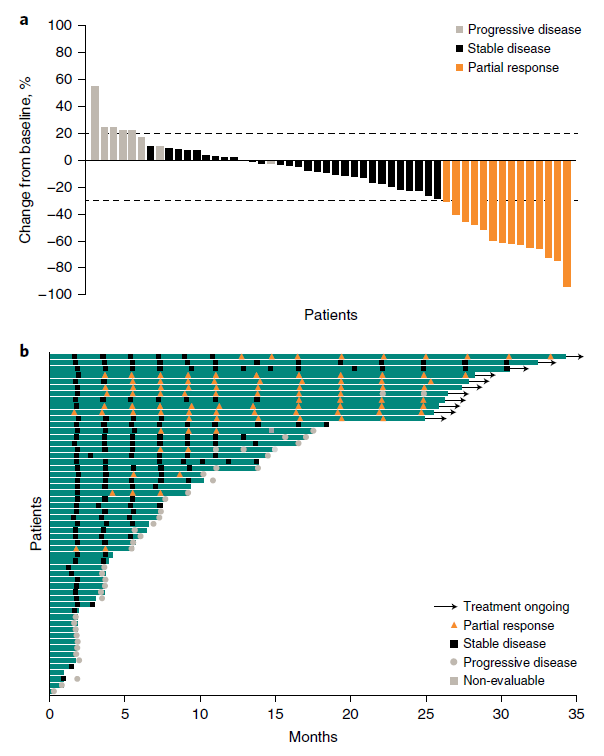
图3 ccRCC队列的疗效(a靶病灶较基线的最佳疗效变化;b治疗持续时间)
(3)SETD2对β-连环蛋白活性的多层次调节,抑制多囊性肾病向透明细胞肾细胞癌转变

摘要:多囊肾病(PKD)的患者发生肾细胞癌的风险很高。然而,在PKD到肾细胞癌的转变过程中,目前研究者们对相关基因或信号通路的变化知之甚少。SETD2是一种组蛋白甲基转移酶,可催化H3K36(H3K36me3)三甲基化,已被证实是ccRCC的肿瘤抑制因子,但其潜在机制仍有待进一步探索。在本项研究中,研究者在c-MYC诱导的小鼠PKD模型中敲除SETD2,促进了PKD向ccRCC的转变。通过竞争性结合β-catenin的靶基因启动子,SETD2可以在转录及转录后水平上抑制β-catenin的转录活性,同时SETD2还可以维持β-catenin破坏复合物的转录水平。因此,SETD2缺失可以导致Wnt/β-catenin信号通路高度活化,促进上皮-间质转化和肿瘤的形成。研究结果显示,在PKD向ccRCC转化过程中,由SETD2介导的竞争性DNA结合和H3K36me3修饰,可参与调控Wnt/β-catenin信号通路的活性,并在过程中发挥着重要的作用。另外,新建立的小鼠PKD和ccRCC模型将有助于开展后续疾病进展相关的临床研究。
崔心刚 教授
海军军医大学第三附属医院
【专家简评】
PKD是常见的遗传性肾脏疾病,也是导致终末期肾病的主要原因之一,而肾细胞癌是泌尿系统常见的恶性肿瘤。临床统计发现,PKD患者常伴发肾细胞癌,约有20%的患者表现为双侧肾脏或多病灶患病。但PKD转变为肾细胞癌的具体分子机制尚未明晰。本项研究利用基因工程工具,建立了c-MYC诱导的小鼠PKD模型,并且定向敲除了SETD2基因,通过体内和体外多项实验,揭示了SETD2在PKD向ccRCC转化过程中的作用机制。基于本文的结论,SETD2可能是PKD患者预防肿瘤发生和ccRCC治疗的一个潜在靶点。另外,SETD2在原发性ccRCC中是否发挥着同样的作用仍需要进一步研究,未来数据值得期待。
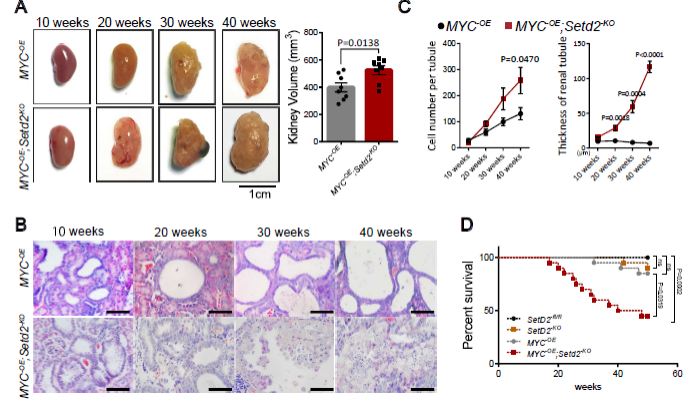
图4 SETD2 缺失加速了c-MYC转基因PKD小鼠向ccRCC转化。
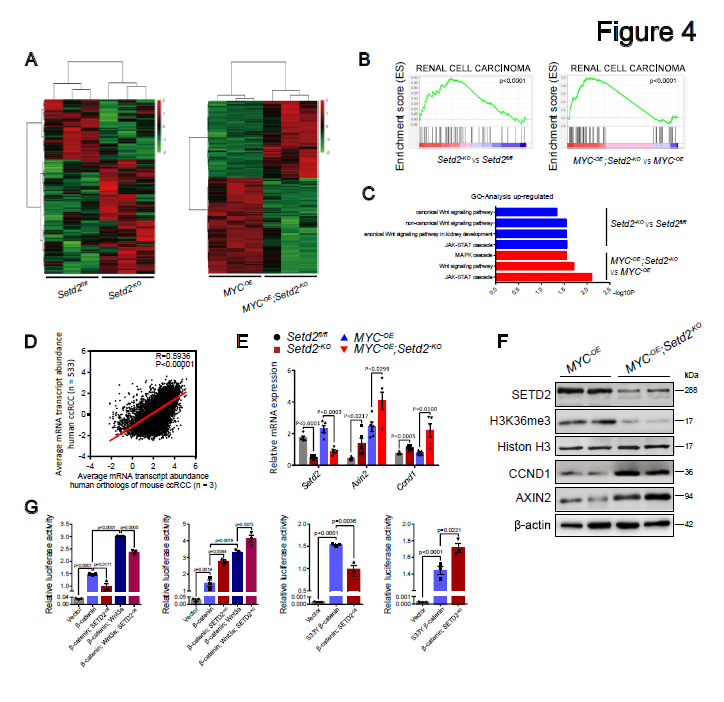
图5 SETD2缺陷的肾小管上皮细胞显示出过度活跃的Wnt/β-连环蛋白信号
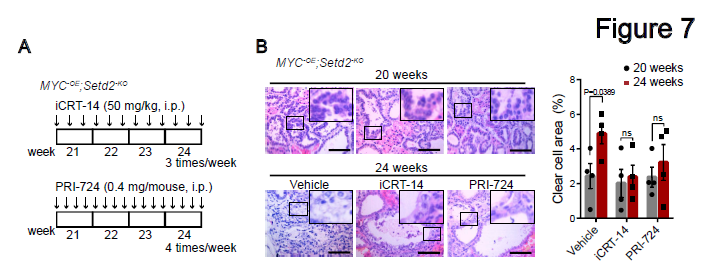
图6 抑制β-连环蛋白信号可缓解小鼠SETD2缺失引起的症状
点评专家介绍
(按姓名首字母排序)
崔心刚 教授
海军军医大学第三附属医院(东方肝胆外科医院)
泌尿外科主任,主任医师,教授,博士生导师
中华医学会泌尿外科分会青委会副主委
中华医学会泌尿外科分会微创学组及机器人学组委员
中国医师协会内镜医师分会委员会副总干事长
中国医师协会内镜医师分会泌尿腔镜专业委员会副秘书长
《中华泌尿外科杂志》常务编委
董文 教授
中山大学孙逸仙纪念医院
副主任医师,医学博士,硕士研究生导师
泌尿外科肿瘤亚专科副主任
深汕中心医院泌尿外科副主任
中华医学会泌尿外科学分会青年学组委员
广东省医学会泌尿外科学分会青年委员会委员
中国自动化学会医学机器人专业委员会委员
广东省医学会男科学分会前列腺学组成员
美国泌尿外科学会国际委员
张树栋 教授
北京大学第三医院
泌尿外科副主任,主任医师,研究生导师
维也纳医科大学博士后
中华医学会泌尿外科分会微创学组委员
中华泌尿外科杂志编委
中华医学会泌尿外科分会青委会肿瘤学组副组长
中国抗癌协会泌尿男生殖系肿瘤专业委员会委员兼肾癌学组委员
香港大学玛丽医院Clinical Fellow Mayo、Cleveland、John Hopkins、MD 安德森癌症中心等多家医院访问学者
参考文献:
1. Motzer R, Alekseev B, Rha SY, et al. Lenvatinib plus Pembrolizumab or Everolimus for Advanced Renal Cell Carcinoma. N Engl J Med. 2021 Apr 8; 384(14):1289-1300.
2. Choueiri TK, Bauer TM, Papadopoulos KP, et al. Inhibition of hypoxia-inducible factor-2α in renal cell carcinoma with belzutifan: a phase 1 trial and biomarker analysis. Nat Med. 2021 May; 27(5): 802-805.
3. Rao H, Li X, Liu M, et al. Multi-level regulation of β-catenin activity by SETD2 suppresses the transition from polycystic kidney disease to clear cell renal cell carcinoma. Cancer Res. 2021 Apr 28: canres. 3960. 2020.

MCC号VOR21062780有效期2022-06-28,资料过期,视同作废。
本文旨在传递医学前沿信息和研究进展,文中所涉及的部分药物尚未在中国获批适应症,相关数据仅供临床医生参考,非商业用途,请自觉保护作品著作权;本资料中引用的公开发表文献仅代表作者的个人观点。



 个人中心
个人中心
 我是园区
我是园区










