
4 月 11 日,CDE 官网显示,武田/大冢的第三代 BCR-ABL 抑制剂「泊那替尼」在国内申报上市,拟纳入优先审评。这是继亚盛/信达的奥雷巴替尼之后,国内第 2 款申报的三代 BCR-ABL 抑制剂。
该药用于既往耐药或不耐受的慢性髓性白血病(CML)、复发或难治性费城染色体阳性急性淋巴细胞白血病(ALL)、T315I 阳性 CML 或 T315I 阳性费城染色体阳性 ALL。

截图来自:CDE 官网
泊那替尼最早由 ARIAD Pharmaceuticals 研发,2014 年 12 月授权大冢制药在日本及其他 9 个包括中国在内的亚洲地区共同开发和商业化;2016 年分别将欧洲权益授权给 Incyte 公司,将阿根廷、巴西、智利、哥伦比亚、墨西哥和其他拉丁美洲国家权益授权给 Pint Pharma。2017 年 1 月,武田以 52 亿美元收购了 ARIAD 公司。
泊那替尼项目全球权益流转图

截图来自:Insight 数据库网页版(http://db.dxy.cn/v5/home/)
早在 2012 年末,该药就在美国获批上市,2013 年度和 2016 年度又分别在欧洲和日本获批。在中国,其首项临床申请在 2017 年递交,于 2018 年 7 月首次公示临床。此前由于国内三代 BCR-ABL 抑制剂的空白,该药曾被纳入第一批临床急需境外新药名单,今日终于申报上市。
泊那替尼项目关键节点

截图来自:Insight 数据库网页版
目前,泊那替尼已经在全球广泛获批用于不同分期的 CML 患者和 Ph+ALL 患者。作为一款 BCR-ABL 激酶抑制剂,泊那替尼能够靶向 BCR-ABL 原型,以及所有已知的单一、治疗耐药性突变,包含最常见的 T315I 突变型。
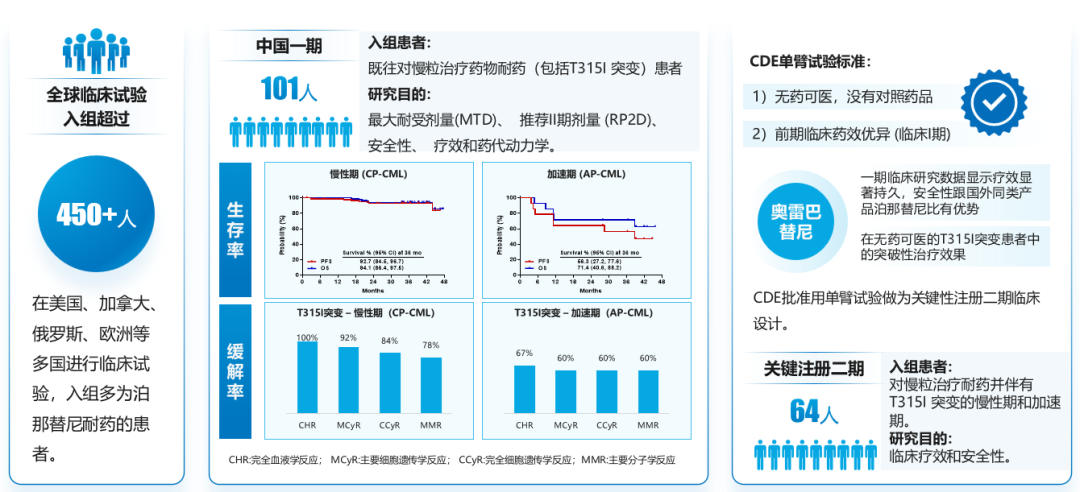
同类药品中,亚盛医药已经凭借自研三代 BCR-ABL 抑制剂奥雷巴替尼在 2021 年 11 月获批上市,并在 2022 年通过谈判进入医保目录。官方资料显示,其全球临床入组患者多为泊那替尼耐药的患者。







 个人中心
个人中心
 我是园区
我是园区




