▎药明康德内容团队报道
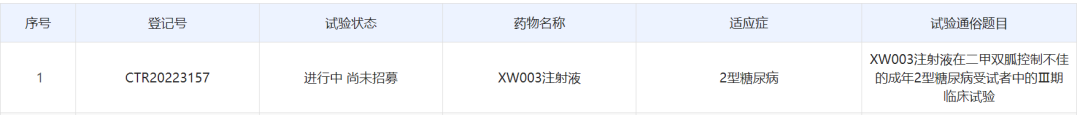
根据中国药物临床试验登记与信息公示平台,先为达生物本次启动的是一项多中心、随机、开放、度拉糖肽阳性对照3临床试验(EECOH-2),受试者为二甲双胍治疗后血糖控制不佳的成年2型糖尿病患者。该试验主要终点指标为给药32周后糖化血红蛋白(HbA1c)相对基线的改变,次要终点指标有:HbA1c相对基线的改变、HbA1c < 7%和HbA1c ≤ 6.5%的受试者比例、 体重相对基线的改变、不良事件(AE)、药代动力学及免疫原性等。试验主要研究者为复旦大学附属中山医院李小英教授,目标入组人数为600人。

值得一提的是,先为达生物于今年8月宣布,XW003已在针对中国成年2型糖尿病患者的2期临床试验中达到试验终点。数据显示,20周治疗期结束时,XW003 1.2 mg队列中88%的受试者HbA1c≤7.0%(vs 安慰剂组21%),72%的受试者达到了HbA1c≤6.5%(vs 9%)。该结果表明,每周皮下注射XW003表现出良好的安全性和耐受性,可明显降低主要疗效终点HbA1c。
2型糖尿病是全球常见的慢性代谢性疾病。患者的主要表现为胰岛素抵抗,导致胰岛素的功能不能得到充分发挥。对于这些患者来说,单纯使用胰岛素不能很好地改善患者病情,因此他们需要其它类型的降糖药物来控制血糖水平。
希望先为达生物XW003在临床研究中进展顺利,早日为更多患者带来新的治疗选择。
[2]先为达XW003 (Ecnoglutide )肥胖症2b 期临床试验获得积极中期分析结果. Retrieved Oct 28 , 2022. From https://www.prnasia.com/story/380866-1.shtml

本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。




 个人中心
个人中心
 我是园区
我是园区




