
扫描图中二维码,进入研发客年会报名通道
撰文|梁贵柏
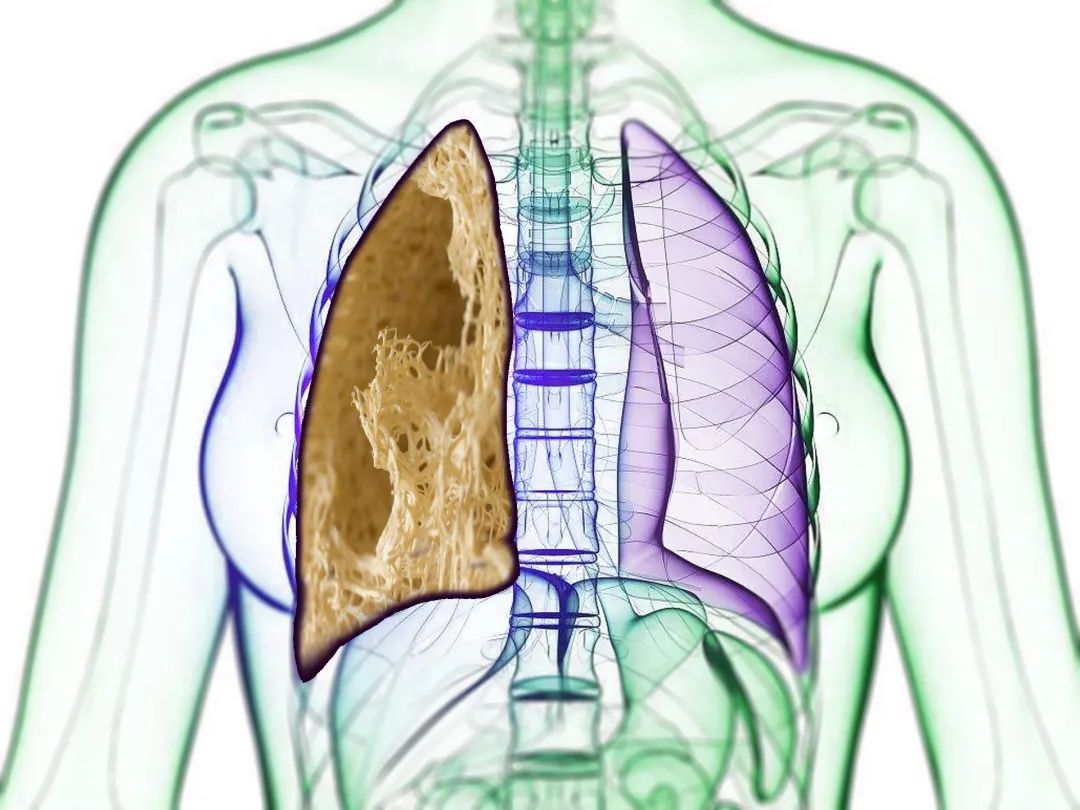
一张触目惊心的肺部CT片呈现在医生的面前:患者的肺部组织呈蜂巢状,看起来就像是一个“网状肺”或“丝瓜筋肺”。
2010年底,年过7旬的郑老伯在例行体检时被确诊为特发性肺纤维化患者。医生告诉郑老伯及家人,这种病无药可治,只能自行在家休养。因为发现得早,当时郑老伯的生活质量暂时还没有受到多大的影响。但是几年后,郑老伯的病情加重了,活动能力严重丧失,几乎不能出门,只能躺在病榻上,整夜不停地咳嗽,度日如年。
在没有特效药的时代,特发性肺纤维化患者被确诊之后的中位生存期仅2~3 年,5年生存率低于30% ,被称为“不是癌症的癌症”。
转机发生在2019年。在医生的推荐下,郑老伯开始服用一款刚刚在中国大陆上市不久的创新药物。这让郑老伯重燃希望,积极与医生配合,坚持按时用药,症状得到很大改善。如今他不但能自己上下楼,还坚持每天出门散步、锻炼,笑容在郑老伯脸上得以重新绽放。
这款新药就是我们这个故事的主角——勃林格殷格翰公司研发的治疗特发性肺纤维化的创新药尼达尼布(nintedanib)。
不是癌症的癌症
但是,如果肺部的损伤-炎症-修复的循环持续不断地发生,有可能会导致不可逆的肺泡壁重塑(remodeling),也就是肺组织的永久性结构变化,肺纤维化疾病开始了。
值得尝试的新适应症

初见成效的模型研究
谨慎乐观的临床试验

令人瞩目的创新药物
值得期待的健康生活
作者简介
贵柏曾在默沙东新药研究院工作多年,潜心钻研药物化学,颇有建树。几年前回国加入药明康德,从事业务开发、项目管理和驻美运营。梁博士是《新药的故事》一书的作者。他以长期的积累、独特的视角和生动的文字,通过《老梁说药》栏目讲述新药研发“背后的故事”,令人耳目一新,脑洞大开。梁贵柏博士目前是偕怡制药联合创始人兼首席科学家,欢迎读者通过邮箱gbliang55@hotmail.com与梁博士联系。




 个人中心
个人中心
 我是园区
我是园区




