▎药明康德内容团队编辑
今日,赛诺菲(Sanofi)公司宣布,美国FDA授予该公司与Sobi合作开发的efanesoctocog alfa(BIVV001)突破性疗法认定,用于治疗血友病A患者。新闻稿指出,这是首个获得突破性疗法认定的凝血因子VIII(FVIII)疗法。Efanesoctocog alfa是一款长效血友病A疗法,目标是通过每周一次预防性治疗,在一周的大部分时间中维持接近正常的FVIII活性。
血友病A是由于编码FVIII的基因出现突变,导致FVIII缺失的遗传性疾病。目前常见的血友病A治疗方法是定期输注FVIII,然而通常患者需要每周接受3-4次FVIII输注,为他们的生活带来极大的不便。
天然FVIII在血液中的半衰期只有12个小时左右,因为在血液中,它与血管性血友病因子(von Willebrand factor ,VWF)结合形成复合体。VWF与FVIII的结合虽然提高了FVIII在血液中的稳定性,但是VWF本身被降解的速度也为FVIII在血液中的滞留时间设置了一个上限,因为当VWF被降解时,与它结合的FVIII也同时被降解。
BIVV001的设计将FVIII与一个VWF片段连接起来,形成的复合体不会与血液中的天然VWF相结合,从而突破VWF设定的半衰期上限。
它旨在让血友病A患者在接受一次注射之后,能够在一周的大部分时间里获得接近正常的FVIII因子活性水平。
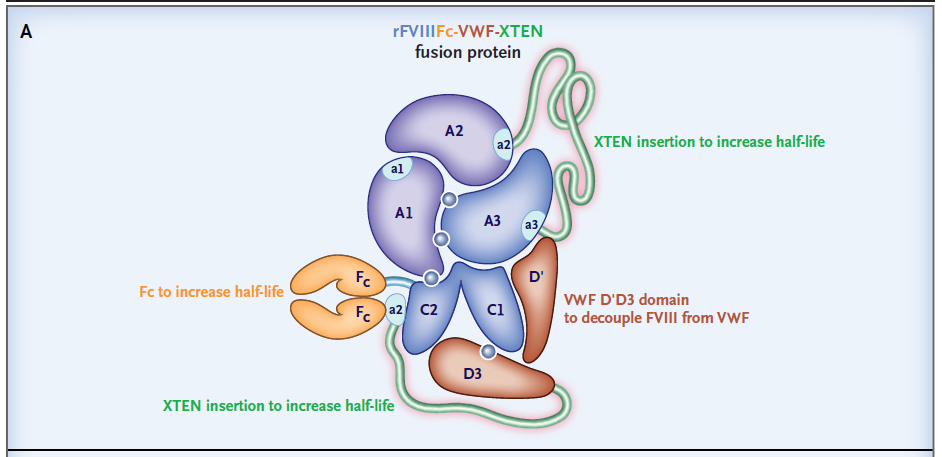
▲BIVV001结构示意图(图片来源:参考资料[2])
这一突破性疗法认定的授予是基于
关键性3期临床试验
XTEND-1的积极结果。试验结果显示,每周一次efanesoctocog alfa预防性治疗,显著降低严重血友病A患者中的年出血率。同时,与此前接受的FVIII预防性治疗相比,efanesoctocog alfa在预防出血方面表现出优效性。
赛诺菲研发全球负责人John Reed博士表示:“突破性疗法认定凸显了efanesoctocog alfa变革血友病A治疗的潜力,它能够在更长时间里提供更高的保护。我们期待与监管机构在申请递交和审评这一创新疗法的过程中继续合作。”
参考资料:
[1] Press Release: FDA grants efanesoctocog alfa Breakthrough Therapy designation for hemophilia A. Retrieved June 1, 2022, from https://www.globenewswire.com/news-release/2022/06/01/2453803/0/en/Press-Release-FDA-grants-efanesoctocog-alfa-Breakthrough-Therapy-designation-for-hemophilia-A.html
[2] Konkle et al., (2020). BIVV001 Fusion Protein as Factor VIII Replacement Therapy for Hemophilia A. NEJM, DOI: 10.1056/NEJMoa2002699
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。








 个人中心
个人中心
 我是园区
我是园区




