
前文回顾: 首款靶向CD19的ADC新药Zynlonta获批!助力大B细胞淋巴瘤治疗
首款靶向CD19的ADC新药Zynlonta获批!助力大B细胞淋巴瘤治疗
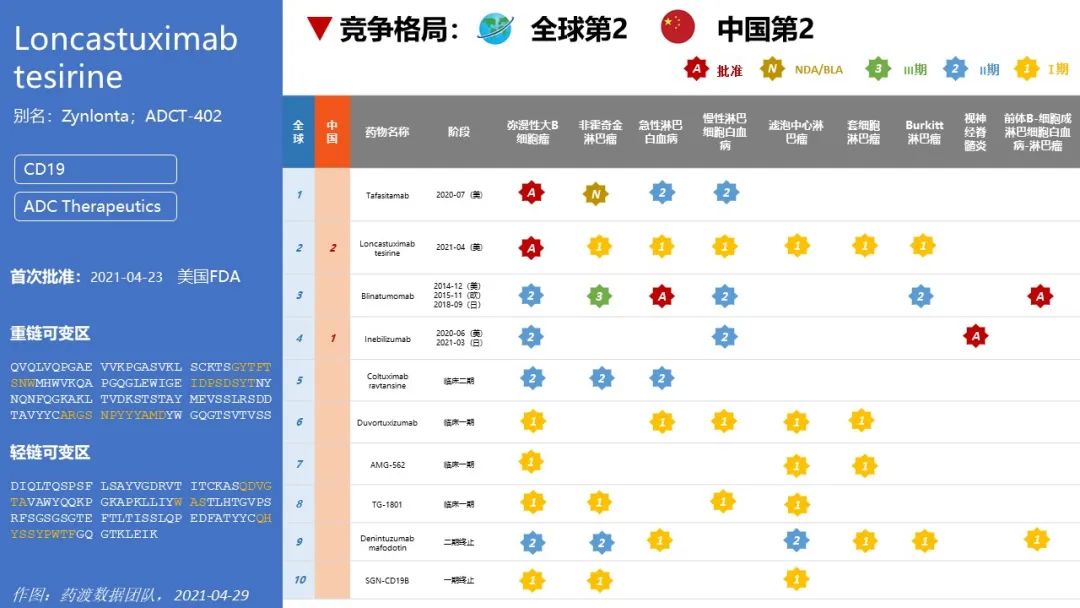
ADC Therapeutics公司研发的Loncastuximab tesirine,已经于2021年4月23日获得FDA批准,用于治疗弥漫性大B细胞淋巴瘤。该药还处于治疗非霍奇金淋巴瘤、套细胞淋巴瘤和滤泡性淋巴瘤的临床一期试验阶段。
Loncastuximab tesirine是一种抗体偶联药物,由3部分组成:1)靶向CD19的嵌合型IgG1kappa单抗loncastuximab;2)有效载荷分子为吡咯开苯并吖庚三烯(PBD)二聚体毒素SCX;3)含有8个PEG分子作为隔离区的可裂解型马来酰亚胺Linker,以缬氨酸-丙氨酸二肽作为组织蛋白酶B的裂解位点。SCX通过Linker偶联到抗体的半胱氨酰,药物抗体比率ADR平均为2.3 [1] 。
也可点击下方链接获取相应PDF高清版:
https://data.pharmacodia.com/v3/insight/#/ListPdf?tag=2
参考资料
1.药渡数据:https://data.pharmacodia.com
2.ADCTherapeutics官网:
https://ir.adctherapeutics.com/overview/default.aspx
3.NCI官网:https://seer.cancer.gov/statfacts/html/dlbcl.html
4.FDA官网:
https://www.accessdata.fda.gov/drugsatfda_docs/label/2021/761196s000lbl.pdf


点击"阅读原文",随时掌握行业动态



 个人中心
个人中心
 我是园区
我是园区







