您还不是认证园区!
赶快前去认证园区吧!
美国 FDA 于 7 月 27 日在《联邦公报》上分别公布了仿制药使用者付费项目(GDUFA)和生物类似药使用者付费项目(BsUFA) 2022 财年(2021 年 10 月 1 日至 2022 年 9 月 30 日)的费率。下面我们分别来看看。
GDUFA
GDUFA 的费率整体有所上涨,但幅度不大。最大的增长出现在新 ANDA 的申请费中,这是可以预料的,因为通货膨胀以及 2022 财年预计需要缴费的 ANDA 数量从 872(867)件减少至 789(788)件,从而导致了申请费的增加(上面括号内为预计原始提交的实际付费申请数量)。这些数据考虑到 FDA 预计一些 ANDA 将在同一财年被拒绝立卷并重新提交的情况。
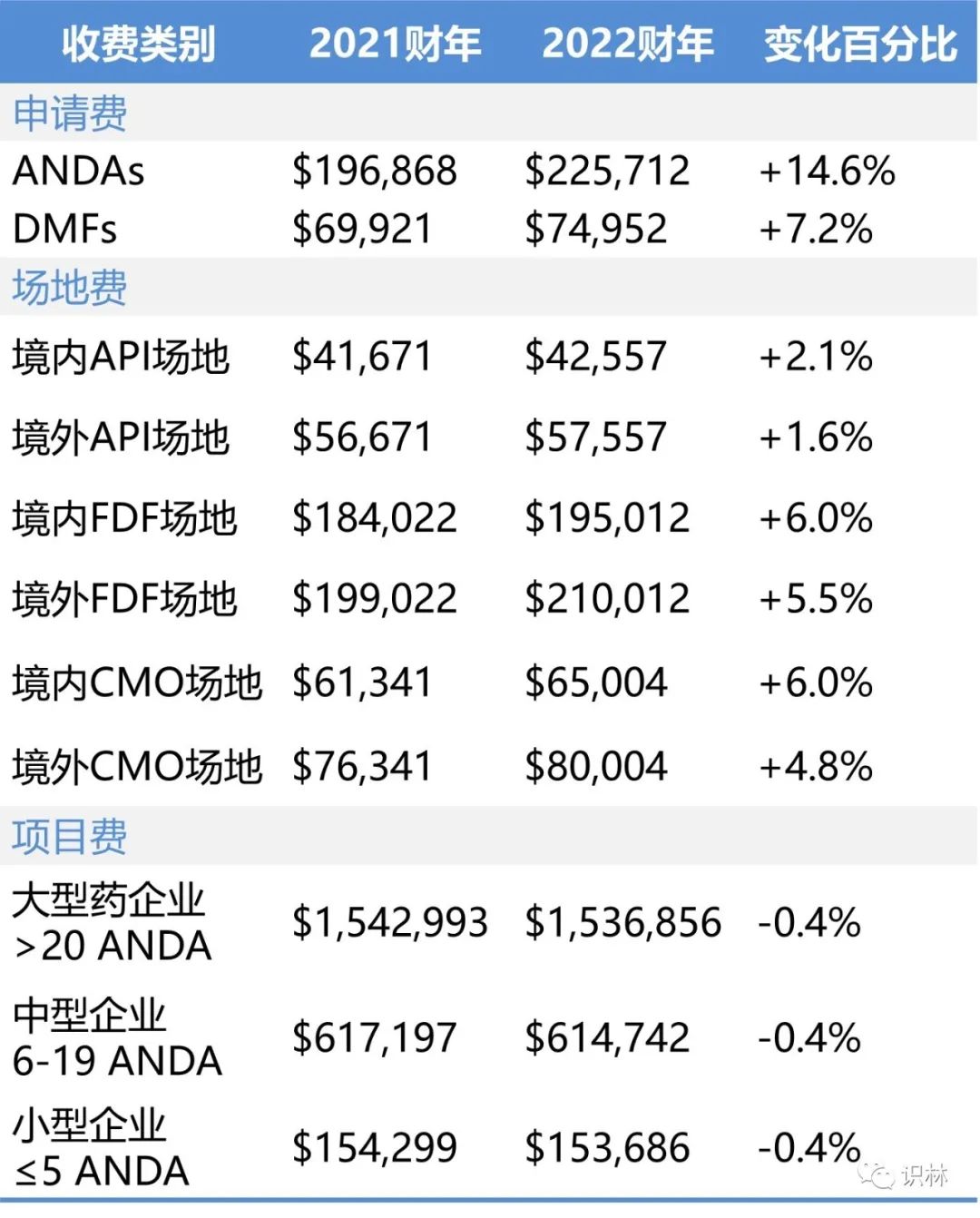
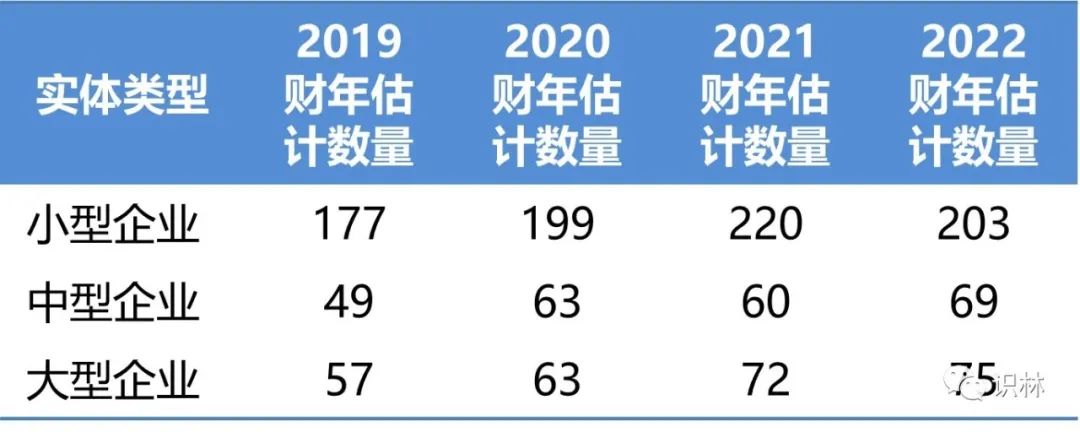
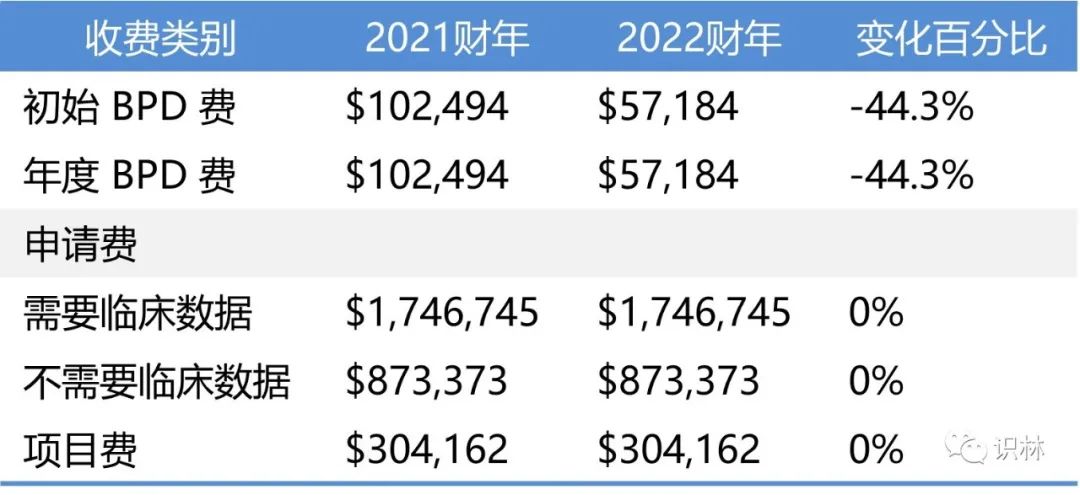
BsUFA 费率在 2022 财年已经是连续第二年有所下降。生物类似药领域看起来似乎不错,在去年生物类似药产品开发(BPD)费和重新激活费用下降 13.1% 之后,今年的预计提交数量继续猛增,今年的这些费用又下降了 44.3%。


长按下方二维码下载识林®App

识林®版权所有,未经许可不得转载。



 个人中心
个人中心
 我是园区
我是园区




