众所周知,基因改变与癌症的发生息息相关,不过近年来,人们意识到另一种重要因素也是促进癌症的罪魁祸首,那就是翻译后修饰。精氨酸甲基化是一种重要的翻译后修饰类型,它影响多种细胞过程,包括基因表达、蛋白质修饰、信号转导和细胞周期进展。蛋白质精氨酸甲酯转移酶(PRMT)是精氨酸甲基化的催化酶,S-腺苷甲硫氨酸(AdoMet/SAM)作为甲基供体,经催化后甲基转移到蛋白的精氨酸残基(图1)。目前,人们已经确定了9种PRMT,分为I、II、III型三种类型,今天我们要介绍的PRMT5属于II型,可催化对称二甲基化(SDMA)和单甲基化(MMA)。
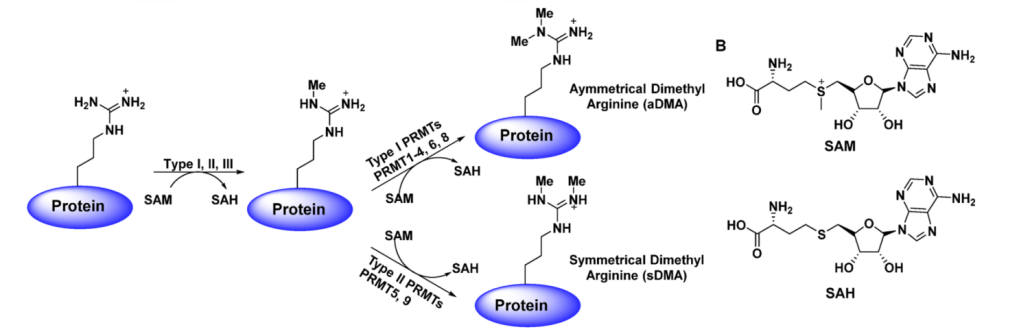
图1 PRMT催化精氨酸甲基化的机理(来源:J Med Chem. 2018 Nov 8;61(21):9429-9441.)
研究表明,PRMT5通过p53和NF-κB等关键转录因子(TF)的甲基化来调节基因表达,从而影响癌症进展中的许多重要细胞过程(图2)。近年来,PRMT5作为抗癌靶点受到了越来越多的关注。PRMT5在各种癌症中过度表达,包括胶质母细胞瘤、黑色素瘤、白血病/淋巴瘤、多发性骨髓瘤、前列腺癌、膀胱尿路上皮癌、卵巢癌、肺癌、胃癌、结直肠癌等,并与不良预后相关。体内外研究发现,抑制或敲除PRMT5会显著降低细胞增殖、迁移和集落形成的能力,但会促进细胞凋亡和细胞周期的停滞。此外,口服PRMT5抑制剂在肺肿瘤异种移植模型中表现出显著的抗肿瘤活性。
图2 PRMT5通过催化甲基化影响癌症进展(来源:J Immunother Precis Oncol. 2022 Jun22;5(3):58-67.)
PRMT5抑制剂的研究进展
鉴于PRMT5在癌症治疗领域表现出巨大的潜力,越来越多的药企和科研机构开始致力于PRMT5抑制剂的研究。目前已有三十多个PRMT5抑制剂在研,其中进入临床阶段的不到一半(图3左),值得注意的是,有三分之一来自国内外科研机构,具有较大的占比(图3右),并且都处于临床前阶段,说明该靶点还处于探索阶段,具有一定的不确定性,但另一方面,也体现出该赛道的竞争相对较小。
进展最快的是Epizyme和GSK联合开发的GSK3326595,已经进入II期临床,也是唯一一个进入II期临床的PRMT5抑制剂,用于治疗乳腺癌、骨髓增生异常综合征、急性髓系白血病和非霍奇金淋巴瘤,其中前三个适应症均已完成I期临床,并表现出积极的疗效,这大大增加了人们对PRMT5抑制剂的信心。
目前进入I期临床的有11个,其中有4个已经完成了I期临床试验,分别是来自Amgen的AMG 193、来自MiratiTherapeutics的MRTX1719、来自SK Life Science的SKL27969、来自TangoTherapeutics的TNG908。国内也有数家企业对PRMT5抑制剂开展了研究,包括先声、圣和、石药,分别开发了SCR-6920、SCR-6920和SYHX2001,并且适应症布局了实体瘤领域,可以说是寄予了厚望。
表1 PRMT5抑制剂研究进展
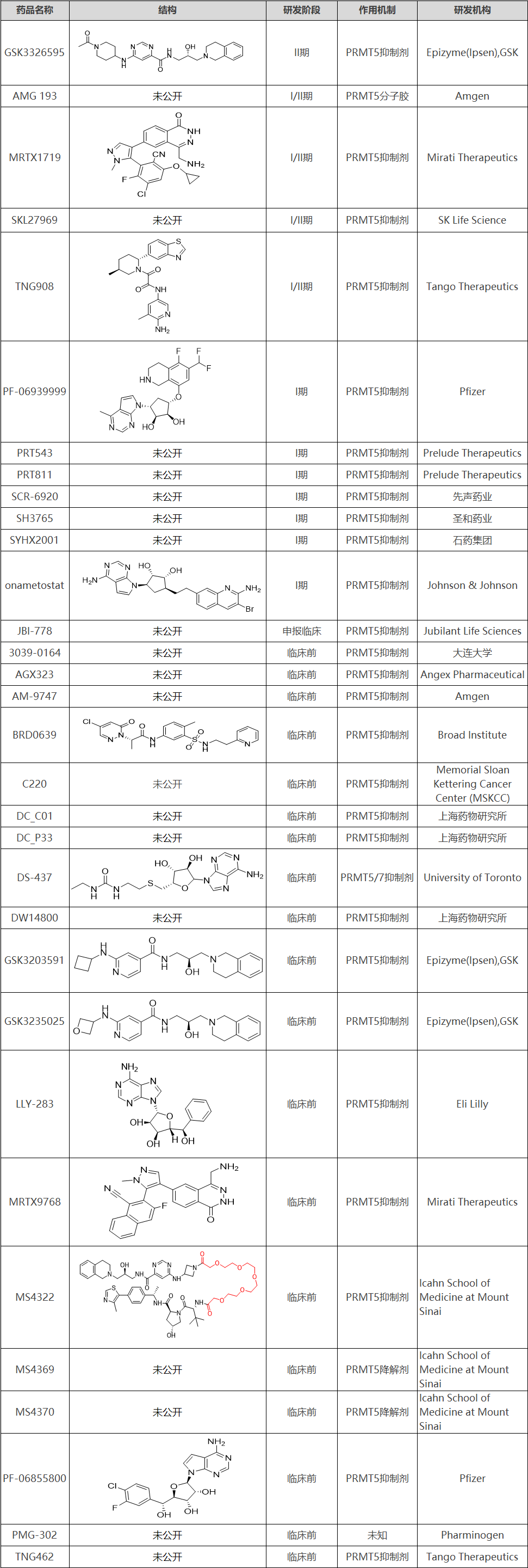
图3 PRMT5抑制剂的研发阶段占比(左)和研发机构类型占比(右)
在现有的PRMT5抑制剂中,已有一半公开了其结构信息,下面我们来介绍一下其化合物专利的布局情况。
目前进展最快的是GSK3326595,Epizyme公司最早在2013年12月20日向全球多个国家或地区申请了化合物专利,其中,CN’226B的权利要求113保护了GSK3326595的具体结构,其同族US’555B2的权利要求1保护了GSK3326595的具体结构。
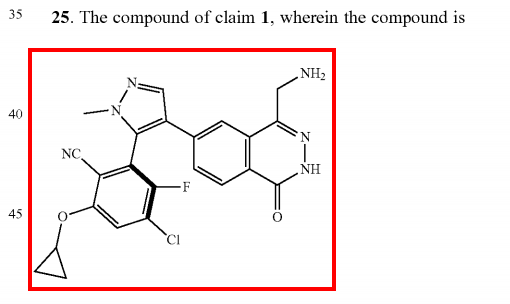
MRTX1719已顺利完成I期临床试验。CN’28912A的权利要求89要求保护MRTX1719的具体结构,US’351B2的权利要求25保护了MRTX1719的具体结构。
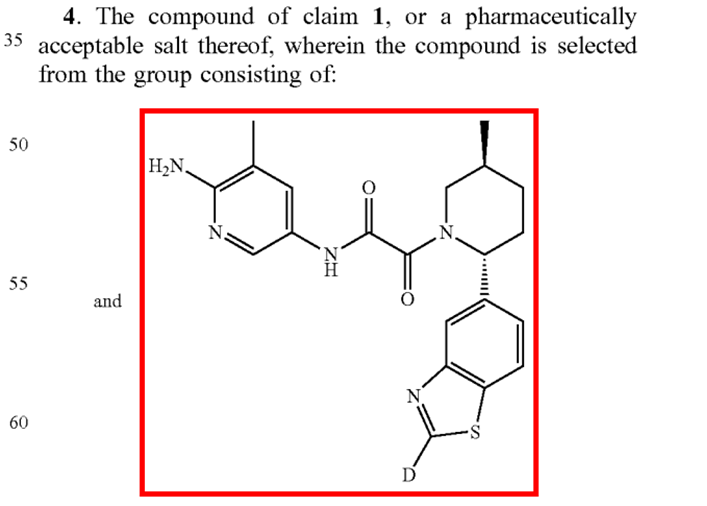
TNG908也顺利完成了I期临床试验,US’350B2的权利要求4保护了TNG908的具体结构,还没有在中国申请其化合物专利。
PF-06939999进展到I期临床就终止了研究,CN’797A的权利要求10要求保护PF-06939999的具体结构,US’037B2的权利要求13保护了PF-06939999的具体结构。
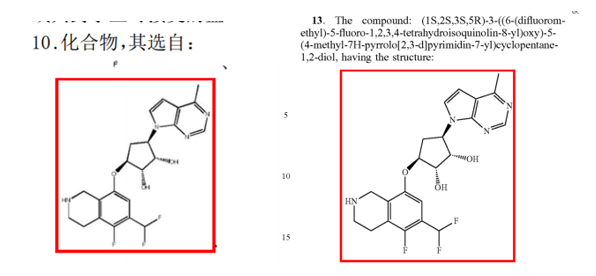
onametostat也处于I期临床阶段,CN’413B的权利要求17保护了onametostat的具体结构,其同族US’711B2的权利要求17保护了onametostat的具体结构。
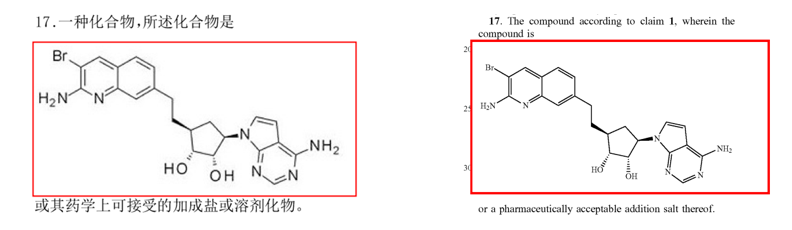
处于临床前研究阶段的PRMT5抑制剂结构公开了8个。BRD0639,WO’144A1的权利要求113要求保护BRD0639的具体结构,目前还没有在中美布局其化合物专利。
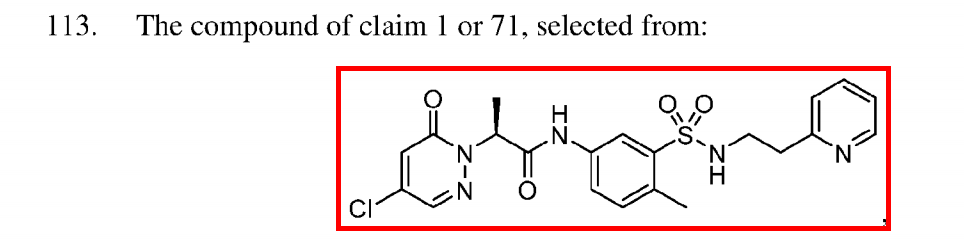
GSK3203591和GSK3235025,与上述的GSK3326595为同系列化合物,CN’226B的权利要求110保护了GSK3235025和GSK3203591的具体结构,同族US’519B2的权利要求35保护了GSK3235025和GSK3203591的具体结构。
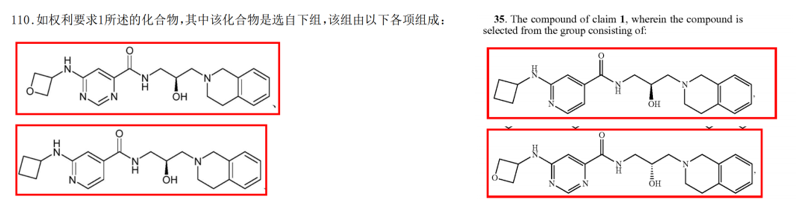
LLY-283,CN’602A的权利要求6要求保护LLY-283的具体结构,US’208A1的权利要求6要求保护LLY-283的具体结构。
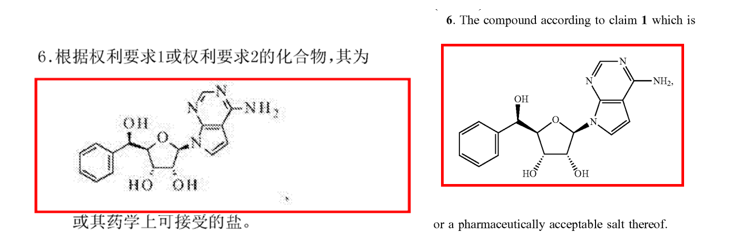
MRTX9768与上述的MRTX1719为同系列化合物,CN’912A的权利要求89要求保护MRTX9768的具体结构,US’351B2的权利要求22保护了MRTX9768的具体结构。
MS4322,US’538A1的权利要求75、77、81要求保护的马库什结构包含MS4322,目前还没有在中国申请化合物专利。
PF-06855800,CN’205A的权利要求17要求保护PF-06855800和C220的具体结构,同族US’475A1的权利要求3保护了PF-06855800的具体结构。
结语
近年来,人们逐渐认识到翻译后修饰与癌症的密切关系,这为抗癌研究增添了新方向,PRMT5作为一种翻译后修饰酶,已经被证实与多种癌症相关,是一个充满前景的癌症治疗靶点,它的追随者不乏一些全球顶尖的制药企业,其适应症直接深入到实体瘤领域,寄托了人们美好的愿望。但同时,它又是充满风险与未知的靶点,进展最快的药物也才进入II期临床,未来PRMT5能否斩获癌症治疗的一片市场,还需要时间来公布答案。
[1] Sapir T, Shifteh D,Pahmer M, Goel S, Maitra R. Protein Arginine Methyltransferase 5 (PRMT5) andthe ERK1/2 & PI3K Pathways: A Case for PRMT5 Inhibition and CombinationTherapies in Cancer. Mol Cancer Res. 2021 Mar;19(3):388-394. doi:10.1158/1541-7786.
[2] Wang Y, Hu W, YuanY. Protein Arginine Methyltransferase 5 (PRMT5) as an Anticancer Target and ItsInhibitor Discovery. J Med Chem. 2018 Nov 8;61(21):9429-9441. doi:10.1021/acs.jmedchem.8b00598.
[3] Feustel K, FalchookGS. Protein Arginine Methyltransferase 5 (PRMT5) Inhibitors in OncologyClinical Trials: A review. J Immunother Precis Oncol. 2022 Jun 22;5(3):58-67.doi: 10.36401/JIPO-22-1.
Copyright © 2023 PHARMCUBE. All Rights Reserved.
欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;如需转载,请给微信公众号后台留言或发送消息,并注明公众号名称及ID。
免责申明:本微信文章中的信息仅供一般参考之用,不可直接作为决策内容,医药魔方不对任何主体因使用本文内容而导致的任何损失承担责任。

























 个人中心
个人中心
 我是园区
我是园区




