▎药明康德内容团队报道
中国国家药品监督管理局药品审评中心(CDE)网站最新公示,恒瑞医药提交了一项PARP抑制剂氟唑帕利胶囊的新适应症上市申请,并于12月24日获得受理。值得一提的是,一周前氟唑帕利刚在中国
,该药不仅是首个获批的由中国企业自主开发的PARP抑制剂,也是恒瑞医药第七款在中国获批上市的1类新药。根据公开资料,氟唑帕利本次申请的适应症可能为复发性卵巢癌维持治疗。
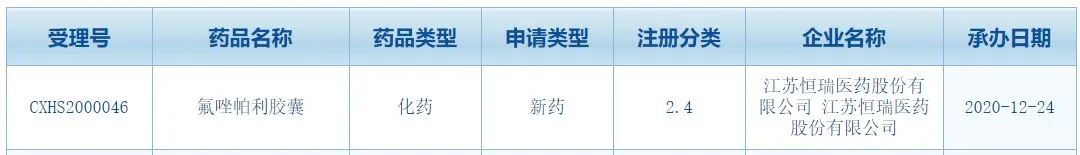
截图来源:CDE官网
PARP(Poly[ADP-ribose] polymerase)是细胞中一种重要的DNA修复蛋白,主要修复DNA双链损伤。PARP抑制剂是首类利用“合成致死”概念在临床上取得成功的药物。“合成致死”是指两个非致死基因同时被抑制,导致细胞死亡的现象。利用这一机制找到肿瘤中的特异突变,再找到它的“合成致死搭档”,进而特异性杀死癌细胞。
氟唑帕利是恒瑞医药自主研发的一种PARP抑制剂,可特异性杀伤BRCA突变的肿瘤细胞。12月14日,氟唑帕利通过优先审评程序获得中国国家药品监督管理局(NMPA)批准上市,用于既往经过二线及以上化疗的伴有胚系BRCA突变(gBRCAm)的铂敏感复发性卵巢癌、输卵管癌或原发性腹膜癌患者的治疗。
目前,恒瑞医药正在探索氟唑帕利针对其它适应症的效果。中国药物临床试验登记与信息公示平台显示,恒瑞医药已登记30多项关于氟唑帕利的临床研究,涉及的适应症包括卵巢癌、小细胞肺癌、胰腺癌、乳腺癌、前列腺癌、胃癌等癌种。其中,氟唑帕利单药或联合阿帕替尼治疗晚期卵巢癌、伴有BRCA1/2突变的乳腺癌、胰腺癌的研究已处于3期临床阶段。
2020年9月,恒瑞医药宣布氟唑帕利在一项用于复发性卵巢癌维持治疗的3期临床研究(FZPL-III-301-OC)中达到主要研究终点。这是一项评估氟唑帕利胶囊对比安慰剂用于复发性卵巢癌(包括输卵管癌、原发性腹膜癌)含铂治疗后维持治疗的随机、双盲、安慰剂对照、多中心3期临床研究,由全国35家中心共同参与。研究的主要终点为由盲态独立评审委员会(BIRC)根据RECIST v1.1标准评估的无进展生存(PFS),次要研究终点包括研究者评估的PFS、无化疗间期(CFI)、总生存期(OS)和安全性等。
根据新闻稿,由独立数据监察委员会(IDMC)判定主要研究终点的期中分析结果达到方案预设的优效标准。研究结果表明,氟唑帕利单药用于铂敏感的复发性卵巢癌、输卵管癌或原发性腹膜癌含铂治疗达到完全缓解或部分缓解后的维持治疗,可显著延长患者的无进展生存期。
恒瑞医药曾在当时的新闻稿中表示,会在近期向CDE递交上市前的沟通交流申请。由此推测,本次氟唑帕利递交的上市申请适应症可能为用于复发性卵巢癌维持治疗。
祝贺恒瑞医药氟唑帕利胶囊的新适应症上市申请获得受理,希望该申请早日获批,惠及更多患者。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。
欢迎扫码关注“
医药观澜
”微信公众号,了解更多中国医药创新动态。

注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
[1]中国国家药监局药品审评中心. Retrieved Dec 24,2020, from http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=3
[2] 我国首个原研PARP抑制剂氟唑帕利获批上市. Retrieved Dec 17, 2020, from http://www.hrs.com.cn/main_newshow/show-6637.html
[3]恒瑞医药1类新药氟唑帕利用于复发性卵巢癌维持治疗的随机、对照III期临床研究达到主要研究终点. Retrieved Sep 28, 2020, from http://www.hrs.com.cn/main_newshow/show-6525.html








 个人中心
个人中心
 我是园区
我是园区




