您还不是认证园区!
赶快前去认证园区吧!

01


02


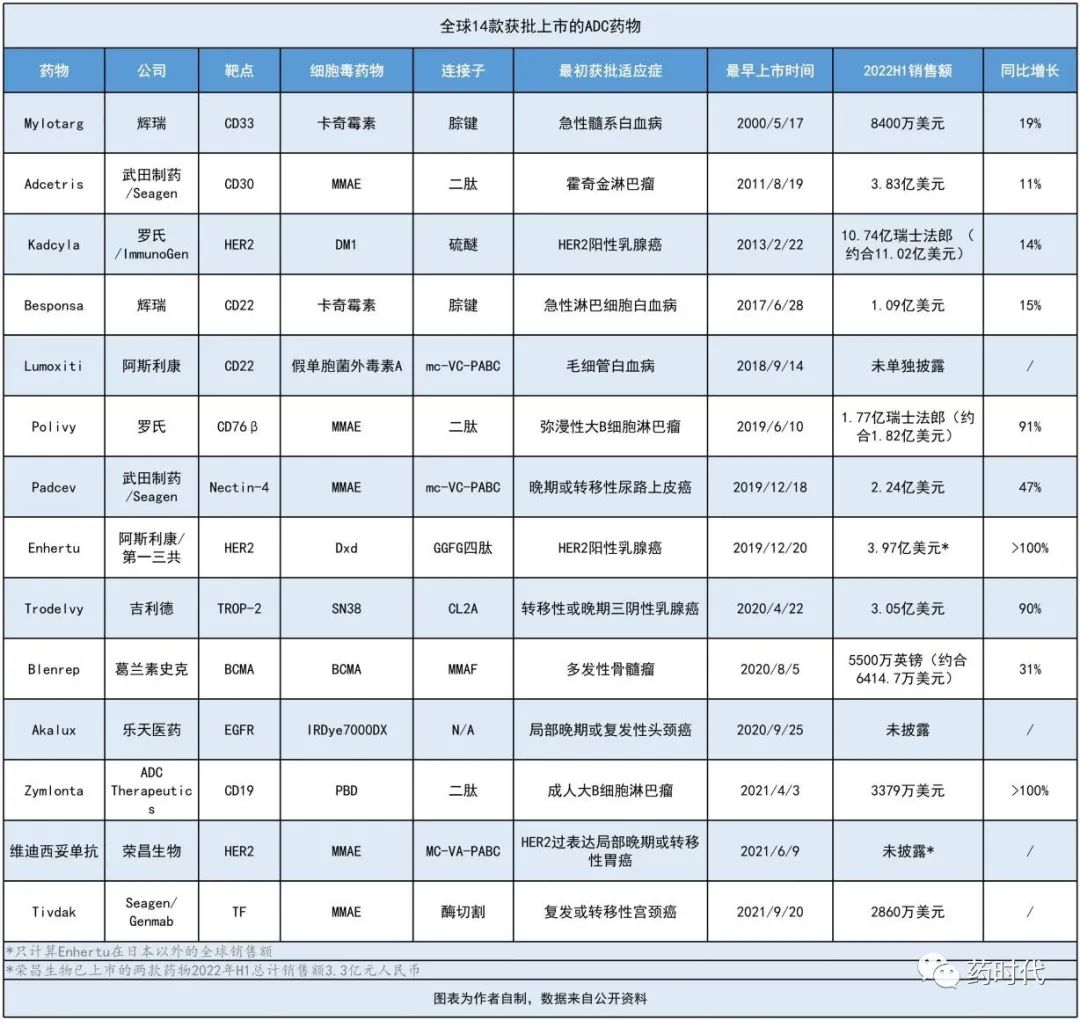
生物制药技术的发展,推动抗体偶联药物进入高速发展阶段,尤其是在肿瘤治疗领域,抗体偶联抗肿瘤药物的研发持续增长。
为了对抗体偶联抗肿瘤药物的临床研发中需要特殊关注的问题提出建议,并指导企业开展更为科学的临床研发,药品审评中心组织撰写了《抗肿瘤抗体偶联药物临床研发技术指导原则》,形成征求意见稿,供药物研发相关人员参考。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:夏琳,宋媛媛
联系方式:xialin@cde.org.cn,songyy@cde.org.cn
感谢您的参与和大力支持。















附件3:《抗肿瘤抗体偶联药物临床研发技术指导原则(征求意见稿)》起草说明



03
药时代发布的~100篇ADC文章

封面图来源:123rf

推荐阅读
 点击这里,报名参加第三届中国新药CMC高峰论坛!
点击这里,报名参加第三届中国新药CMC高峰论坛!



 个人中心
个人中心
 我是园区
我是园区




