文章作者多达 28 位,投稿期间经历 4 次修改,从 2020 年 1 月第一次投稿,历时 22 个月,27 页正文,93 页附件,18 个视频。

图 | 相关论文(来源:Nature Biotechnology)
11 月 16 日,哈工大仪器学院海归教授李浩宇参与的最新论文,终于发表在 Nature Biotechnology 上。他表示:“只要对这个世界还有好奇心,我们追求分辨率的脚步就不会停止。”

图 | 李浩宇(来源:李浩宇个人首页)
论文题为《稀疏解卷积增强活细胞超分辨荧光显微镜的分辨率》(Sparse deconvolution improves the resolution of live-cellsuper-resolution fluorescence microscopy),哈工大李浩宇教授和北大陈良怡教授为论文共同通讯作者。

图 | 当期论文(来源:Nature Biotechnology)
打破物理衍射极限

该论文的发表,也意味着李浩宇老师和合作者们,在光学超分辨显微成像技术领域取得了突破性进展。在低光毒性条件下,将结构光显微镜的分辨率,从原来的 110 纳米提升至 60 纳米,实现超快速、长时程的活细胞超分辨成像。
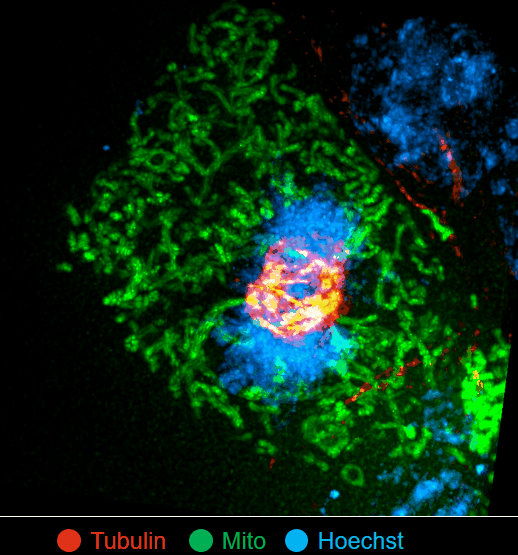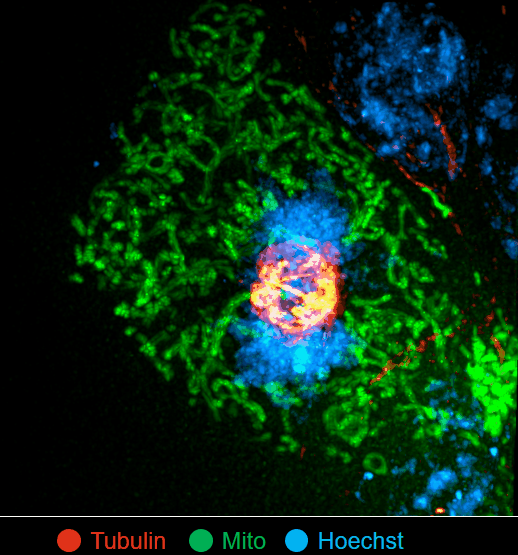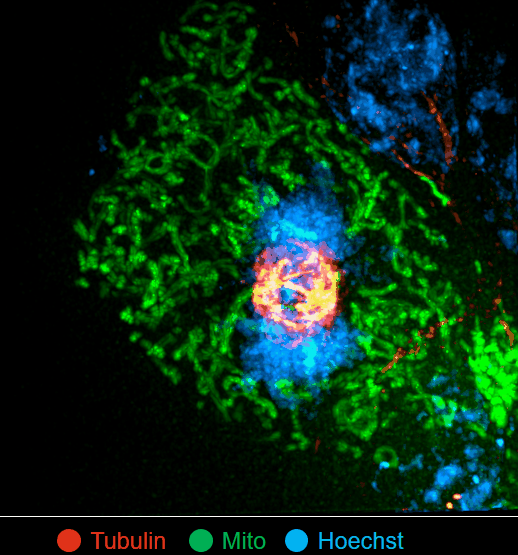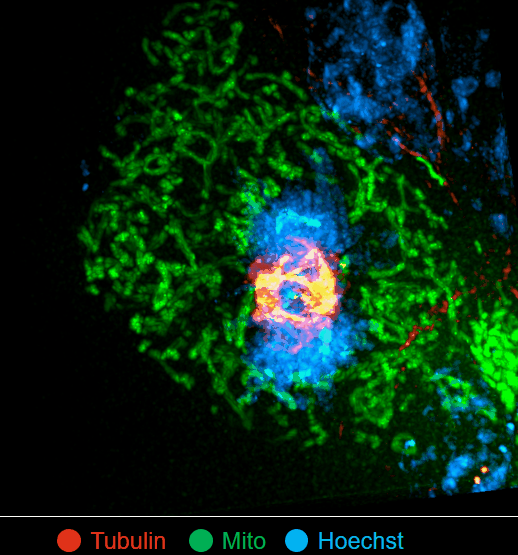
(来源:Nature Biotechnology)
李浩宇介绍称,光学超分辨打破了光的物理衍射极限。2014 年的诺贝尔化学奖,颁给了利用操控荧光蛋白的办法解决上述物理极限的科学家。
发展至今,物理方法和化学方法实现超分辨成像已经走到了瓶颈,追求更高的显微镜分辨率,正面临着很大的挑战。而本次研究实际上是一个广义的数学算法框架,可把几款常用的荧光显微镜仪器的成像分辨率提升两倍。
以转盘共聚焦显微镜为例,它的商用仪器正常分辨率是大约 160 纳米,借助该成果可把它提高到 80 纳米左右。因此该团队等于从最优化求计算的角度,把此前可达到的瓶颈极限分辨率向前推了一大步。
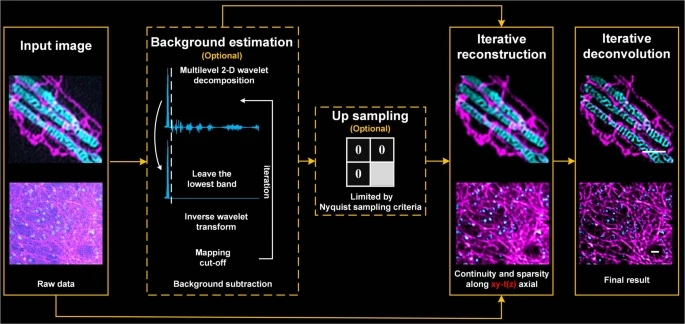
(来源:Nature Biotechnology)
研究中,他和团队提出一种计算显微成像方法,该算法可突破光学衍射极限,基本原理是借助荧光成像的前向物理模型以及压缩感知理论,当利用稀疏性和时空连续性的双约束条件时,即可建立起一种通用的图像解算方法,该框架搭载稀疏解卷积技术,让此前光学超分辨显微系统的硬件限制得以突破,时空分辨率和频谱也可得到扩展。
以此技术为基础,李浩宇等人联合北京大学陈良怡团队,合作研发出一款超快的结构光超分辨荧光显微镜系统(Sparse-SIM),具备超分辨、高通量、低毒性、非侵入等特点。当处于高速成像时,该系统不仅能实现 60 纳米的分辨率,也可实现1小时以上的超长时间活细胞动态快速成像。
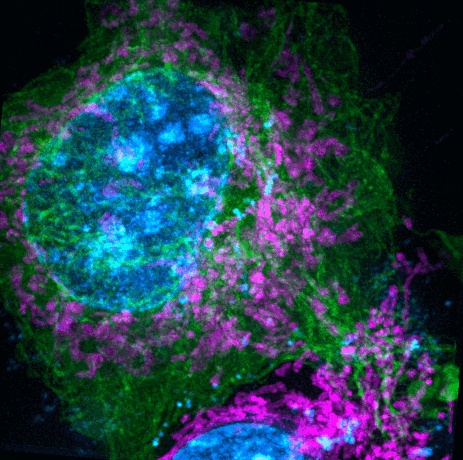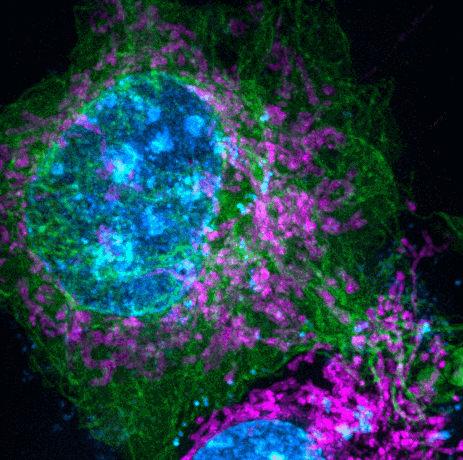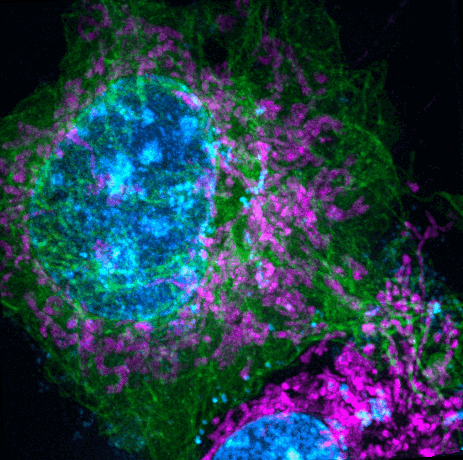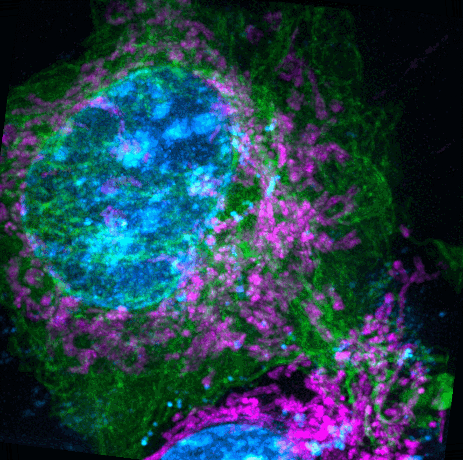
(来源:Nature Biotechnology)
借助该成果中的影像技术,肌动蛋白动态网络、细胞深处溶酶体和脂滴的快速行为也可得到观测,以及双色线粒体内外膜之间的精细运动也可被观测到。
概括来说,在物理方法和化学方法基础上,从另一个数学计算的角度出发,李浩宇和团队首次提出了一款突破光学衍射极限的通用算法模型,这不仅是从 0 到 1 的原创性研究,借此也研发出了活细胞光学显微成像中分辨率最高、成像时间最长、速度最快的超分辨显微仪器。
令人惊喜的是,该技术框架也被证明适用于目前多数荧光显微镜成像系统模态,均可实现近两倍的稳定空间分辨率提升,为精准医疗和新药研发提供了新一代生物医学超分辨影像仪器,使未来大幅度加速疾病模型的高精度表征成为可能。

(来源:李浩宇)
和北大团队的 “缘分” 合作

2017 年底回国入职哈工大后,李浩宇师一直专注于高分辨率光场显微镜,尽管这不是在超分辨尺度范畴,但是其的分辨率牺牲比较大一直困扰着这个领域,所以他一直在思考如何解决该难题。
2018 年 4 月,北京大学陈良怡教授发表了一篇领域内十分有影响力的论文,提出利用海森矩阵约束空时连续性,抑制结构光显微镜的高频伪影,实现了超灵敏的超分辨显微成像。他看到论文后,对提高分辨率也产生一些新想法,比如使用稀疏解卷积的方法,再结合海森矩阵,即可让数据的最优化迭代更加合理,如此便可得到更合理的约束,那么最终结果是否也更出色?

图 | 陈良怡(来源:资料图)
于是,李浩宇和其博士生赵唯淞在光场显微镜成像结果中进行了初步尝试,结果发现计算重建的已知尺寸的空心三维微球体的分辨率有明显的提高。

图 | 左:赵唯淞;右:李浩宇(来源:李浩宇)
2018 年 8 月,测量与仪器国际研讨会在云南举行,李浩宇有幸认识了北京大学的程和平院士,当时程院士和陈良怡老师刚刚发表了微型化佩戴式双光子荧光显微镜的新成果,李浩宇十分敬佩并借此机会也介绍了他自己最新的光场显微镜拍摄的细胞内线粒体动态变化的经过。
程院士对此十分感兴趣,邀请李浩宇去北大做报告。做报告时,陈良怡对他提到的算法很感兴趣,认为该算法也可能从超分辨系统移植到其他显微镜,并有不错的潜力。

图 | 程和平院士(来源:资料图)
当然,现在该论文的发表已经证明它可被移植到所有荧光显微镜中,但当时他们并未做出过于大胆的想象,怀着慎重态度和探索精神,只是不断地尝试,其中在结构光显微镜中,发现分辨率的确提高了。
但是,研究结构光显微镜的学者们很难接受这一观点,因为结构光显微镜在重建超分辨图像的过程中,在高频的频谱有滤波操作,所以人们认为在线性结构光显微镜系统中的高频谱是被人为滤掉的,大家会依据以往的经验认为这是已消失信息,不太相信可以再被恢复。
陈良怡在第一次看到重建后的图像分辨率提升这一结果后也非常惊讶,并打算小心的验证,为此想到了一个特别严谨的思路:小窝蛋白的尺寸大约有 60 个纳米左右,并且是一个圆环结构,如果真的能让分辨率从 110 纳米达到 60 纳米,那么就能分辨该蛋白的环状结构。
另外,为了验证实验更贴近生物学家的实际应用,特别选择在活细胞上做成像。接下来,陈良怡课题组做了大量实验数据,经过算法处理后发现果然可以分辨小窝蛋白的环状结构,而且测量统计出来的直径,也和非线性结构光显微镜下记录的结果十分吻合。
基于此,双方开始认真考虑计算方法能提高分辨率这一更大胆、也更广义的想法。在执笔论文时李浩宇写道,陈良怡老师很早就意识到,从实际成像的性能角度出发,真正做到活体细胞 60 纳米分辨率此前在全世界都是没有的。此前,一些做法是要抛开成像速度去谈成像分辨率,因此尽管当时很多成果报道称可达到 60 纳米分辨率,但并没有真正在活细胞任何状态下。因此,该团队当时提出这样的观点十分具有挑战性。

(来源:Nature Biotechnology)
倾尽全力,从质疑到认可

留学欧美,回国任职

2017 年 12 月,李浩宇的母校哈工大在全球招聘青年学者,随后他决定结束海外留学生涯,回到哈工大加入仪器学院担任教职。回国以后,以谭久彬院士团队为平台,他仍在坚持研究如何提高分辨率,以及如何才能构建出更好的显微镜计算框架,于是便有了文章开头的新成果。






 个人中心
个人中心
 我是园区
我是园区





