▲点击上方的蓝色“医谷”关注我们
“置顶公众号”获取最有价值行业趋势信息
医谷微信号:yigoonet
近日,科济药业Claudin18.2 CAR-T疗法CT041治疗消化道系统肿瘤的一期临床数据在《Nature Medicine》上发表。文章公布了详细的中期数据及CT041治疗患者的疗效和安全性特征、CAR-T细胞的扩增、CAR-T的免疫原性及CT041 T细胞亚群与临床疗效的相关性。

CT041是一种潜在全球同类首创的、靶向CLDN18.2的自体CAR-T细胞候选产品,用于治疗CLDN18.2阳性实体瘤,主要治疗胃癌/食管胃结合部腺癌及胰腺癌。此前,CT104已于2020年获FDA授予“孤儿药”资格,于2021年获欧洲药品管理局(EMA)授予“孤儿药产品”资格、“优先药物”(PRIME)资格,于2022年获FDA授予“再生医学先进疗法”(RMAT)资格。
此次发表于《Nature Medicine》的研究是一项在中国开展的、多中心、开放标签的Ⅰ期临床试验,旨在评估CT041治疗CLDN18.2表达阳性的晚期消化系统肿瘤患者的安全性、有效性和细胞代谢动力学。
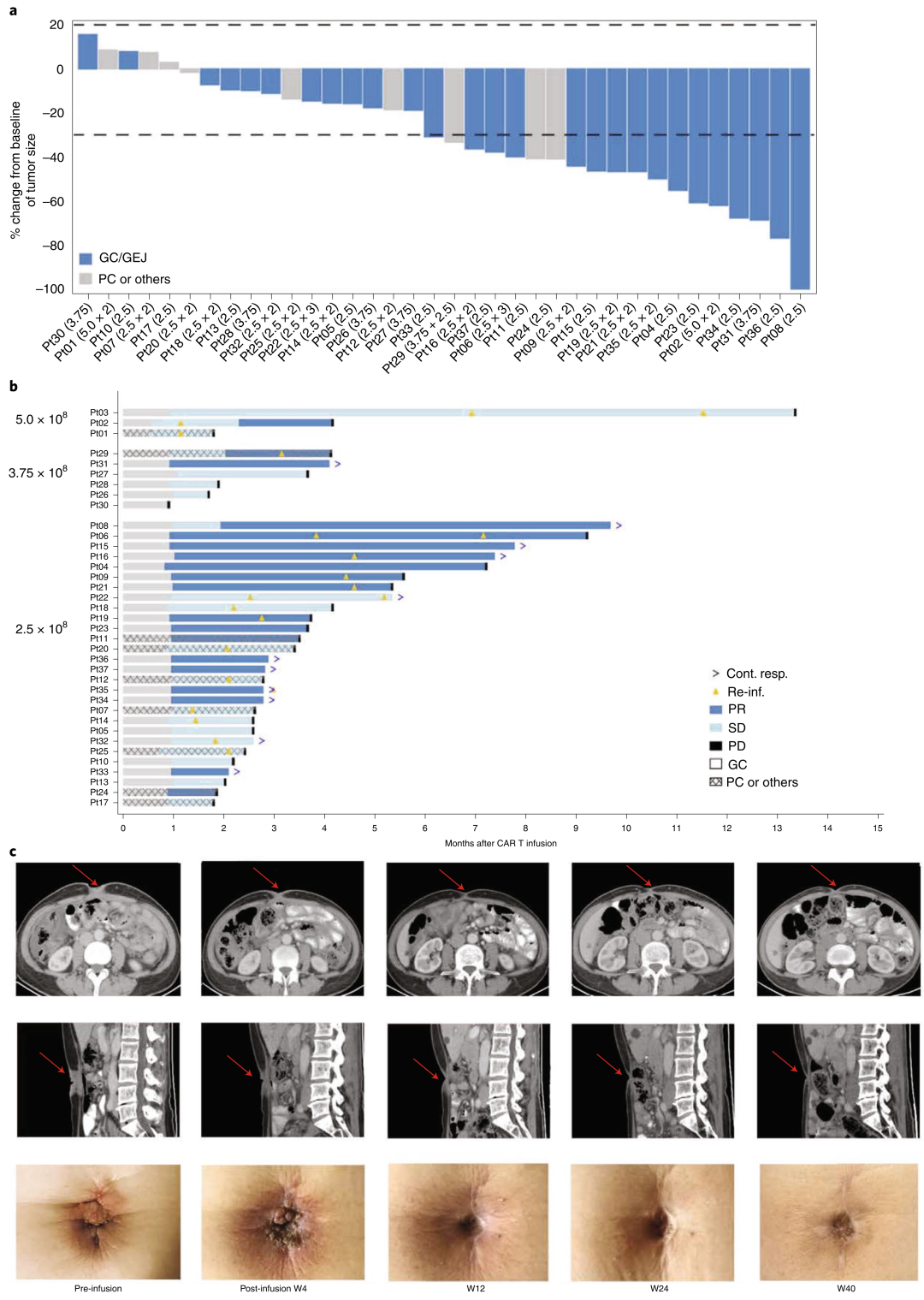
2019年3月26日至2021年4月8日,37例患者纳入此次中期分析,包括28例胃癌/胃食管结合部腺癌(GC/GEJ)患者、5例胰腺癌(PC)患者和4例其他消化系统肿瘤患者。所有患者均被确诊发生转移,其中50%得到患者转移累及至少3个器官。在28例GC/GEJ患者中,25例(89.3%)既往接受过至少2线治疗或氟尿嘧啶、奥沙利铂和紫杉醇的三联治疗,12例(42.9%)既往接受过抗PD-1/PD-L1单抗治疗。这些患者分别接受了2.5×10^8(28名)、3.75×10^8(6名)和5.0×10^8(3名)细胞剂量的CT041输注,并在第一次输注后完成了至少12周的安全性、有效性和药代动力学评估。自单采以来的中位随访时间为8.5个月(2.9-19.4个月)。



结果显示,在37例晚期消化系统肿瘤患者中,CT041整体耐受性良好且安全性风险可控,在输注后的28天内未发生剂量限制性毒性(DLT),最常报告的≥3级不良事件为预处理相关血液学毒性(37/37,100%)、白细胞减少症(31/37,83.8%)、中性粒细胞减少症(25/37,67.6%)、贫血(15/37,40.5%)和血小板减少症(6/37,16.2%)。这类血液学毒性AE发生于输注后28天内,中位恢复时间为4-9天。同时,35/37例(94.6%)患者发生1级或2级细胞因子释放综合征(CRS),未发生≥3级CRS,未发生神经毒性综合征(ICANS),无治疗相关死亡事件。疗效方面,在消化系统肿瘤患者中的客观缓解率(ORR)和疾病控制率(DCR)分别为48.6%和73.0%,在胃癌患者中的ORR和DCR分别达到57.1%和75.0%。

截止目前,CT041是全球唯一已获得美国FDA和中国国家药监局及加拿大卫生部的IND/CTA批准、并正在进行临床试验研究的靶向CLDN18.2的CAR-T细胞候选产品。科济药业计划于2024年上半年向中国国家药监局提交NDA,并计划于2024年向美国FDA提交BLA。
文 | 医谷
参考文献
《Claudin18.2-specific CAR T cells in gastrointestinalcancers: phase 1 trial interim results》(原文链接请点击下方“阅读原文”)
推荐阅读
《首次实现药物减重超20%,礼来tirzepatide三期结果出炉》






 个人中心
个人中心
 我是园区
我是园区




