
近期,勃林格殷格翰(BI)更新了靶向SOS1的新型口服泛KRAS抑制剂BI1701963国内临床研究状态。更新的信息显示,勃林格殷格翰已经主动终止了BI 1701963联合伊立替康治疗KRAS突变阳性不可切除的局部晚期或转移性结直肠癌患者的I期开放性剂量递增试验(CTR20201961)。
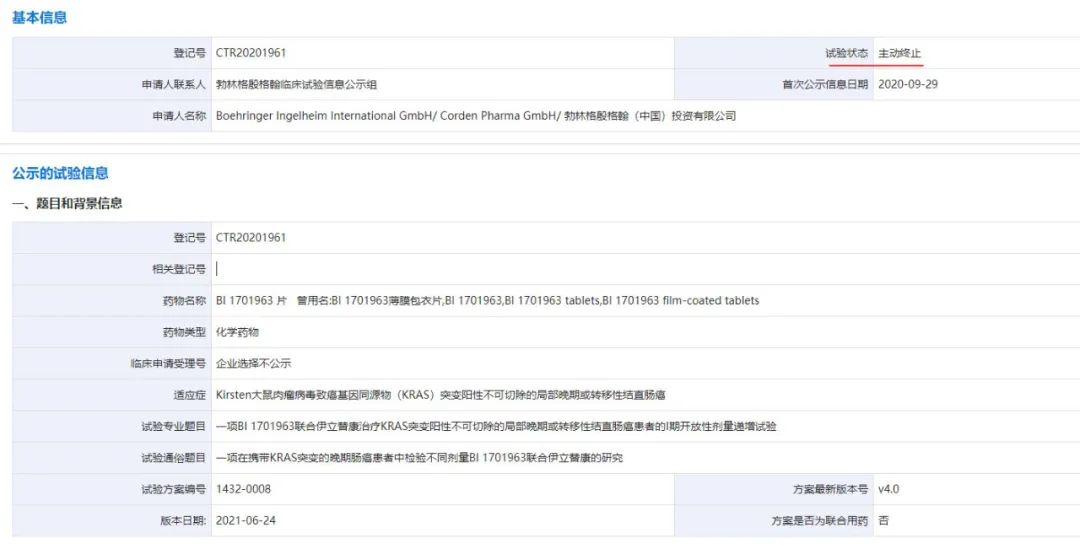
试验终止的原因主要是勃林格殷格翰对试验药物相关试验中产生的安全性、疗效和PK数据进行了分析,分析的结果是BI 1701963有了新的风险-获益评估结论。
主要包括:1)BI 1701963 的安全问题:致死性结局的 ILD 发生率高(在BI发起的试验中接受治疗的所有患者的3%以上),所有3例 ILD 病例均发生在亚洲患者中;关于暴露与ILD的关系无法得出确切的结论。2)BI 1701963 具有挑战性的PK特性:亚洲患者的平均暴露量较高(2-3 倍);所有剂量水平的变异性都非常高(不分种族)。3)非常有限的有效性:接受 BI 1701963 单药治疗的患者未确认缓解。因此,根据临床试验方案的要求(第3.3.4节),勃林格殷格翰决定终止试验。
BI 1701963通过与SOS1结合来抑制KRAS。通过将RAS绑定的GDP交换为GTP,SOS1能够帮助激活KRAS。对SOS1的选择性抑制体现了一种治疗概念,即无论KRAS突变类型如何,均可实现KRAS阻断,达到泛突变抑制。
此前,BI曾在EORTC-NCI-AACR、AACR、ESMO等多个国际会议上公布BI 1701963的临床前和临床研究数据。不过,正如BI所述, BI 1701963 单药治疗的患者未确认缓解,目前临床最好的疾病响应是SD。
2021年7月,Mirati Therapeutics开启了一项KRAS G12C抑制剂adagrasib联合BI 1701963治疗KRAS G12C突变晚期实体瘤的临床研究(NCT04975256)。BI在自主开发了一款KRAS G12C抑制剂BI 1823911之后,同期开始了BI 1823911单药或联合BI 1823911的临床研究(NCT04973163)。
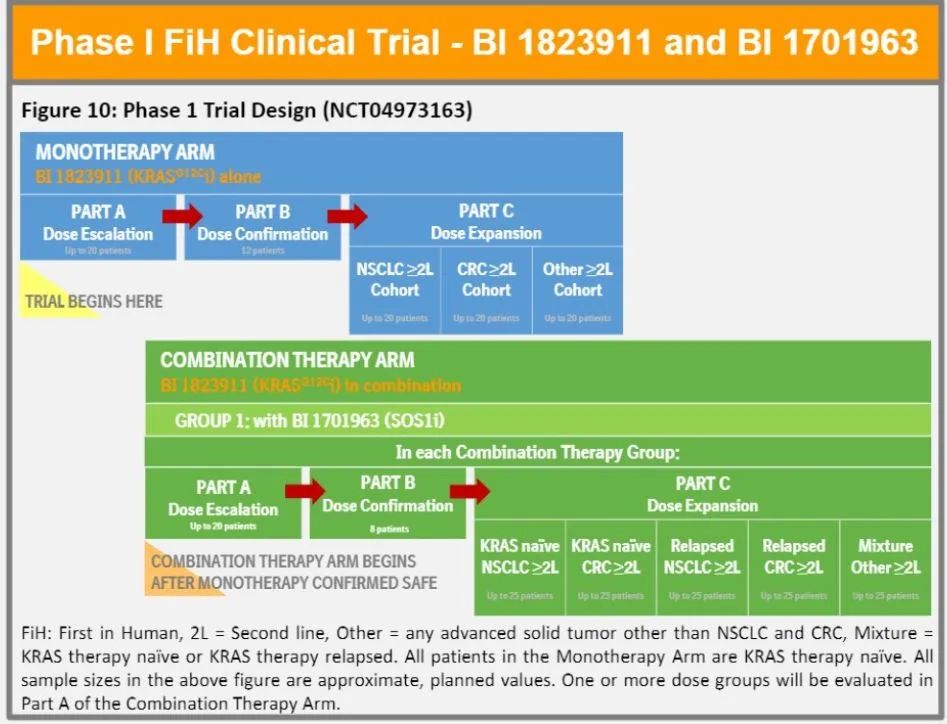
此外,clinicaltrials.gov网站信息显示,BI也已经终止了BI 1701963单药或联合MEK抑制剂BI 3011441 (NCT04835714)的临床研究。

推荐阅读



 个人中心
个人中心
 我是园区
我是园区




