
▎药明康德内容团队编辑
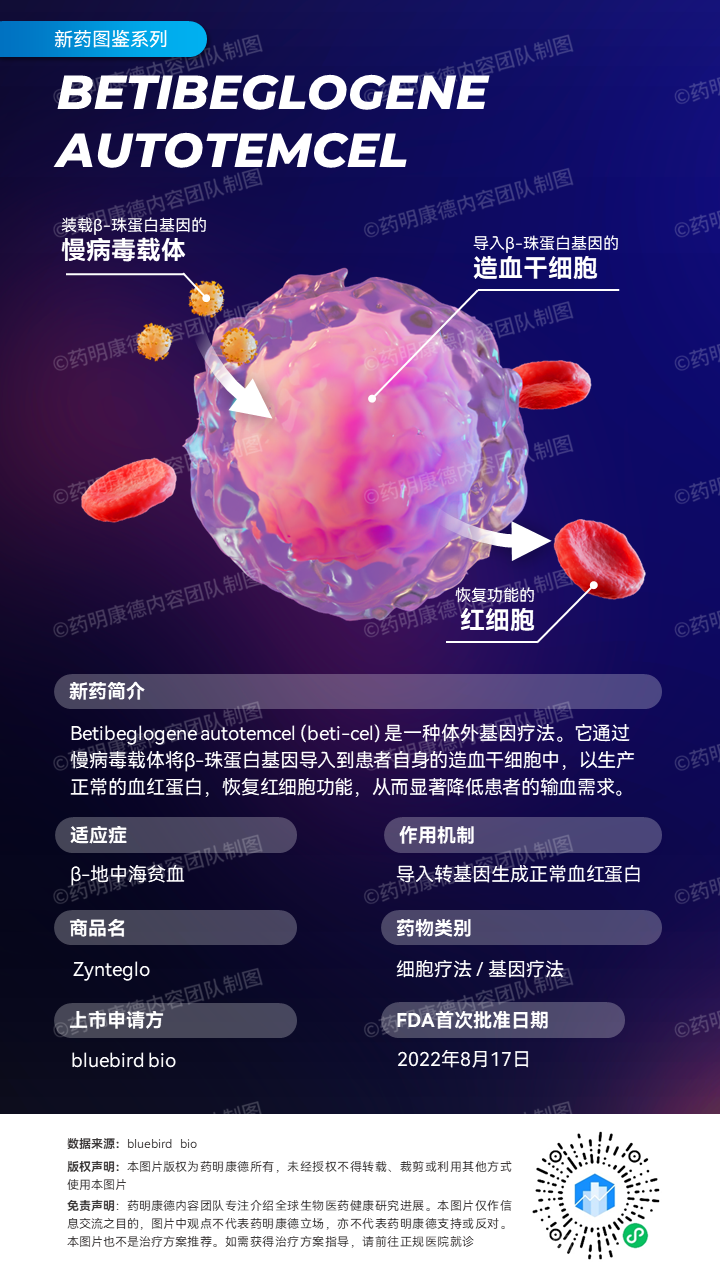
今日,美国FDA宣布,批准bluebird bio公司开发的基因疗法Zynteglo(betibeglogene autotemcel,beti-cel)上市,用于治疗需要接受常规血红细胞输注的β地中海贫血患者。新闻稿指出,这是针对这一患者群体首款获得FDA批准的基因疗法。

β地中海贫血是一种严重的遗传病。由于编码β珠蛋白的基因发生突变,患者体内的血红蛋白水平显著下降,甚至缺失。为了生存,患者不得不终身接受输血治疗。虽然输血可以暂时缓解与严重贫血相关的症状,包括疲劳、虚弱和呼吸急促,但它们并不能从根本上治疗疾病,并可能产生因为铁过载和多器官损伤导致的严重并发症。
Zynteglo是一款一次性基因疗法。它将从患者体内分离的造血干细胞在体外进行基因工程改造,让它们能够生成功能正常的β珠蛋白。
这些造血干细胞在输注回患者体内后,会源源不断地生成具有正常功能的血红细胞,极大减少患者对输血的需求。在理想情况下,患者甚至不需要进行输血治疗。这款疗法此前已获得FDA授予的孤儿药资格、突破性疗法认定和优先审评资格,并在欧盟获得批准。
Zynteglo的效果和安全性得到两项多中心临床研究的支持。参与者包括需要接受常规血红细胞输注的成人和儿童β地中海贫血患者。疗效的评估标准为输血独立性(transfusion independence),定义为患者在不接受血红细胞输注的情况下,维持预定的血红蛋白水平至少12个月。在接受Zynteglo治疗的41名患者中,89%达到输血独立性。最新随访结果显示,这一疗效表现出良好的持久性。
bluebird bio公司首席执行官Andrew Obenshain先生表示:“经过十多年的研究和临床开发,依托临床医生、患者和他们家人的韧性,Zynteglo的获批是基因疗法领域的分水岭。作为美国FDA批准治疗β地中海贫血的首款慢病毒载体离体基因疗法,我们正在揭开一个新时代的帷幕。针对承受终身治疗负担的患者,基因疗法具有革新已有治疗模式的潜力。”
今年是基因疗法治疗血液疾病大爆发的一年
,除了Zynteglo获得美国FDA批准,BioMarin Pharmaceutical公司开发的基因疗法Roctavian(valoctocogene roxaparvovec)也已经获得欧洲药品管理局
人用药品委员会的支持
,有望在今年成为首款获批治疗血友病A的基因疗法。CSL Behring与uniQure合作开发的基因疗法etranacogene dezaparvovec也已经获得美国FDA授予的
优先审评资格
,有望在今年成为首个治疗血友病B的基因疗法。期待创新疗法的出现让患者摆脱终身接受治疗的负担,迎接更为健康、积极的生活!
了解更多FDA获批新药
请点击下图访问我们的小程序


作为药明康德旗下专注于细胞和基因疗法的CTDMO,药明生基致力于加速和变革基因和细胞治疗及其他高端治疗的开发、测试、生产和商业化。药明生基能够助力全球客户将更多创新疗法早日推向市场,造福病患。如您有相关业务需求,欢迎点击下方图片填写具体信息。

▲如您有任何业务需求,请长按扫描上方二维码,或点击文末“阅读原文/Read more”,即可访问业务对接平台,填写业务需求信息
参考资料:
[1] FDA Approves First Cell-Based Gene Therapy to Treat Adult and Pediatric Patients with Beta-thalassemia Who Require Regular Blood Transfusions. Retrieved August 17, 2022, from https://www.prnewswire.com/news-releases/fda-approves-first-cell-based-gene-therapy-to-treat-adult-and-pediatric-patients-with-beta-thalassemia-who-require-regular-blood-transfusions-301607860.html
[2] Bluebird wins U.S. approval for a gene therapy to treat patients with a rare blood disorder. Retrieved August 17, 2022, from https://www.statnews.com/2022/08/17/bluebird-wins-fda-approval-for-gene-therapy-for-beta-thalassemia/
[3] bluebird bio Announces FDA Approval of ZYNTEGLO®, the First Gene Therapy for People with Beta-Thalassemia Who Require Regular Red Blood Cell Transfusions. Retrieved August 17, 2022, from https://www.businesswire.com/news/home/20220817005667/en
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。










 个人中心
个人中心
 我是园区
我是园区






