BioNews | Solid Biosciences:公布DMD2期临床试验中期数据,盘前下跌14.8%
收藏
关键词:
临床期临床science
资讯来源:蹊之美股生物医药 + 订阅账号
发布时间:
2021-03-16
微信公众号:蹊之美股生物医药 / CaesarBiotech
标的公司:Solid Biosciences Inc. (NASDAQ:SLDB)
1、来自6名患者的中期数据提供了SGT-001在North Star动态评价量表(NSAA)、6分钟步行测试(6MWT)、肺功能测试(PFT)和经临床验证的由患者报告的结局指标(PROM)等功能终点获益的证据。
2、注射SGT-001的7号患者经历了短暂且可控的不良事件,没有严重不良事件发生(SAE)。在给药后17-37个月,6名
先前给药的患者未显示新的与药物相关的安全性发现;筛选和招募患者进入IGNITE DMD的工作仍在继续。
3、将在2021年肌肉营养不良协会(MDA)临床与科学线上会议上发表演讲。
4、公司将于美国东部时间下午4:30举行电话会议和网络广播,讨论临床数据和财务结果。
Solid Biosciences公布该数据后,盘前股价下跌14.8%,值得注意的是在我们的统计中,该公司在2020年Q4获得了3家基金的增持,分别是RA Capital,Boxer Capital和Perceptive Advisors,3家机构占该公司的Ownership也达到了29.51%。(
Solid Biosciences Inc. (Nasdaq: SLDB),一家专注于治疗杜氏肌营养不良症的生命科学公司,今天报告了令人鼓舞的中期功能性数据(NSAA,6MWT和PFT)、生物标志物数据,以及来自正在应用基因治疗候选药物SGT-001进行IGNIT DMDE I/II期临床试验的6名患者报告的结局指标(PROMs)。公司还宣布,IGNITE DMD 7号患者已安全给药,出现短暂且可控的不良事件,没有1例SAE。7号患者是根据先前报道的临床方案修订并使用其第二代工艺生产的SGT-001给药的第一位患者。此外,在给药后17-37个月,先前给药的6名患者未显示与药物相关的安全性发现。当前收集的所有数据以及给药的重新开始,都支持继续纳入受试者进入IGNITE DMD研究。
这些数据将在3月18日(星期四)举行的2021 MDA虚拟临床与科学会议的口头会议和公司主办的专题讨论会上介绍。
佛罗里达大学Powell基因治疗中心主任,儿科副主任,IGNITE DMD临床研究的首席研究员,医学博士Barry Byrne表示:“所有功能和生物标志物数据以及今天报道的患者报告的结局指标表明,SGT-001可能为杜氏肌营养不良症患者带来益处。与疾病的自然病史数据相比,这些早期数据令我特别感到鼓舞。我期待着IGNITE DMD的继续入组受试者,并随着研究的进行对数据进行评估。”
“根据修订的临床方案,我们对IGNITE DMD试验中根据修订的临床方案成功恢复给药以及使用第二代工艺生产的SGT-001感到鼓舞。随着IGNITE DMD临床试验的发展,第7位患者的安全给药使我们对剂量策略更具信心。我们感谢该患者及其家人以及所有选择参加临床试验的人。” Solid Biosciences首席执行官,总裁兼联合创始人Ilan Ganot说,“我们期待在2021年下半年继续纳入受试者进行治疗,并报告更多患者的临床结局。”
报告的数据收集来自治疗后12-24个月,IGNITE DMD给药的前6名患者,包括3名以低剂量(5E13vg/kg)给药患者和3名以高剂量(2E14vg/kg)给药患者的数据。来自延迟治疗队列的数据(作为未治疗对照组)与代表性自然历史数据一起进行评估。基线时,这6名患者的年龄为5岁-14岁。这些数据先前已与FDA,IGNITE DMD数据安全监控委员会的成员和临床顾问共享。
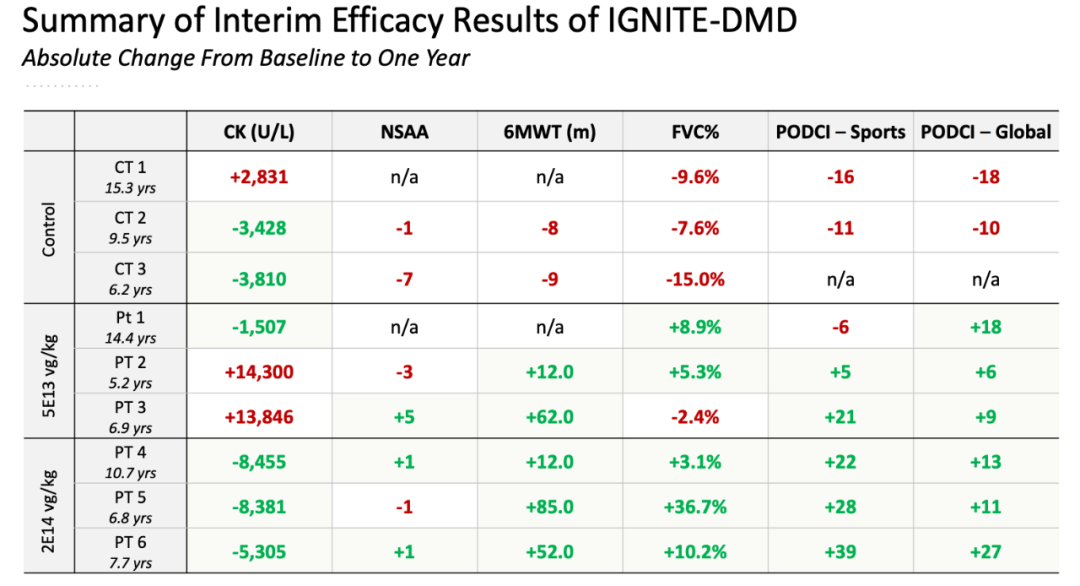
1、
在低剂量和高剂量队列的患者中,与自然史数据中通常观察到的轨迹相比,一年后的North Star动态评估量表(NSAA)得分表明治疗后受益。自然数据分析表明,与入选IGNITE DMD患者年龄相似的患者,正常情况下预计其疾病逐年进展,
得分范围从得分停止增长到下降3-3.7分。
未经治疗的对照组的患者从基线开始,1年平均下降4.0分。
低剂量组的患者同期平均改善1.0分,高剂量组患者相比基线平均改善了0.3分。
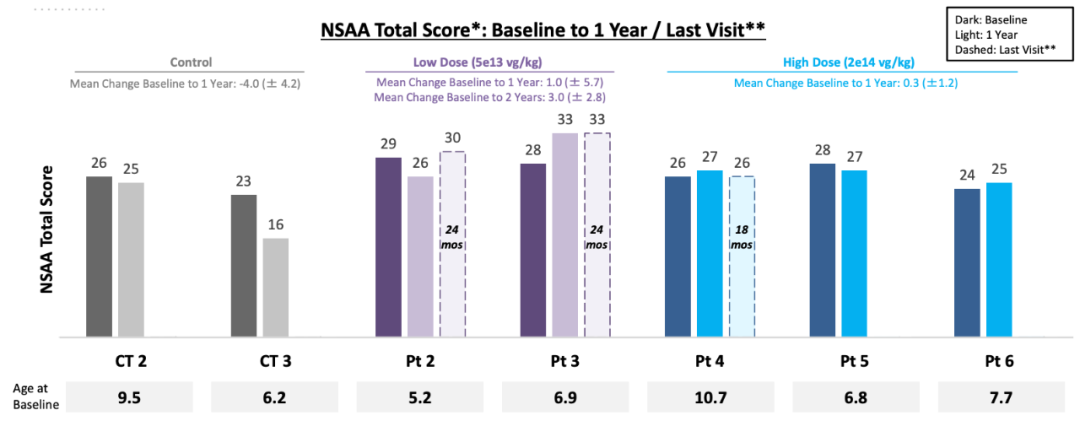
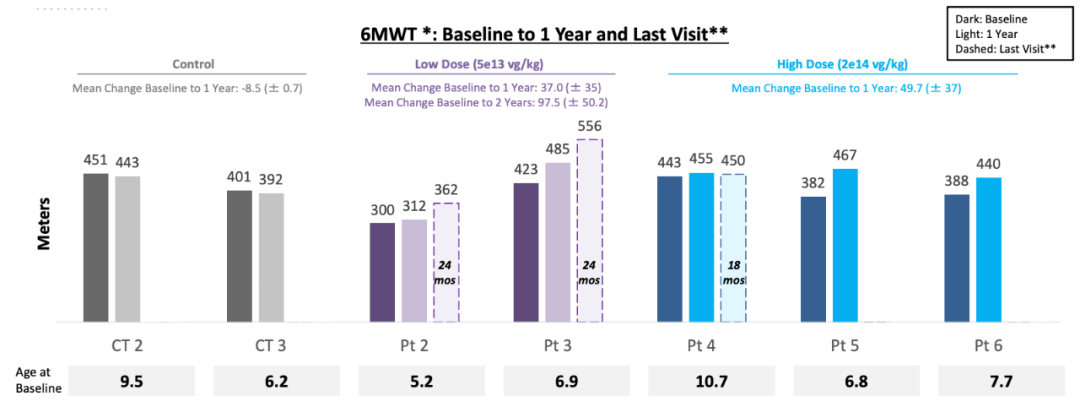
2、在治疗后的低剂量和高剂量组中,6分钟步行测试(6MWT)距离的平均改善均高于30米,这是普遍接受的具有临床意义的最小差异值(MCID)。未经治疗的对照队列患者从基线开始,一年下降8.5米,而低剂量队列患者的平均改善37米,高剂量队列患者同期平均改善49.7米。
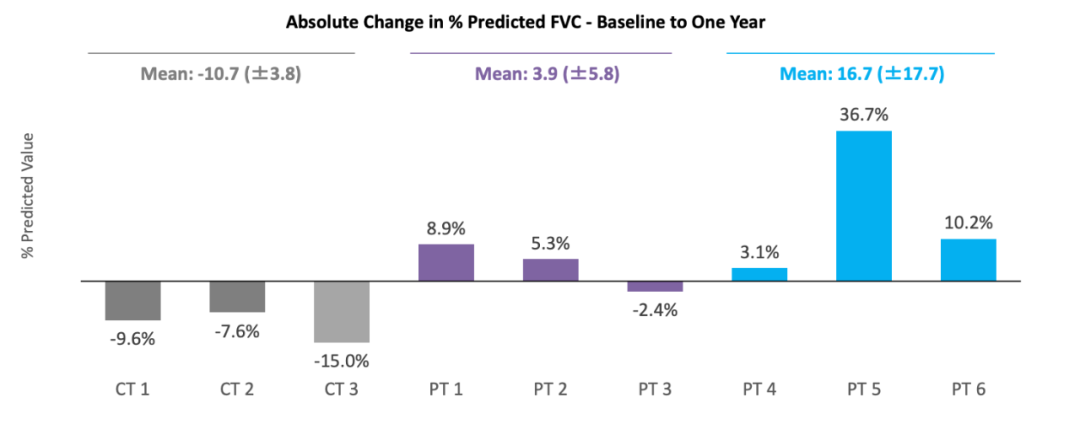
3、关于肺功能测试(PFT),这两个剂量组的大多数患者在一年内都表现出肺活量改善(预计FVC的百分比),杜氏肌营养不良症患者1年内通常可观察到肺功能下降。从基线到一年,未经治疗的对照队列患者的绝对值平均下降10.7%,而低剂量和高剂量队列的患者在同一时期平均改善分别为3.9%和16.7%。
1、如过去报道,以2E14vg/kg的剂量单次输注SGT-001后三个月的骨骼肌活检显示,微量肌营养不良蛋白阳性肌纤维广泛分布,与神经元一氧化氮合酶(nNOS)和β-糖聚糖的共定位于这些患者的肌肉中。
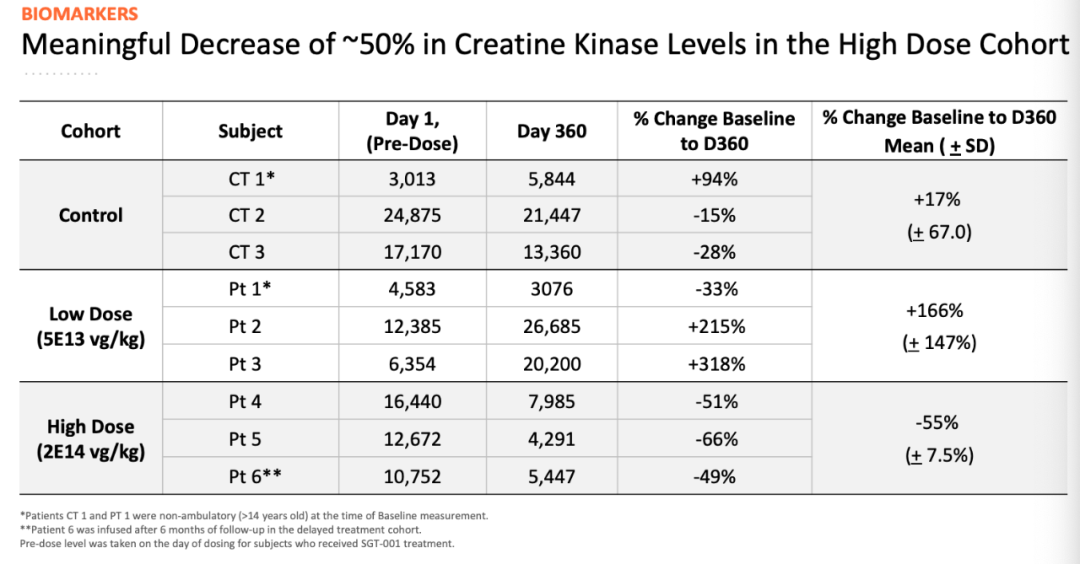
2、6名患者的肌酸激酶(CK)评估,为单次大剂量SGT-001输注治疗一年后提供了阳性或稳定作用的潜在生理证据。在高剂量队列中,患者平均持续CK下降约50%。在低剂量组中,CK平均增加约166%,而在对照组中,观察到平均CK增加约17%。
Patient Reported Outcome Measures (PROMs) Data
患者报告的治疗一年后的结局指标显示,运动功能分量表和疲劳性评估与剂量呈正比改善趋势,为支持低剂量和高剂量患者临床和生物标志物的不同程度受益,提供了真实世界的证据。
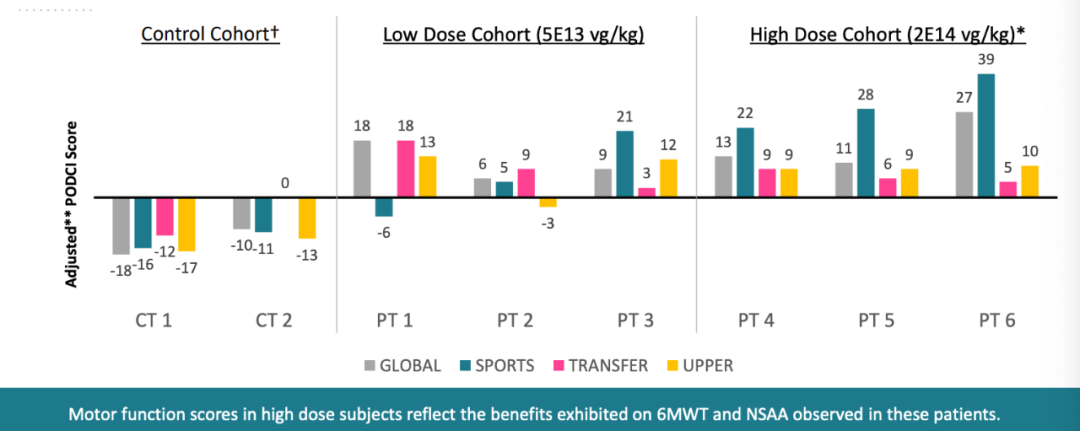
1、儿科结果数据收集工具(PODCI)呈现出有意义的改善,该工具已经过验证,它包含一些问题,可以帮助看护者和孩子评估步行、站立和执行日常活动以及娱乐活动的能力。运动功能评分同样反映了在所有剂量患者中观察到的6MWT的增加和NSAA的获益。
2、Modus Outcomes Ltd对患者和看护者进行的涉及杜氏肌营养不良症对功能的影响的半结构化、定性访谈证明,功能活动和学校相关影响(例如,下肢活动能力,与同伴保持同步,爬楼梯,运动)在低剂量和高剂量队列中得到整体改善,两个治疗队列的所有患者的主观疲劳性降低。
如先前的报道,在2020年实施的方案修订之前的首批6名患者中,有3名出现了4次严重不良事件(SAE)。先前的所有SAE均已完全解决,并且在给药后17-37个月的随访中未发现新的与药物相关的安全性发现。此外,正如今天报道的那样,随着IGNITE DMD给药恢复,第七例患者出现轻度至中度不良事件,这些事件均已完全解决。恢复给药是在一项经过修订的临床方案下进行的,并使用经过改进的工艺生产的SGT-001,两者均旨在提高患者的安全性。
Data Presentations at MDA
Byrne博士将于2021年3月18日(星期四)美国东部时间下午4:00在MDA会议上进行口头报告,介绍IGNITE DMD的疗效和安全性数据。同样,3月18日,PROM数据将在公司主办的午间下午12:00的研讨会上呈现。
Solid的SGT-001是一种新型的腺相关病毒(AAV)载体介导的基因疗法,旨在解决杜氏病的潜在遗传原因。Duchenne是由肌营养不良蛋白基因突变引起的,该突变导致肌营养不良蛋白缺乏。SGT-001是一种全身给药的候选药物,可将合成的肌营养不良蛋白基因(称为微肌营养不良蛋白)递送至人体。这种微肌营养不良蛋白编码在肌肉中表达的功能蛋白替代物,并稳定必需的相关蛋白,包括神经元一氧化氮合酶(nNOS)。来自Solid的临床数据表明,无论基因突变或疾病阶段如何,SGT-001都有减缓或阻止Duchenne肌营养不良的发展的潜力。
SGT-001是基于华盛顿大学Jeffrey Chamberlain博士和密苏里大学的段东升博士在肌营养不良蛋白生物学方面的开创性研究药物。SGT-001在美国被授予罕见儿科疾病称号(RPDD),并被授予快速通道称号,在美国和欧盟被授予孤儿药称号。
Solid Biosciences是一家生命科学公司,致力于推进变革性疗法以改善Duchenne肌营养不良症患者的生活。以疾病为中心,并由直接为受Duchenne影响的家庭创立。
追踪和剖析全球最前沿生物科技公司,寻找低估值/革命性的生物科技产品或技术平台,深入挖掘其投资价值。
联系方式:CaesarBiotech@aliyun.com






 药选址
药选址




