
关注我们
药谷消息
为抗击新冠肺炎进行的医药研发以及深入研究依然是目前全球科学家关注的热点之一。就在今天,张江科学城创新药研发企业和高校科研平台联合发布了重要消息!2月8日,Science在线发表了中国科学院上海药物研究所徐华强教授/尹万超博士团队与济民可信邓俗俊博士团队合作的题为“Structures of the Omicron spike trimer with ACE2 and an anti-Omicron antibody”的最新成果!
该论文由济民可信邓俗俊博士团队与中科院上海药物所徐华强教授/尹万超博士团队联合发表,阐述了奥密克戎变异株传播和免疫逃逸的分子机制,揭示治疗抗体JMB2002的作用机制,为广谱抗新冠抗体的研发提供了新的思路,也为全球新冠疫苗研发提供新的参考。

该研究解析了Omicron刺突蛋白与人源受体ACE2或广谱抗新冠抗体JMB2002复合物的高分辨冷冻电镜结构,阐述了Omicron变异株传播迅速和免疫逃逸的分子机制,并揭示了治疗抗体JMB2002全新的作用机制,为JMB2002对新冠病毒Omicron变异株仍具有中和功能及进一步开展临床试验研究提供了理论基础。为广谱抗新冠抗体的研发提供了新的思路,也可为全球新冠疫苗研发提供新的参考。

研究者发现Omicron刺突蛋白结合其受体ACE2相比于野生型提高6-9倍,通过解析Omicron变异株刺突蛋白与人源受体蛋白ACE2复合物的高分辨率冷冻电镜结构(图1A),从结构中观察到Omicron刺突蛋白三聚体相邻的RBD存在相互作用(图1B),利于Omicron刺突蛋白的RBD持续处于开放状态,增强了Omicron变异株的传染性;结合热动力学实验发现Omicron刺突蛋白的RBD高度灵活且不稳定,其热溶解温度降了超过5 °C(图1C),使得刺突蛋白更容易从闭合构象向开放构象转换,进一步增强Omicron变异株的传染性。简而言之,Omicron刺突蛋白RBD的相互作用及不稳定性,促进Omicron刺突蛋白与ACE2的相互作用,从原子水平解释了Omicron变异株传染性增强的潜在机制。
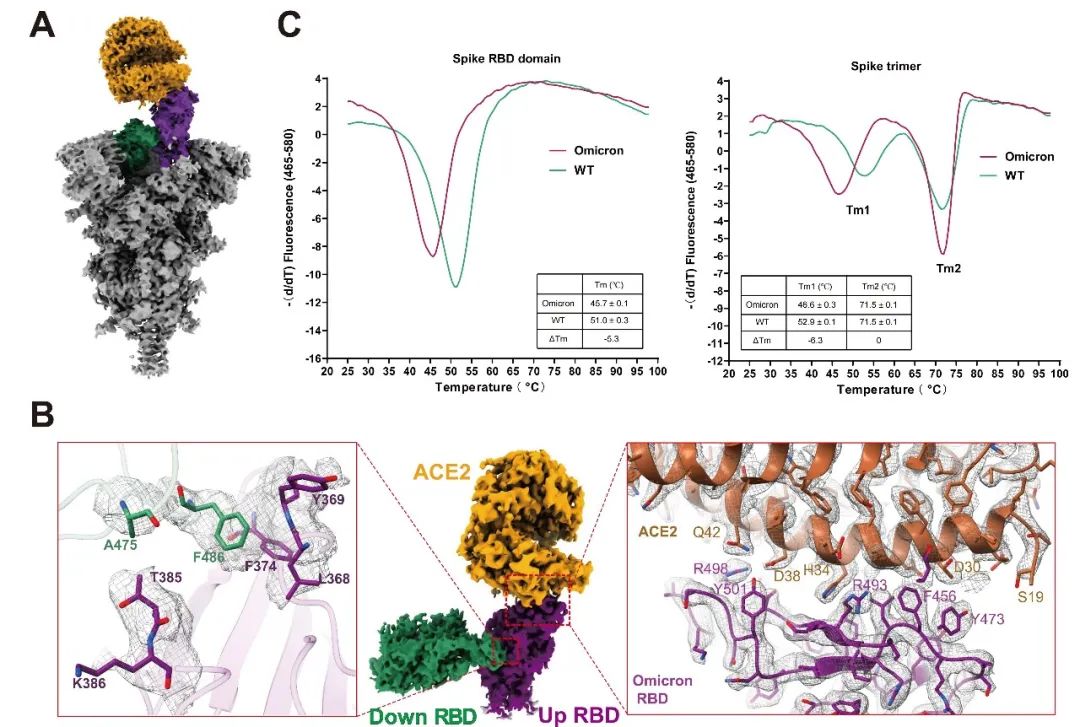
图1 Omicron刺突蛋白结合人源受体ACE2的结构。A展示Omicron刺突蛋白结合人源ACE2结构的整体构象,B为RBD-RBD二聚体,以及RBD结合ACE2的相互作用界面,C为刺突蛋白的热稳定结果。
从解析的结构中看到Omicron刺突蛋白的众多突变位点位于蛋白表面,导致了大部分中和抗体对Omicron突变株失去了中和活性。值得庆幸的是,济民可信自主研发的新冠中和抗体JMB2002对Omicron刺突蛋白的亲和力是对野生型的4倍,展示出强大的抑制Omicron变异株的潜力。为阐述JMB2002抗Omicron变异株的分子机制,研究者解析了Omicron刺突蛋白与JMB2002复合物的结构(图2A-C);从结构中发现Omicron刺突蛋白三聚体内同样存在RBD相互作用(图2D),JMB2002抗体结合Omicron刺突蛋白RBD后阻碍了人源受体蛋白ACE2与RBD的结合(图2E);令人惊奇的是,JMB2002以一种全新的构象结合在RBD与人源ACE结合界面的背部,是一种全新的结合表位的中和抗体(图2F)。
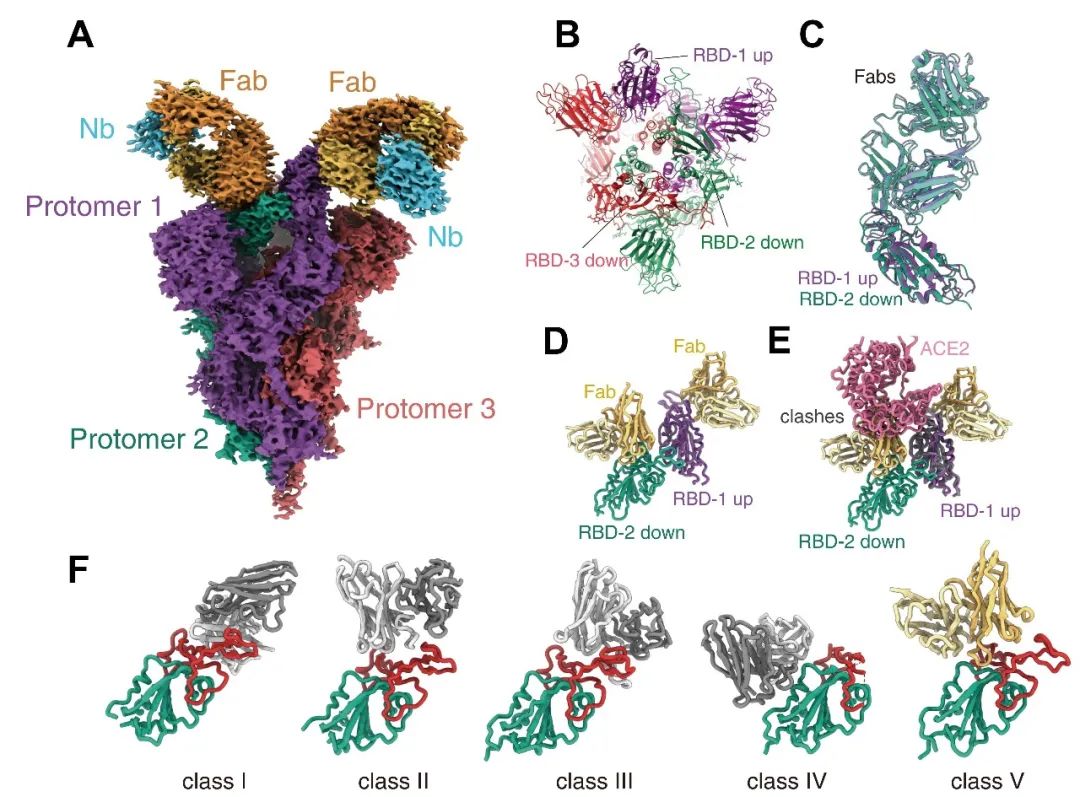
图2 Omicron刺突蛋白结合抗体JMB2002的结构。A展示JMB2002抗体结合Omicron刺突蛋白的整体结构,B复合物中Omicron刺突蛋白的构象,C为与JMB2002抗体结合的两个RBD的结构比较,D为JMB2002抗体结合Omicron刺突蛋白的结构中RBD-RBD的二聚体,E展示了JMB2002抗体结合Omicron的RBD后阻断ACE2进一步结合,F为抗新冠病毒中和抗体的分类,JMB2002抗体为新型抗体,被归为第五类。
在新冠病毒变异株Omicron大流行之际,本次研究成果极具原创性与新颖性,论文通过同行评审并在Science发表,将助力全球科研工作者充分了解Omicron变异株的特性,为JMB2002对新冠病毒Omicron变异株仍具有中和功能及进一步开展临床试验研究提供了理论基础。为广谱抗新冠抗体的研发提供了新的思路,也可为全球新冠疫苗研发提供新的参考。
上海药物所徐华强教授团队主要成员和济民可信邓俗俊博士团队主要成员为该文的共同第一作者。上海药物所徐华强教授、尹万超研究员和济民可信邓俗俊博士为该文共同通讯作者。
据公开信息显示,目前国内共有7款抗新冠药物在研。
7款在研抗新冠药物
1.VV993--由中国科学院上海药物研究所和中国科学院武汉病毒研究所共同研发:
1月26日,君实生物公司与苏州旺山旺水生物医药有限公司(旺山旺水)达成合作,共同承担靶向3CL蛋白酶的可口服抗新冠病毒候选新药VV993在全球除乌兹别克斯坦、吉尔吉斯斯坦、哈萨克斯坦、土库曼斯坦、塔吉克斯坦(中亚五国)外的国家或地区范围内的研究、生产及商业化工作。
2、VV116--由上海药物所、武汉病毒所、中国科学院新疆理化技术研究所、旺山旺水、中国科学院中亚药物研发中心共同研发,由君实生物与旺山旺水共同承担该药物在全球范围内的临床开发和产业化工作:
首款小分子口服核苷类抗新冠病毒药物VV116目前正在开展全球多中心临床研究,其中3项在中国开展的I期研究已于近日完成,初步结果显示临床安全性良好,针对轻中度COVID-19患者的国际多中心II/III期临床试验正在进行中。
3、GDI-4405--由清华大学等科研机构自主研发:
1月25日,由全球健康药物研发中心主任、清华大学药学院院长丁胜表示临床候选药物分子,以新型冠状病毒3CL蛋白酶为靶标的临床前候选特效药物分子GDI-4405加速推进多项临床试验申报研究和药物生产,预计2022年下半年进入临床。
4、BRII-196/BRII-198--清华大学与深圳市第三人民医院及腾盛博药合作研发:
2021年12月8日,由清华大学医学院教授、清华大学全球健康与传染病研究中心与艾滋病综合研究中心主任张林琦教授领衔研发的的新冠单克隆中和抗体安巴韦单抗罗米司韦单抗联合疗法(此前称BRII-196BRII-198联合疗法)获得中国药品监督管理局(NMPA)的上市批准,用于治疗新型冠状病毒(SARS-CoV-2)检测结果为阳性,同时伴有进展为重型COVID-19危险因素的成人和儿童(≥12岁,体重≥40kg)患者。此获批标志着中国拥有了首个全自主研发并经过严格随机、双盲、安慰剂对照研究证明有效的抗新冠病毒特效药。
5、JS016--中国科学院微生物研究所与上海君实生物联合开发,君实生物授权礼来在大中华区外的市场进行商业化开发:
我国自主知识产权的新冠肺炎治疗性抗体新药JS016已完成国际多中心Ⅱ期临床试验,正在积极推进Ⅲ期临床试验。礼来公司将JS016抗体与其自有的另一株单抗联合进行了多个Ⅲ期临床试验,结果显示,对轻到中度伴有转重症高危风险的新冠肺炎病人而言,联合疗法能显著降低其住院和全因死亡事件的发生风险(70%~84%),对死亡病例的保护达100%。该联合疗法获得了美国、欧盟、印度、巴西等15个国家和地区的紧急使用授权,是目前三个在国际上使用的新冠抗体疗法之一。
6、BGB-DXP-604--由北京大学和北京丹序研发:
已于2021年2月获得国家药监局批准开展临床试验,并已在澳大利亚完成I期临床试验,安全性和耐受性良好。
7.2B11--国药集团的中国生物与中科院上海高等研究院、中科院武汉病毒研究所合作研发:
目前还未进入临床试验。

本文消息来源于企业,7款抗新冠肺炎药物信息来源于网络公开信息





 个人中心
个人中心
 我是园区
我是园区




