CAR-T细胞疗法在治疗B细胞恶性肿瘤方面显示出高应答率和持久的疾病控制。然而,在实体瘤中,CAR-T细胞表现出的疗效有限,这部分归因于CAR信号的内在缺陷。
近日在Science Translational Medicine期刊上的“Chimeric STAR receptors using TCR machinery mediate robust responses against solid tumors”研究报道了清华大学林欣教授团队的发明的STAR(synthetic T cell receptor (TCR) and antigen receptor)技术,有望解决CAR-T在实体瘤中表现不佳的困境。
STAR结合了抗体的抗原识别结构域和TCR的恒定区,使用了内源性CD3信号转导机制(图1)。其不仅可以通过TCR的信号激活T细胞,同时又不受抗原识别分子MHC的限制,具有直接识别抗原的能力。通过这种构象,STAR有望继承其亲本抗体的高亲和力和特异性,并维持天然TCR复合物的有效的信号传导能力。
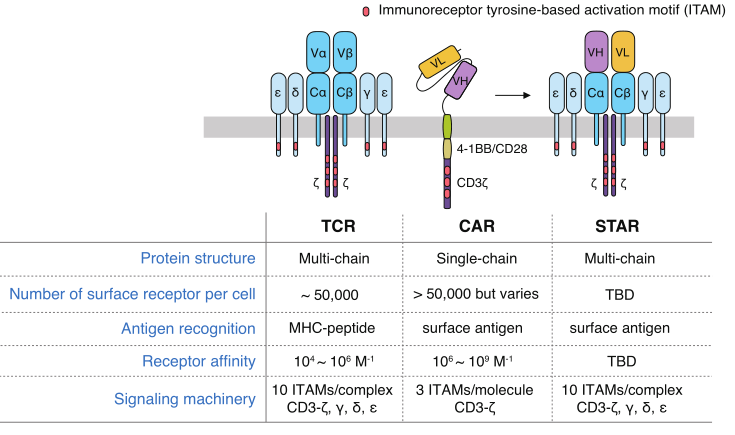
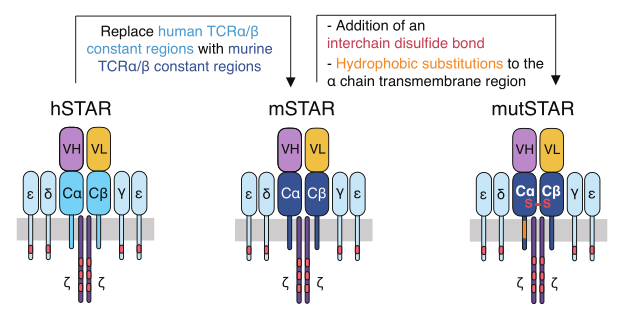
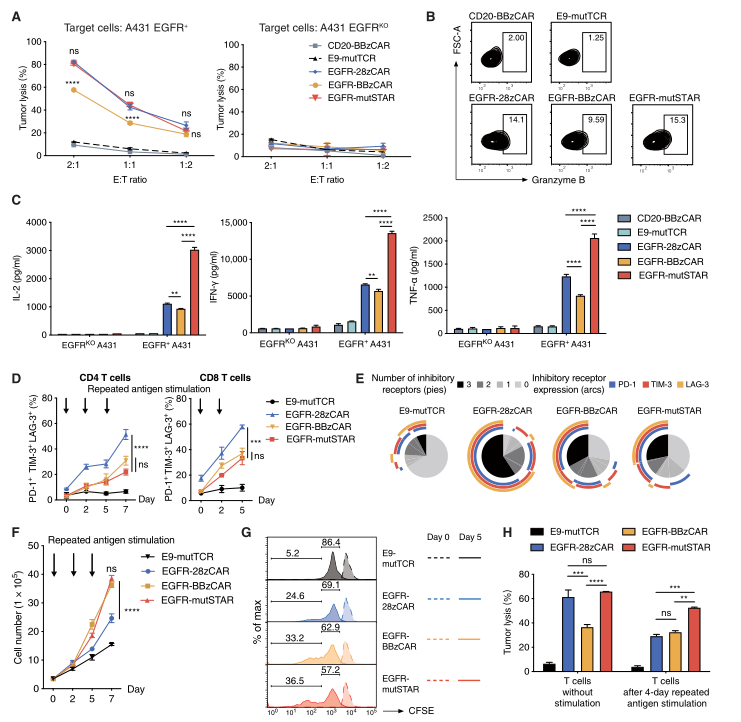
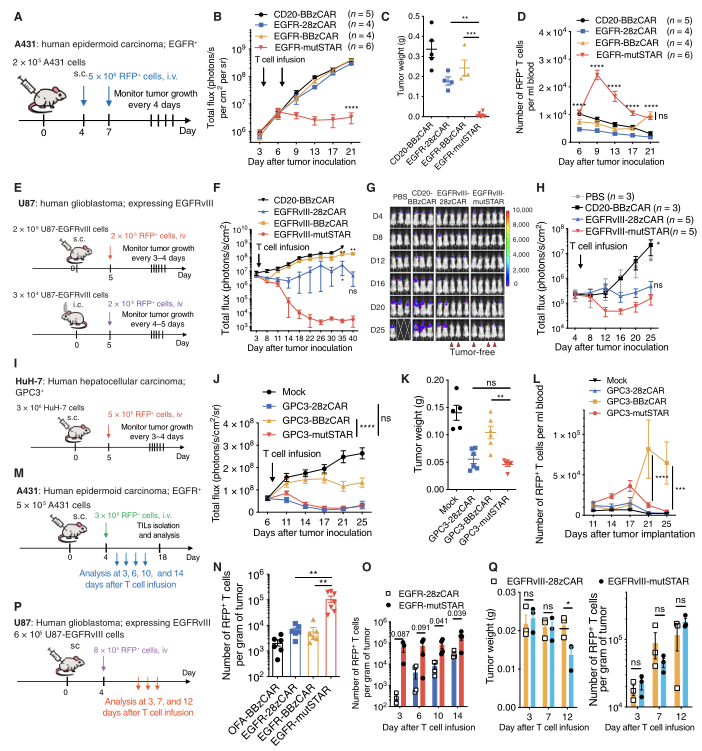
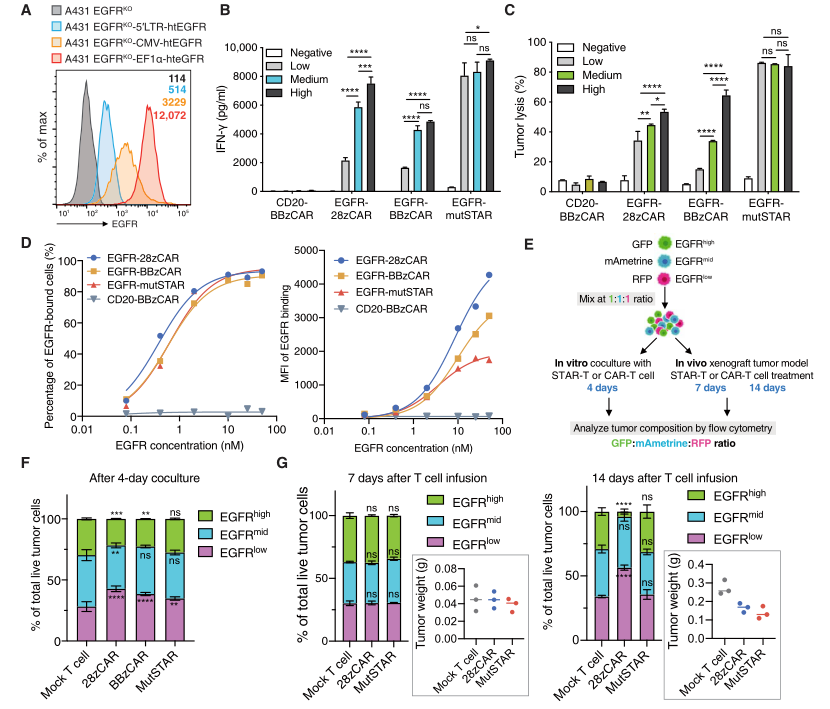
图5. MutSTAR-T比CAR-T对抗原低的肿瘤表现出更高的敏感性
小编总结
STAR-T兼具CAR-T的抗体特异性识别抗原以及高亲和力的特点,以及类似天然TCR的信号转导能力。临床前实验证明了STAR-T具有优越的抗肿瘤活性,且无明显毒性。由于天然TCR样信号的优势,STAR-T细胞可能在治疗难治性实体肿瘤方面具有优势。
STAR-T技术平台目前为华夏英泰的创新型T细胞改造技术平台 ,由著名免疫学家林欣教授团队创建,目前已经有多款针对实体瘤的产品在研(图6),我们期待后续的临床进展。
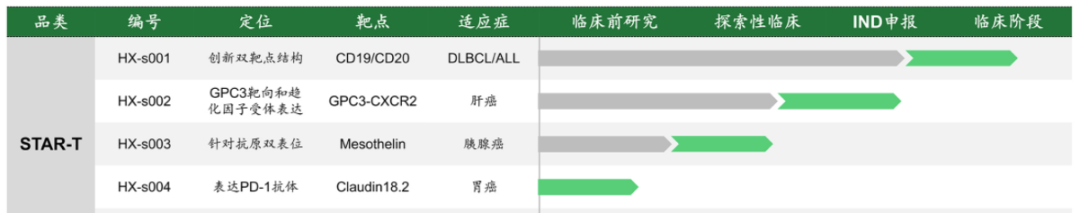
图6. 华夏英泰的STAR-T技术平台的肿瘤管线
参考来源
1.Chimeric STAR receptors using TCR machinery mediate robust responses against solid tumors.
2.华夏英泰官网。
 ▼点击【阅读原文】,了解更多~
▼点击【阅读原文】,了解更多~



 个人中心
个人中心
 我是园区
我是园区










