您还不是认证园区!
赶快前去认证园区吧!
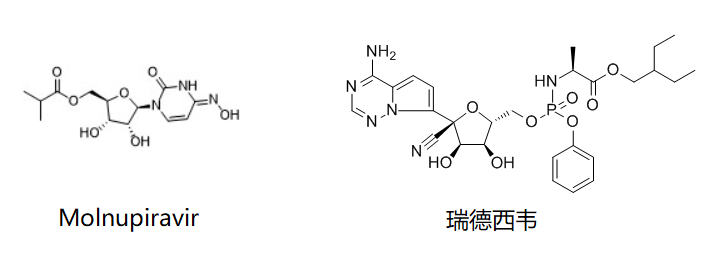
11月4日,默沙东/Ridgeback宣布英国药品和保健产品监管局(MHRA)已在英国批准molnupiravir (MK-4482, EIDD-2801)上市,用于治疗轻至中度COVID-19成人患者。Molnupiravir是全球首个获批用于治疗成人轻度至中度COVID-19的口服抗病毒药物,这些患者经SARS-CoV-2诊断测试呈阳性且至少存在一个发展为严重疾病的风险因素。

点击图片,进入优惠报名通道,立减1000元!
EBC作为连通生物医药全产业链的大型会+展,在论坛和展览双通道模式下,从上游原料/设备-科研-产业-临床-投资等方面,全方位覆盖BIO领域从业者。其中EBC展览旨在为生物医药企业提供一站式采购服务。
展览名称:2022第七届易贸生物产业展览EBC
展览时间:2022年2月26-28日
展览面积:30000平(苏州国际博览中心B1C1D1馆)
参展机构:300+(涵盖原辅料、试剂、耗材、设备、服务、工程等生物产业供应链各环节)
观众人数:10000+(来自IVD/创新药/细胞与基因治疗/mRNA等细分领域的管理层和中层负责人)

易企说专访
|
周珺 |
|||
近期融资/IPO
|
|
|
|
|
|
|
|
行业分析




 个人中心
个人中心
 我是园区
我是园区




