【CMC 与仿制药】
10.21【FDA】BE 指南 新增8篇,修订72篇
【注册、审评、审批】
【创新研发与临床】
10.20【FDA】指南定稿 临床研究中多个终点
【GxP 与检查】
【药典相关】
【监管综合】
10.17【EU】全球药品供应链的脆弱性 - 关于药品供应安全的结构性对话
10.19【FDA】推进真实世界证据计划
【医疗器械】
(内容导读请在下列文本框中上下滑动查看,可点击跳转至识林小程序阅读原文)
【CMC 与仿制药】
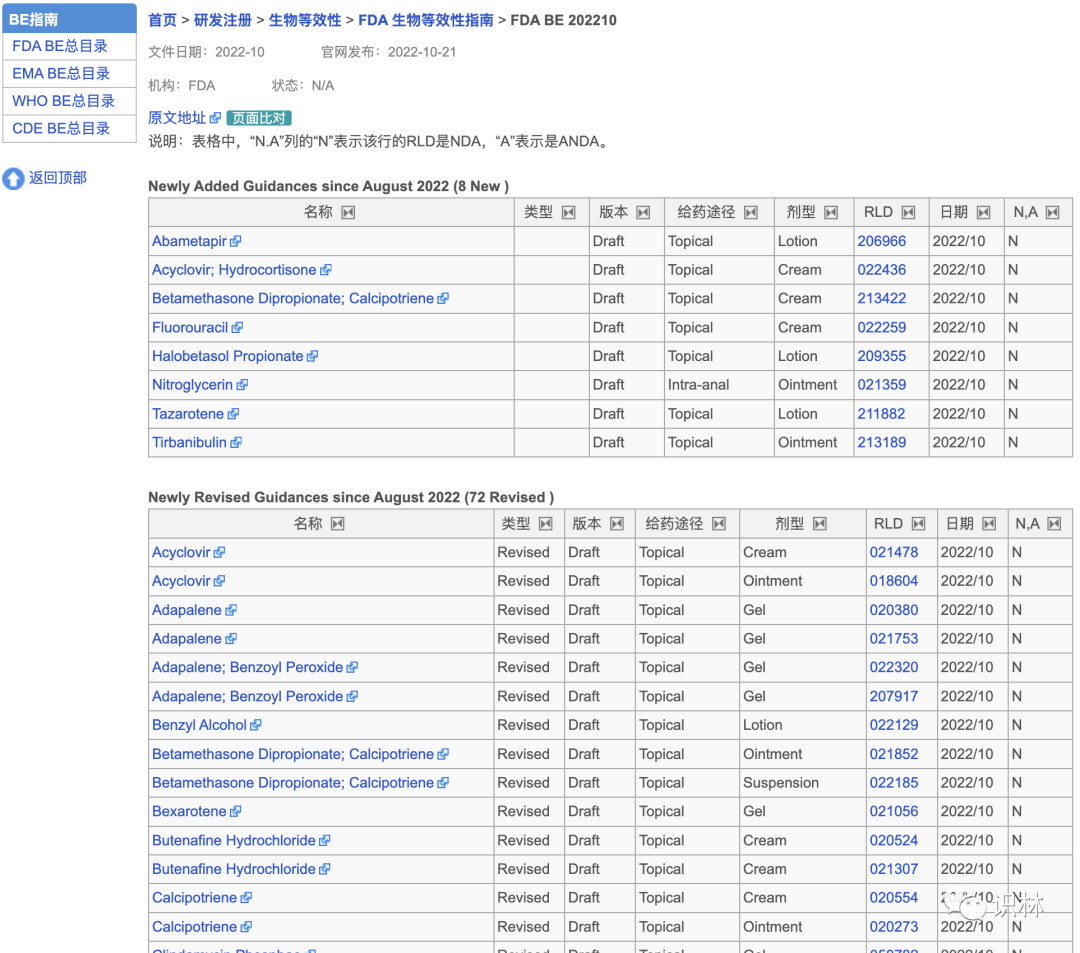
登陆识林BE指南数据库,阅览来自FDA/EMA/WHO/和CDE的全部具体产品指南。
10.21【FDA】指南草案 ANDA 提交的局部药品的物理化学和结构(Q3)表征
10.21【FDA】指南草案 ANDA 提交的局部药品的体外释放试验研究
10.21【FDA】指南草案 ANDA 提交的局部药品的体外渗透试验研究
10.21【FDA】指南草案 外用皮肤皮质类固醇:体内生物等效性
10.21【FDA】即将发布的复杂仿制药研发特定产品指南
10.20【FDA】仿制药计划月度绩效活动报告(2022财年)更新
10.17【FDA】ANDA 类的 RS 对应的 RLD 列表
【注册、审评、审批】
10.20【PMDA】药品 PMDA 风险沟通 更新
10.20【PMDA】医疗器械 审评报告 新增 nodoca
10.20【PMDA】药物 修订注意事项 页面更新
10.19【EMA】CTIS 评估时间线 内容更新
10.19【FDA】SOPP 8212: 突破性疗法产品-认定和管理
10.19【FDA】FDA D.I.S.C.O. Burst 版: FDA 批准 Pedmark(硫代硫酸钠)降低1个月及以上儿童局部非转移性实体瘤患者与顺铂相关的耳毒性风险
10.17【FDA】FDA D.I.S.C.O. Burst 版: FDA 批准 Imfinzi(durvalumab)用于局部晚期或转移性胆道癌成人患者
10.14【EMA】寻求科学建议和方案协助申请人指南 内容更新
【创新研发与临床】
10.21【ICH】M11 协同的电子结构化临床试验方案(CeSHarP)
10.21【EMA】临床试验亮点 - 2022年10月
10.21【FDA】指南定稿 神经退行性疾病的人类基因治疗
10.17【FDA】指南定稿 急性髓细胞白血病:开发用于治疗的药品和生物制品
10.17【FDA】指南草案 肿瘤中组织未定性药品的研发
10.17【FDA】指南草案 癌症免疫治疗临床试验中免疫介导的不良反应的特征、收集和报告
10.17【FDA】FDA 局长 Robert M. Califf 在2022年 NORD 突破峰会上的讲话
10.17【FDA】授予19项与罕见疾病(包括ALS)相关的赠款和两份合同
【GxP与检查】
10.20【FDA】483 比利时 Catalent Belgium SA
10.19【FDA】483 美国 ImClone Systems, LLC
10.19【FDA】483 美国 Compound Preferred LLC
10.19【FDA】483 美国 Hikma Injectables USA Inc
10.18【FDA】警告信 美国 American Cleaning Solutions
10.18【FDA】警告信 中国 北京兴谷绿伞科技有限公司
10.18【FDA】警告信 美国 Forcemech International LLC
10.18【FDA】进口禁令 55-03 更新中国 Chongqing Baijie Changhong Casing Co., Ltd 、四川雄健实业有限公司和郑州元隆化工产品有限公司
10.18【FDA】进口禁令 66-79 新增巴西 Unibeleza Industria E Comercio De Cosmeticos Ltda
10.17【FDA】进口禁令 99-32 新增中国 汕头市橄榄枝生物科技有限公司
10.17【FDA】483 印度 Torrent Pharmaceuticals Limited
【药典相关】
10.21【EDQM】“未来的 CEP”:第二次项目更新
10.21【EDQM】未来的 CEP 项目
10.21【EDQM】CEP 持有人受邀对欧洲药典34.4发表的各论草案进行评议
10.20【EDQM】EDQM 变更关于多晶型化学申请的 CEP 政策
【监管综合】
10.21【MHRA】在发现两批 Targocid 200mg被污染后,敦促患者检查包装
10.21【FDA】FDA 综述:2022年10月21日
10.20【FDA】COVID-19 药品和非疫苗生物制品紧急使用授权 页面更新
10.20【FDA】COVID-19 疫苗紧急使用授权 页面更新
10.18【FDA】FDA 综述:2022年10月18日
10.14【EMA】2022年年中报告
【医疗器械】
10.20【FDA】指南草案 选择突破性设备计划指南的更新:减少健康和医疗保健方面的差距
10.17【FDA】CDRH 2023财年拟议指南
点击下方卡片,快速绑定/注册识林小程序
长按下方二维码下载识林®App

识林®版权所有,未经许可不得转载



 个人中心
个人中心
 我是园区
我是园区




