您还不是认证园区!
赶快前去认证园区吧!

国家药品监督管理局官网截图 ▲
关于“微识医疗”
微识医疗是一家人工智能(AI)医学影像软件公司,旨在使用少量开发样本实现AI临床价值,为医用光学影像领域提供改写临床指南级别的数字医疗创新。
坚持自主研发
“成都高新造”三类创新医疗器械获批上市
EndoScreener®是一款用于在结肠镜检查视频流中实时检测并提示病灶,进而辅助医生发现癌前病变的智能辅助检测(CADe)软件。
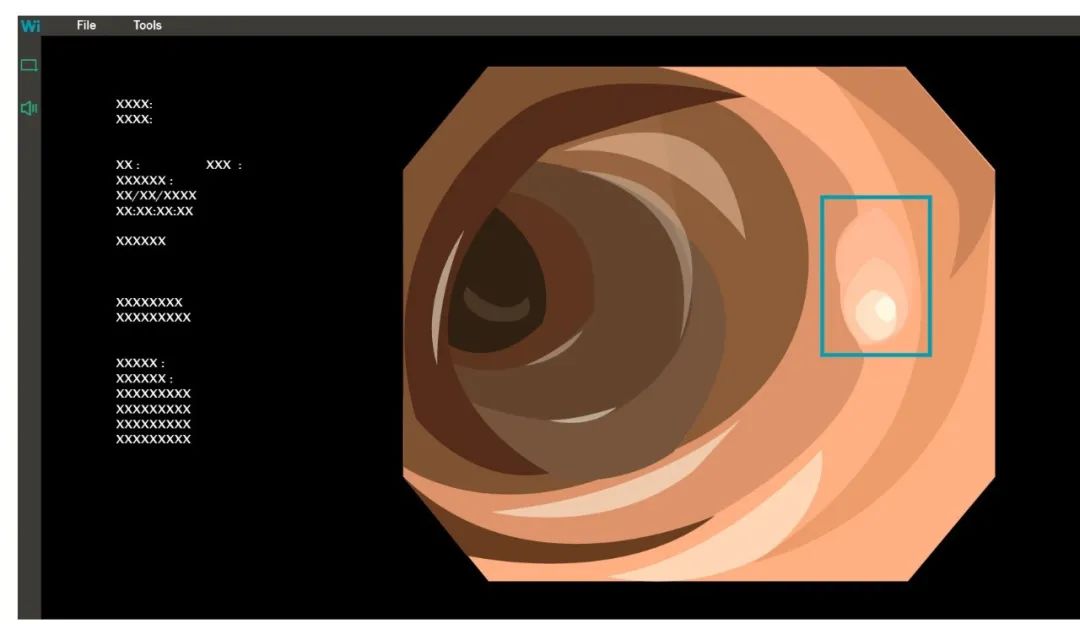
EndoScreener示意图 ▲
EndoScreener®
该产品为国内首个利用深度学习技术对内窥镜图像中息肉进行辅助检测的医疗器械软件,采用了小样本深度学习技术和局部标记技术进行算法模型框架的选择和开发,能够在较小样本下实现高性能、强泛化性和鲁棒性。
该产品与电子结肠内窥镜配合使用,可帮助医生在进行结肠镜检查时找出疑似息肉位置,有利于更早发现直肠癌的癌前病变,从而降低直肠癌发生率和死亡率。
作为国内首个获批的消化内镜AI辅助诊断产品,此次EndoScreener®的获批,实现了四川省内的三类国家创新医疗器械上市从0到1的突破,也是国家药监局批准的全国首个实时动态AI软件三类证。

此外,该产品在获国家药监局批准上市后,也成为了全球首个同时拥有中国国家药监局(2022年8月)、美国FDA(2021年11月)和欧盟CE-MDR(2021年11月)三重认证的消化内镜医疗AI产品。
获益于创新医疗器械绿色通道的鼓励政策,EndoScreener®在中国注册获批过程中节约了大量的时间和成本。作为企业,我们也必将用高性价比的产品和服务来回馈社会。
——微识医疗CEO刘敬家
加快生物医药与人工智能协同创新发展
成都高新区药械创新成果显著


成都前沿医学中心一期
在政策的助推下,成都高新区生物医药产业创新平台和重磅品种也取得突破进展:





 个人中心
个人中心
 我是园区
我是园区




