12月7日,Revolution Medicines宣布,赛诺菲方面已发出通知,将终止双方从2018年开始价值5亿美元的SHP2抑制剂的开发和商业化合作。而协议终止后,Revolution Medicines将重新获得赛诺菲根据协议获得的所有全球权利,包括关于研发的决策权,以及RMC-4630的所有商业收益权。

据悉,赛诺菲的发言人声称,终止其与RM公司的商业伙伴关系的决定是在“最近的投资组合审查和优先排序”之后做出的。
受到这一消息影响,Revolution Medicines公司的股价短时间出现一波近14%的大幅跳水,随后才逐渐反弹。而赛诺菲方面的股价也有所波动,在7日和8日接连小幅下滑。
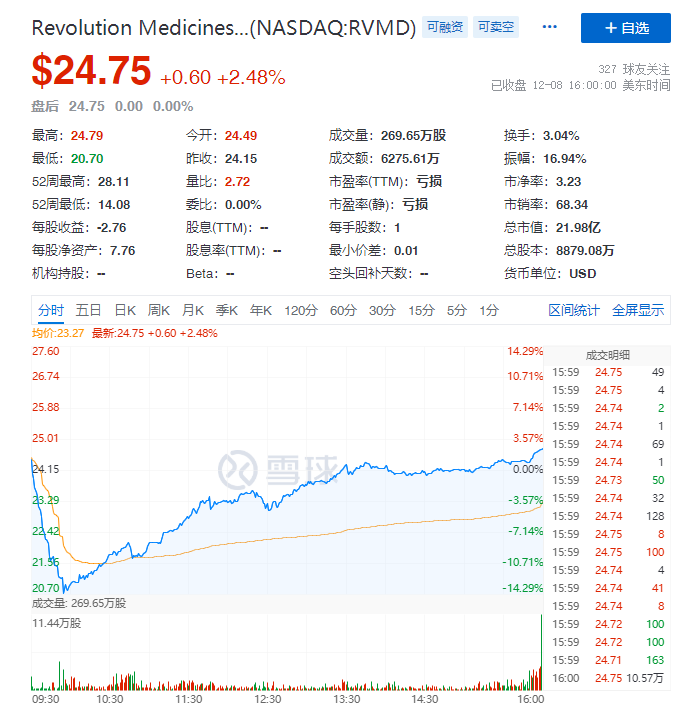
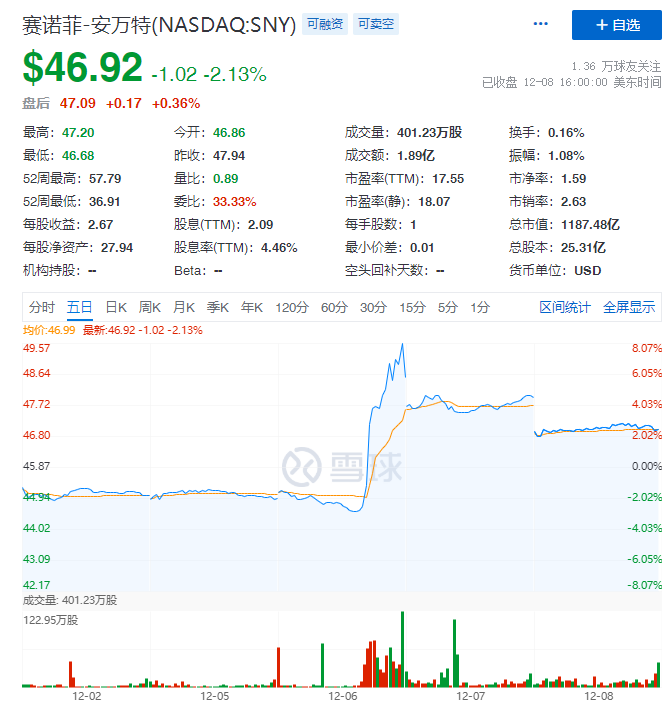
这样一看,市场方面似乎更肯定了赛诺菲方面的说法,是因为战略布局而做出了取舍。那么从现有事实来看,赛诺菲方面的说法可信吗?这可以先从赛诺菲对RMC-4630的临床开发来看以及SHP2靶点的作用机理来看。
SHP2靶点的作用机理与临床开发方式
作为一种非受体蛋白酪氨酸磷酸酶,SHP2在受生长因子、细胞因子和整合素受体调节的细胞信号转导下游发挥重要作用,并参与包括细胞存活、增殖和迁移在内的细胞过程。
首先,越来越多的证据表明,SHP2参与了癌细胞中的许多信号级联,包括RAS-MAPK、PI3K-AKT和JAK-STAT通路。对于PD1-PDL1通路的影响也在研究中。
其次,Th1免疫能力的恢复和T细胞的激活也依赖于SHP2的抑制,Th1免疫能力的恢复和T细胞的激活能够激活肿瘤微环境内的免疫反应。
再次,通过对SHP2的药理抑制可以增强CD8+ 细胞毒性T细胞介导的抗肿瘤免疫来降低肿瘤负担。
最后,SHP2的过度激活突变已在努南综合征和各种类型的癌症中被发现,包括白血病、非小细胞肺癌(NSCLC)、胃食管癌和乳腺癌。因此,SHP2被认为是癌症治疗的潜在治疗靶点。
尽管如此,SHP2这一靶点最初被认为是难以成药的,最初的几项靶向药物(如PTP结合位点的传统抑制剂,如PHPS1、GS-493和NSC-87877)普遍存在细胞渗透性低和生物利用度差的问题。,但后来通过蛋白变构和高通量筛选得到的SHP2变构抑制剂通过变构机制稳定了自抑制构象,更重要的是,变构抑制剂和其他激酶抑制剂的联合应用可以协同降低耐药的可能性。
而目前,临床上较为前列的SHP2抑制剂包括诺华的TNO155、RMC-4630、加科思的JAB-3068和JAB-3312。其中JAB-3068已获得孤儿药认证。这些药物许多都采用了联合治疗的策略。
以RMC-4630的临床开发策略为例,RMC-4630由于其在RAS-MAPK通路上的作用,因此可以与Amgen全球首个上市的KRAS G12C抑制剂Sotorasib(AMG510),以及另外一款KRAS G12C抑制剂Adagrasib联用。
与Sotorasi初步的临床结果则表明疗效限制,且安全可控:
在纳入的11例非小细胞肺癌患者中:3例(27%)有确认部分缓解;7例(64%)疾病控制(部分缓解+疾病稳定)。在接受最高剂量RMC-4630联合治疗的4例未经KRAS靶向治疗的非小细胞肺癌患者中:3例(75%)确认部分缓解,其中2例仍在持续缓解,4例(100%)疾病控制。有1例患者在既往索托雷赛治疗后疾病进展,在联合RMC-4630治疗5.5个月后肿瘤缩小超30%,治疗6.9个月时疾病进展。安全性方面,没有任何患者出现≥4级治疗相关不良事件。
还有文献表明,MEK抑制剂似乎是SHP2抑制剂的“好伙伴”,在动物体内,SHP2抑制剂在KRAS突变的NSCLC同样可以导致肿瘤细胞衰老效应,这种效应能够被MEK抑制剂增强。因此RMC-4630能够与罗氏的MEK抑制剂Cobimetinib联用。
而除此之外,RMC-4630还与LY3214996(ERK抑制剂),Osimertinib(第三代EGFR抑制剂),K药(PD-1抑制剂)等诸多药物展开临床应用。
从合作内容和临床试验的举办者来看,这些广泛展开的临床主要由赛诺菲推动,但这样一看,临床开展的是不是太多了?毕竟许多临床研究也只是联合用药的探索……
推测
笔者推测,如果以赛诺菲的角度来看,虽说Sotorasib与RMC-4630的联用展现出了较好的初步效果,但从另外一个方面来看,拓展临床太多也可能造成太高花费。
如果将5亿美元与如此多的临床项目相比,这样做似乎让赛诺菲本身承担了太多风险,而赛诺菲将这个“球”扔还给了RM。
毕竟再怎么说,赛诺菲的肿瘤业务也不是主营业务。
参考来源:
OA03.03 Sotorasib in Combination with RMC-4630, a SHP2 Inhibitor, in KRAS p.G12C-Mutated NSCLC and Other Solid Tumors
Song Z, Wang M, Ge Y, Chen XP, Xu Z, Sun Y, Xiong XF. Tyrosine phosphatase SHP2 inhibitors in tumor-targeted therapies. Acta Pharm Sin B. 2021 Jan;11(1):13-29. doi: 10.1016/j.apsb.2020.07.010. Epub 2020 Jul 26. PMID: 33532178; PMCID: PMC7838030.
Mainardi, S., Mulero-Sánchez, A., Prahallad, A. et al. SHP2 is required for growth of KRAS-mutant non-small-cell lung cancer in vivo. Nat Med 24, 961–967 (2018). https://doi.org/10.1038/s41591-018-0023-9




 个人中心
个人中心
 我是园区
我是园区





