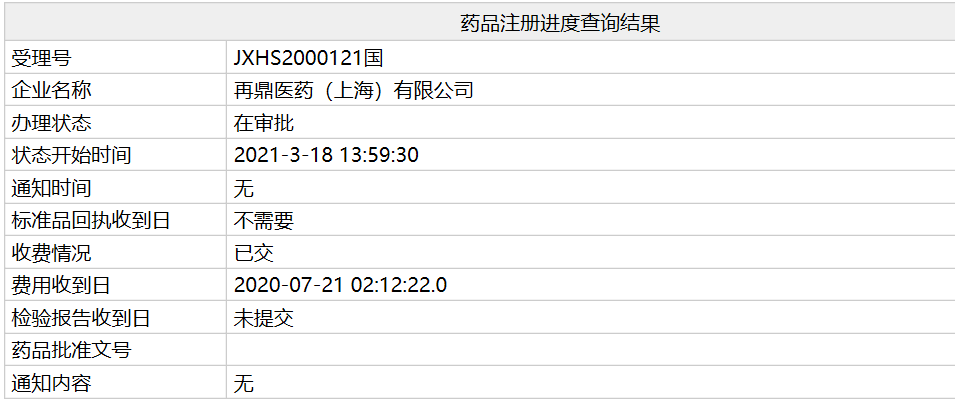
3月19日,国家药监局官网显示,再鼎医药瑞派替尼片上市申请(受理号:JXHS2000121) 已处于“在审批”阶段,有望于近期获得NMPA批准上市,用于治疗已接受过包括伊马替尼在内的3种或更多种激酶抑制剂治疗的晚期胃肠道间质瘤(GIST)成人患者。
瑞普替尼(Ripretinib)是一种酪氨酸激酶开关控制抑制剂,通过使用独特的双重作用机制来调节激酶开关和激活环,从而广泛抑制KIT和PDGFRα突变激酶。Ripretinib抑制参与GIST的外显子9、11、13、14、17和18中的起始和继发性KIT突变,以及参与SM的主要外显子17 D816V突变。Ripretinib还抑制GIST子集有关的外显子12、14和18中的主要PDGFRα突变,包括外显子18 D842V突变。
瑞派替尼由Deciphera开发,2019年6月,再鼎医药与Deciphera签订了独家许可协议,获得了ripretinib在大中华区(中国大陆、香港、澳门和台湾)开发和商业化的权利。
一项代号为INVICTUS的III期随机、双盲、安慰剂对照国际多中心临床研究评估了瑞派替尼与安慰剂对比在129例晚期GIST患者中的安全性、耐受性和有效性,患者此前已接受过包括伊马替尼、舒尼替尼和瑞戈非尼的治疗。患者按2:1的比例随机分配至每日150mg瑞派替尼组或安慰剂组。
研究结果显示,瑞派替尼尼组患者中位无进展生存期为6.3个月,而安慰剂组仅为1.0个月,达到了主要终点,并且患者疾病进展或死亡的风险显著降低了85%(危险比0.15,p <0.0001)。
同时研究也达到了客观缓解率(ORR)和总生存期(OS)的次要终点。瑞派替尼组的客观缓解率为9.4%,而安慰剂组为0%(p=0.0504)。瑞派替尼组中位总生存期为15.1个月,而安慰剂组为6.6个月,并且死亡风险降低了64%(危险比为0.36)。
安全性方面,最常见的不良反应(≥20%)为脱发、乏力、恶心、腹痛、便秘、肌肉疼痛、腹泻、食欲不振、掌跖红肿综合征和呕吐。8%的患者发生了导致永久停药的不良反应,24%的患者由于不良反应引起剂量中断,7%的给药患者由于不良反应引起剂量减少。





 个人中心
个人中心
 我是园区
我是园区




