从首个CD73药物进入临床阶段至今,7年过去,积累了一大堆有参考意义的临床数据,而它也将成为后PD(L)1时代不可或缺的组成部分。

对于早期临床数据的判断,犹如管中窥豹,是十分困难的,不像2/3期临床试验一样,适应症明确,患者数量也足够,看完安全性与有效性指标后,还是可以让药企与投资者得到较为值得信服的判断。
对于FIC靶点,在泛瘤种、不同药物组合的早期临床试验里,更多的是发现积极信号和异常信号,如对什么样的瘤种有阳性结果,出现了什么样的异常不良反应等,如同计算机里的“0”或“1”,不太需要达到统计学上的差异,要达到统计学上的差异,这是后面样本量足够大的后期临床试验的事了。
所以本文主要根据“0”或“1”的原则,总结CD73靶点药物起效的瘤种与不良反应事件谱。有的试验里包括非CD73药物的组别,暂不纳入统计。

▌DLT
2021 ASCO GI上,在ARC-8(NCT04104672)试验里,吉利德研究quemliclustat联合PD-1单抗zimberelimab与化疗治疗1L mPDAC,50mpk组里出现1例2级自身免疫性肝炎,给与相应药物处理后能完全恢复,接着参与试验。
▌因AE中止治疗
2018 AACR上,在(NCT02754141)试验里,BMS研究BMS-986179±O药治疗晚期实体瘤,1例由于3级ALT升高而中止治疗。
▌因AE导致死亡
2021 ASCO上,在(NCT02503774)试验里,阿斯利康研究oleclumab±I药治疗CRC/PDAC/EGFRm NSCLC,1例由于全身炎症反应综合征而导致死亡。
▌AE谱
下图橙色的是仅在CD73单药中出现的,未出现在其他联用药物的最常见AE里(≥10%),如寒战与注射相关反应。寒战发生在mupadolima和quemliclustat药物里,大多为1~2级,单药(mupadolima)发生率最高为45.8%(11/24),mupadolima联合A2aR拮抗剂ciforadenant的发生率最高为18.8%(3/16),quemliclustat联合PD-1单抗联合zimberelimab+标准化疗的发生率为21%(4/21)。
注射相关反应发生在mupadolimab和uliledlimab里,单药(mupadolima)发生率最高为16.7%(2/12);uliledlimab联合T药的发生率为65%(13/20),主要发生在第一针注射时,并得到很好的处理。
下图黄色的为单药与联合其他药物均出现的AE,但都为1~2级AE,如恶心、呕吐、疲劳、头痛和瘙痒,其中3级及以上疲劳未出现在单药里。
下图的蓝色部分更多的是联合的其他药物的常见AE,尚不能表明是CD73药物造成的,如淋巴球减少症、中性粒细胞减少症、血小板减少症、AST/ALT/ALP升高、肌酐升高、腹泻、食欲下降、便秘、口腔炎、发热、脱发、皮疹、皮肤干燥、肺炎、贫血、低钠血症、低白蛋白血症、关节痛、肌痛、呼吸困难。
下图的灰色部分为小样本事件,且并非涉及联合药物的常见AE,不能判断是否与研究药物(包括联用)有关,如肺栓塞、带状疱疹、发热性中性粒细胞减少症。
下图的白色部分,并非涉及联合药物的常见AE,但也不能判断是否与CD73药物有关,如白细胞计数减少、结肠炎、血管性水肿、不适感、甲沟炎、高血压、视力模糊、甲亢、癌痛。
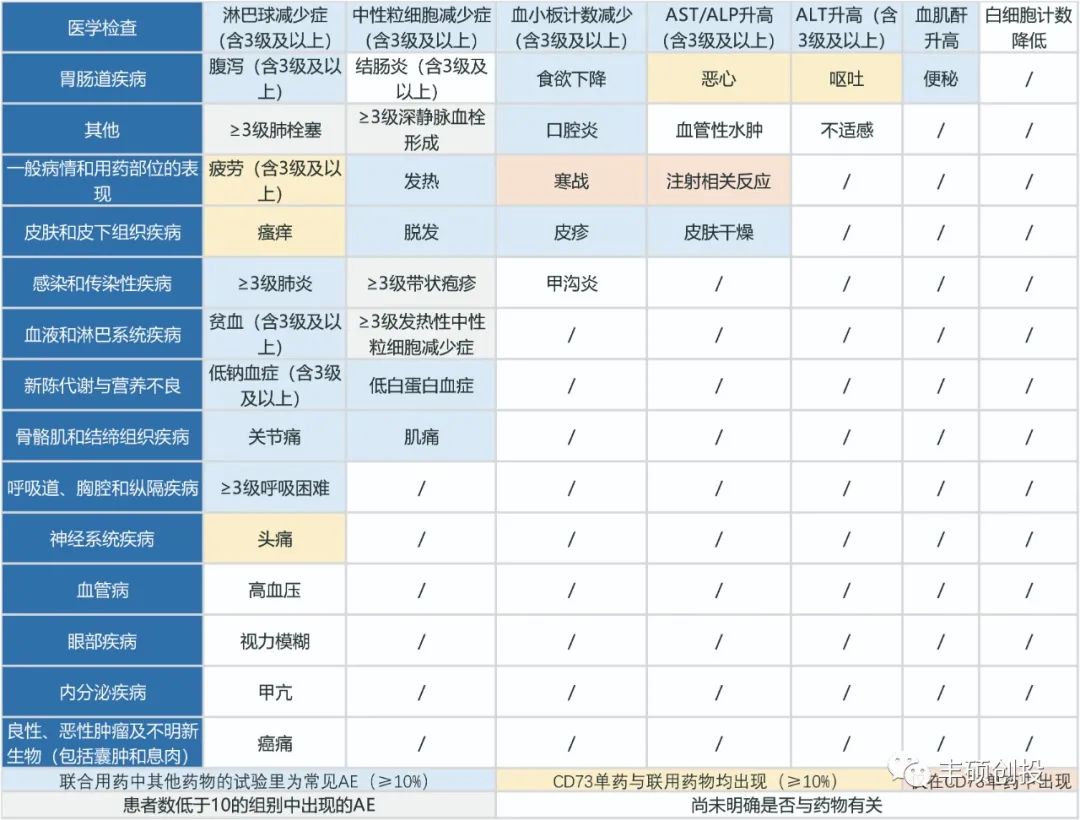
图1 CD73药物现有临床数据的AE总谱(丰硕创投整理)
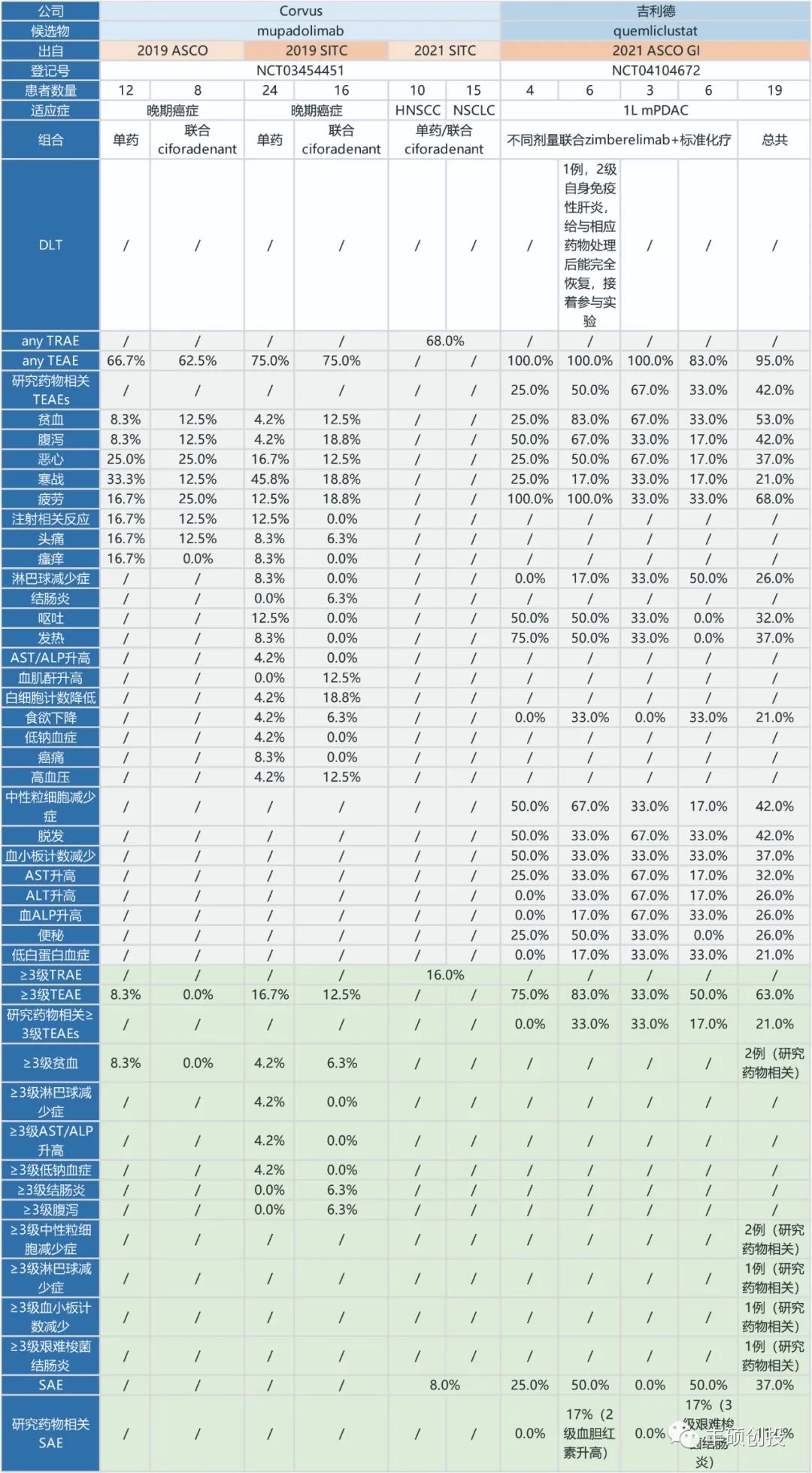
图2 CD73药物现有临床数据的AE谱1(丰硕创投整理)
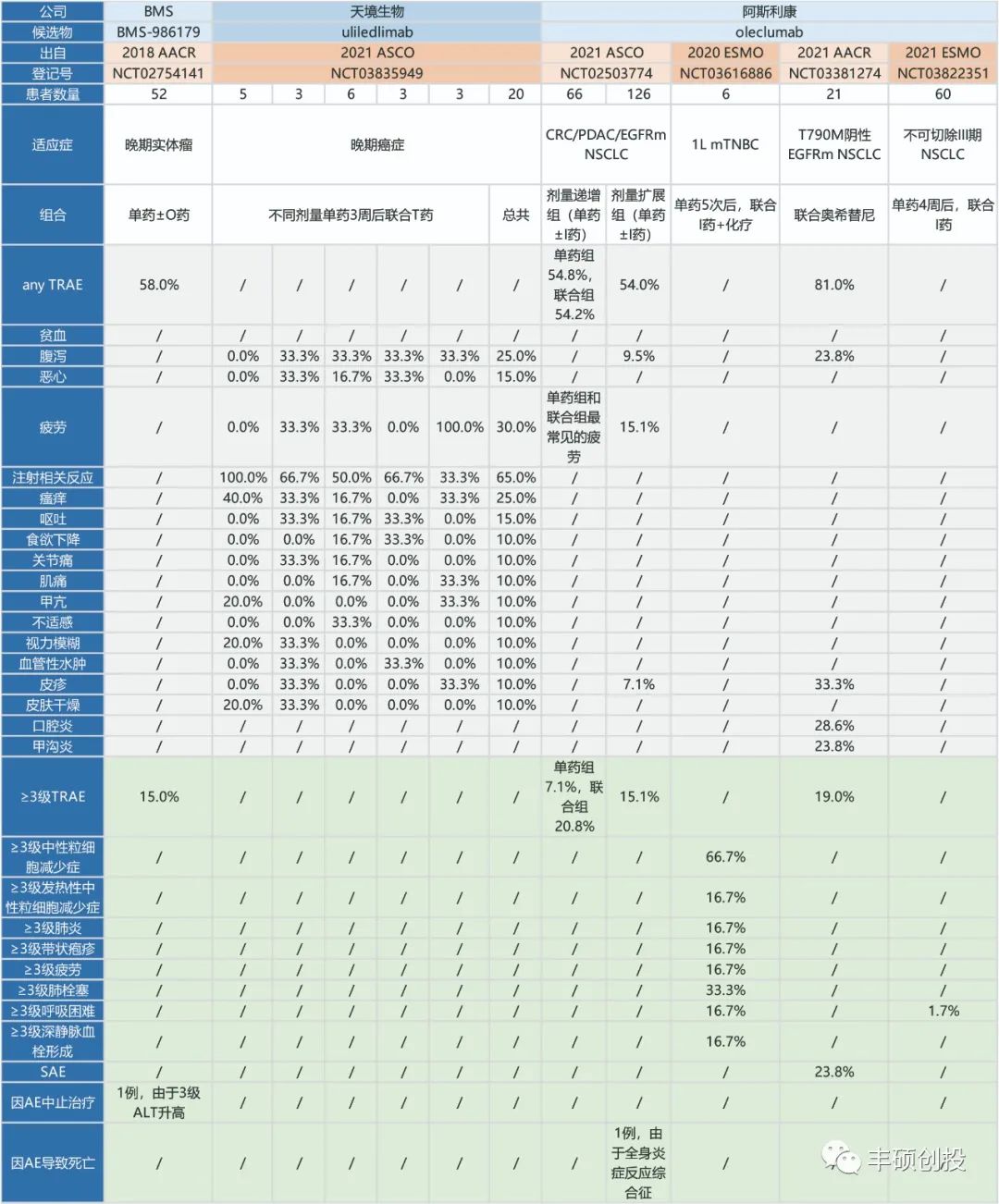
图3 CD73药物现有临床数据的AE谱2(丰硕创投整理)


▌3项结果
2021 ASCO GI上,吉利德公布了ARC-8(NCT04104672)试验结果,研究quemliclustat联合PD-1单抗zimberelimab和标准化疗治疗1L mPDAC,在17例可评估患者中,PR达到41%,现有标准化疗NP/Gem的ORR为23-29%。添加CD73药物后,在胰腺癌里能额外增强缩瘤效果。
2021 AACR上,阿斯利康公布了(NCT03381274)试验结果,研究oleclumab联合奥希替尼治疗T790M阴性EGFRm NSCLC,21例患者中,4例PR(19%),13例SD(61.9%),3例PD,1例未评估,DCR 81%,mPFS为11个月,6个月PFS率为63.5%,9个月PFS率为52.9%,mOS未达到(11.7-未评估),6个月OS率为100%,9个月OS率为90%。
与既往奥希替尼单药治疗这类人群中,它们两者的ORR相似(21% vs 19%),但联合组的mPFS更长(11.0 vs 2.8个月)。添加CD73药物后,能够延缓T790M阴性EGFRm NSCLC的进展时间。
2021 ESMO上,阿斯利康公布了COAST(NCT03822351)试验结果,研究了oleclumab单药4周后,联合I药治疗不可切除III期NSCLC,I药组(n=67)与I药+oleclumab组(n=60)的未确认ORR分别为25.4%和38.3%,16周DCR分别为58.2%和81.7%,mDOR分别为NR(2.3,NA)和12.9(6.7,NA),10个月PFS率分别为39.2%和64.8%。添加CD73药物后,能够增强III期NSCLC的缩瘤效果,并延缓进展时间。
▌3项启示
2021 ASCO上,天境生物公布了(NCT03835949)试验结果,研究uliledlimab单药3周后,联用T药治疗晚期实体瘤,在生物标志物分析上,临床缓解与PD-L1和CD73的表达情况有关,与A2AR的表达情况无关。
2021 ASCO上,阿斯利康公布了(NCT02503774)试验结果,研究oleclumab±I药治疗CRC/PDAC/EGFRm NSCLC,瘤体CD73的表达情况与临床缓解有关。
2020 WCLC上,阿斯利康公布了HUDSON(NCT03334617)试验结果,研究oleclumab联合I药治疗既往接受过化疗和PD(L)1治疗的NSCLC,根据生物标志物和耐药情况分为3组,队列A生物标志物匹配组(CD73H突变),队列B生物标志物不匹配组,队列细分为PD(L)1原发性耐药和获得性耐药。结果只在队列B的获得性耐药组中出现缓解。
小结:临床缓解情况与CD73和PD-L1的表达情况有关,但与CD73H的突变及A2AR的表达情况关系不大。
从下图看到,CD73药物目前披露能够获益的瘤种包括非小细胞肺癌、三阴性乳腺癌、结直肠癌、皮肤癌、前列腺癌、宫颈癌、胰腺癌、肾癌、卵巢癌、头颈癌、肛门癌和肉瘤。
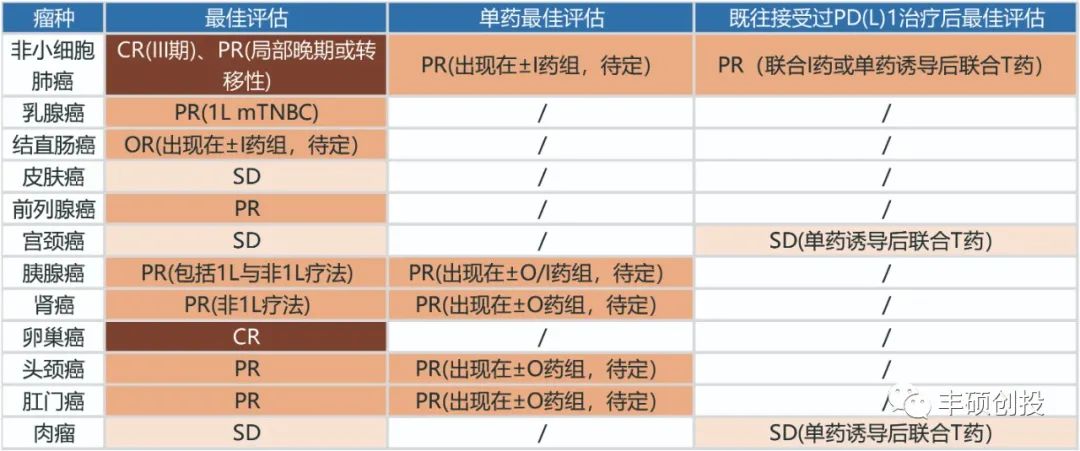
图4 CD73药物现有临床数据的有效性1(丰硕创投整理)
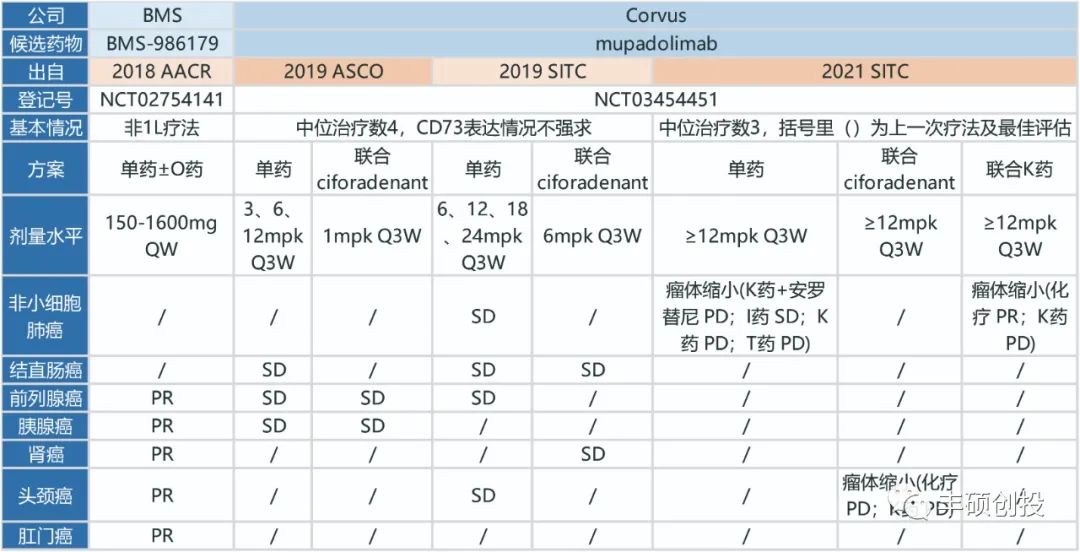
图5 CD73药物现有临床数据的有效性2(丰硕创投整理)
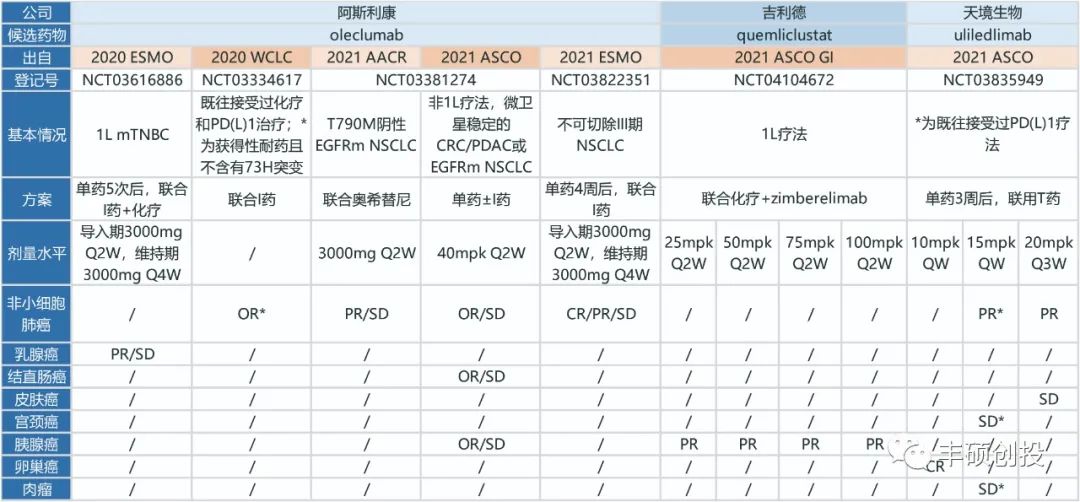
图6 CD73药物现有临床数据的有效性3(丰硕创投整理)





 个人中心
个人中心
 我是园区
我是园区




