艾滋病超长效鸡尾酒已是一种趋势,吉利德的超长效抗艾滋病新药喜获FDA批准
收藏
关键词:
吉利德新药FDA药FDA批准
资讯来源:药事纵横 + 订阅账号
发布时间:
2022-12-26
12月22日,FDA批准了吉利德的超长效衣壳蛋白抑制剂Lenacapavir,在联合其它抗逆转录药物的基础上,用于治疗高度耐药的HIV-1感染患者,包括现有的治疗方案因耐药治疗失败、不耐受或因安全性考虑而无法使用现有治疗方案治疗的患者。在此之前,EMA已经在8月份批准了该产品。
本品是一种全新机制的抗艾滋病药物,特点是半衰期长,口服给药的半衰期长达10-12天,而大剂量注射剂的半衰期长达8-12周,故只需半年注射一次。虽然是超大剂量的注射剂,但本品不同于以往的注射混悬液,而是一种含聚乙二醇300的澄清溶液,由于本品几乎不溶于水,在聚乙二醇的作用下溶解,注射到皮下后仍然有一个缓慢吸收的过程。由于注射剂释放较慢,注射后数天内血药浓度较低,口服制剂配合使用以快速提高血药浓度,以达到快速起效的作用。
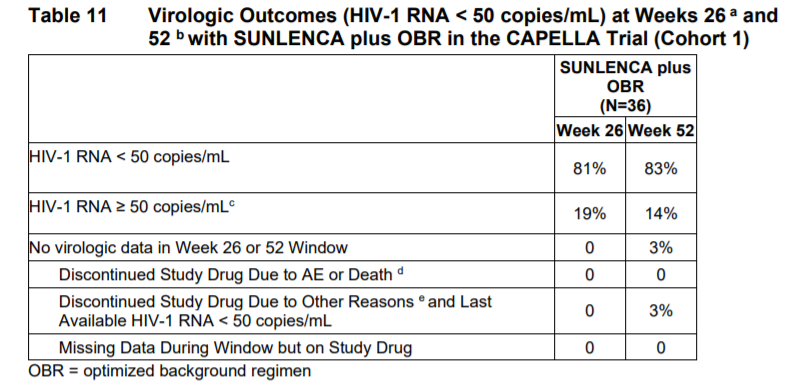
本品的安全有效性,在一项为期52周,安慰剂对照,随机双盲的多中心临床试验中得到了初步的确认。72名既往经历过多种治疗方案治疗失败,且体内病毒载量≥ 400拷贝/ml的患者加入了临床试验。该试验分为两个队列,36名患者入组后进入了队列一(随机组),进入该队列的患者皆为在随访中病毒载量下降量小于0.5 log10拷贝/ml的患者,队列二为非随机组,在随访中病毒载量下降量大于等于0.5 log10拷贝/ml或超过队列一规划样本数量的患者被纳入该队列。队列一的患者入组胡,先按2:1的比例随机接受本品或安慰剂进行为期14天的功能性治疗,在结束功能性治疗后再接受最佳治疗方案+本品联合治疗。主要治疗终点为在功能性治疗期间,体内病毒载量下降大于等于0.5 log10拷贝/ml的患者比例。结果显示,本品治疗组有87.5%的患者达到了治疗终点,而安慰剂组仅为16.5%。在随后的长期治疗中,26周和52周体内病毒载量低于50拷贝/ml的患者比例分别为81%和83%。队列二的患者则入组后直接接受最佳治疗方案+本品联合治疗,26周和52周体内病毒载量低于50拷贝/ml的患者比例分别为81%和72%。
本品的获批具有里程碑的意义,为耐药患者带来新的希望的同时,也大幅改善患者的依从性。因为艾滋病治疗是长期用药,方案的便捷性非常关键,从每日口服2-3次到每日口服一次,再到数月注射一次。GSK和强生联合开发的Cabenuva(cabotegravir/利匹韦林)开启了超长效治疗方案的的先河,cabotegravir+利匹韦林是最早的超长效鸡尾酒疗法,属于纳米晶制剂,最早于2020年获得加拿大药监局批准,最大给药周期是每两个月一次,但该产品在2021年在美国获批时,仅批准了一个月一次的方案。本品的获批将又是长效艾滋病药物史上的巨大跨越,然而虽然可以六个月一次给药,但本品并非全方案鸡尾酒,需要联合其它口服药物一同使用。
不难想象的是,未来的几年里,艾滋病治疗将进入一个超长效竞赛的时代。EvaluatePharma预测GSK的cabotegravir超长效注射剂在2028年的销售额可达,而本品在2026年的销售额将达8.77亿美元,2028年的销售额将达16.02亿美元。
除了单药疗法,吉利德为了充分利用本品的价值,也在积极开发鸡尾酒疗法,本品与默沙东的非核苷类逆转录酶抑制剂islatravir的联合用药方案已经处于2期临床开发阶段,该方案有望成为首个每周一次的口服鸡尾酒疗法。与整合酶抑制剂bictegravir和非核苷类逆转录酶抑制剂 GS-5894的联合用药方案也已经处于1期临床研究阶段。
各位朋友好,觉得本文对您有帮助,请随手点一下下方的在看,以便让你的朋友也能看到哦。

 药选址
药选址

