
辉瑞(Pfizer)近日公布了etrasimod一项3期研究ELEVATE 12(NCT03996369)的阳性顶线结果。etrasimod是一款在研的口服、每日一次、选择性鞘氨醇1-磷酸(S1P) 受体调节剂,正被开发用于治疗中度至重度活动性溃疡性结肠炎(UC)。
ELEVATE 12是一项全球性、多中心、随机、双盲、安慰剂对照3期研究,共入组了354例先前至少接受过一种常规、生物或JAK疗法但治疗失败或不耐受的中度至重度活动性UC患者。研究中,这些患者被随机分配,接受每日一次口服2mg剂量etrasimod或安慰剂作为诱导疗法治疗12周。
数据显示,该研究达到了主要终点:与安慰剂组相比,etrasimod组患者在第12周临床缓解率方面有统计学意义的显著改善。此外,全部关键次要终点也具有统计学意义的显著改善。该研究中的安全性概况与之前的2期研究一致。
该研究的结果将在未来的科学出版物上公布。这些数据以及另一项52周3期研究ELEVATE 52(NCT03945188)的结果预计将构成未来计划监管备案的基础。后一项研究的结果将在第一季度末公布。
辉瑞全球产品开发部炎症与免疫学首席开发官Michael Corbo表示:“这些阳性结果表明,如果获得批准,etrasimod对于接受当前疗法病情无法改善的溃疡性结肠炎患者而言可能是一个潜在突破性选择。我们继续致力于开发新的疗法来治疗免疫炎症性疾病,并解决UC患者对常规或先进疗法应答不足、失应答或不耐受的口服治疗需求。”
溃疡性结肠炎(UC)是一种影响大肠的慢性疾病。大肠黏膜的慢性炎症和表面溃疡造成排便频繁、腹泻和大便带血等症状。炎症通常发生在直肠,或可累及全部或部分结肠。现有治疗方案在副作用、耐受性、疗效和给药途径方面具有局限性。
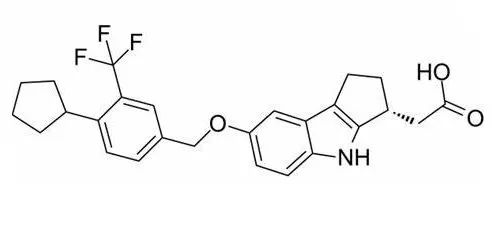
etrasimod化学结构式(图片来源:medchemexpress.com)
etrasimod是一种新一代、口服、高选择性鞘氨醇1-磷酸(S1P)受体调节剂,具有同类更优的潜力。基于现有的研究数据及其选择性地与S1P受体1、4和5结合的特点,与现有同类药物相比,etrasimod可能具有更好的安全性与有效性。
etrasimod由Arena制药公司开发,该公司最近被辉瑞收购。2017年12月,云顶新耀(Everest Medicines)与Arena达成合作伙伴关系,获得了etrasimod在大中华区和韩国的商业化权益。
在Arena针对中度至重度UC患者开展的随机、双盲2期OASIS临床试验中,etrasimod达到预定的疗效终点,并且耐受性良好。云顶新耀目前正在开展针对UC的3期临床试验,以期该药物能够在其业务领域内获得治疗中度至重度UC患者的上市批准。etrasimod也具有治疗其他自身免疫性适应症的潜力,包括克罗恩病(CD) 与特应性皮炎(AD)等。
原文出处:Pfizer Announces Positive Top-Line Results for Phase 3 Trial of Etrasimod in Ulcerative Colitis Patients



 个人中心
个人中心
 我是园区
我是园区




