据世卫组织相关报告,目前全世界至少有8.5亿人因各种原因导致肾脏病,而且肾脏病已上升为全球十大死因之一,预计2040年慢性肾脏病将成为全球第5大致死病因。
目前,全球已多家企业开始布局肾脏疾病药物市场,而且出现了一些专注于肾脏疾病药物研发企业,如Vifor Pharma、Akebia Therapeutics、Chinook Therapeutics。为了加速肾脏疾病药物的研发,近年来这些企业达成数项交易。
2021年11月,Vifor Pharma和 Sanifit Therapeutics两家企业宣布双方已达成最终收购协议。据协议,Vifor Pharma 将收购 Sanifit Therapeutics 的全部已发行股份,获得后者SNF472 的全部全球权利,以增强公司的创新资产组合。SNF472是 Sanifit Therapeutics的主打产品,是一款新型血管钙化抑制剂,通过与正在生成或者已经存在的羟基磷灰石晶体结合,阻止晶体的生成和继续增长,从而防止心血管钙化的产生。2019年10月,Sanifit Therapeutics宣布SNF472治疗接受透析的终末期肾病(ESKD)患者的2b期临床试验达到主要终点:SNF472治疗组患者冠状动脉钙化水平较安慰剂组显著降低。今年2月,该药又被FDA授予治疗晚期肾脏疾病(ESKD)患者外周动脉疾病(PAD)的孤儿药资格。
2021年9月,Vifor Pharma 和 Travere Therapeutics达成合作开发和许可协议,获得Sparsentan在欧洲、澳大利亚和新西兰的独家商业化权利。Sparsentan是一种具有双重机制的内皮素/血管紧张素受体拮抗剂,临床前数据表明其通过阻断内皮素A和血管紧张素Ⅱ的1型通路,可减少蛋白尿,保护足细胞并防止肾小球硬化和系膜细胞增殖。今年8月,该药治疗IgA肾病(IgAN)的关键性3期临床试验PROTECT取得积极初步中期结果:在治疗36周后,sparsentan组蛋白尿与基线相比的降低幅度,是活性对照组的3倍以上(p<0.0001)。
2020年12月,大冢制药与Aurinia Pharma达成了一项合作及许可协议,在欧盟、日本、英国、俄罗斯、瑞士、挪威、白俄罗斯、冰岛、列支敦士登、乌克兰开发和商业化voclosporin治疗狼疮肾炎,该药是一款口服钙调神经磷酸酶抑制剂,2021年1月被FDA批准联合背景免疫抑制治疗方案,用于治疗活动性狼疮性肾炎(LN)成人患者。
2021年6月,Akebia Therapeutics与Cyclerion Therapeutics达成一项全球独占许可协议,获得后者口服sGC激动剂praliciguat在全球范围内的研究、开发和商业化权利。
2020年11月,Vifor Fresenius Medical Care Renal Pharma (VFMCRP,Vifor Pharma 和费森尤斯卡比成立的合资公司)与费森尤斯卡比(Fresenius Kabi)达成一项协议,将高钾血症药物Veltassa在中国市场的独家销售权授予费森尤斯卡比。Veltassa是一种无钠钾结合剂,作为一种粉状药物,通过与水混合经口服使用,批准用于治疗高钾血症。该药通过与钾离子结合以交换钙离子,主要是在结肠部位中起作用,然后钾通过正常的排泄过程从体内排出。
2020年10月,Vifor Pharma与Cara Therapeutics公司签署一份商业许可协议,获得后者Korsuva(difelikefalin)在美国的商业化权利。Korsuva的活性成分difelikefalin是一种首创外周κ阿片受体(KOR)激动剂,作用于人体外周神经系统和某些免疫细胞。今年8月,该药被FDA批准用于接受血液透析的患者,治疗慢性肾脏病相关的中度至重度瘙痒(CKD-aP),成为FDA批准的第一个治疗血液透析成人患者CKD-aP的药物。
2020年1月,Chinook Therapeutics与AbbVie达成许可协议,获得后者内皮素受体拮抗剂atrasentan在全球范围内的专有权。atrasentan是一种有效且选择性的ETA受体拮抗剂,在人类原发性肾小球疾病中被激活,可引起蛋白尿,肾脏炎症和瘢痕形成,从而导致进行性肾功能丧失。
2019年11月,Vifor Pharma 和 Evotec SE 宣布成立一家合资企业,专注于发现和开发新型肾病疗法。据协议,Vifor Pharma 将获得外部研发能力以开发自己的肾脏病管线,Evotec将通过合资企业将开发的所有肾脏病学资产授权给 Vifor Pharma 。同月,Vifor Pharma与强生达成合作,共同在美国商业化INVOKANA(canagliflozin),针对降低2型糖尿病(T2D)和糖尿病肾病(DKD)患者的心衰住院风险的适应症。
2019年6月,云顶新耀与Calliditas公司签订独家授权许可协议,获得在中国(包括香港、澳门、台湾地区)和新加坡开发和商业化Nefecon的专属权利。Nefecon是Calliditas Therapeutics公司开发的一款布地奈德的口服靶向释放制剂,被开发用于治疗原发性IgA肾病。
2019年5月,阿斯利康与BenevolentAI宣布达成长期研发合作协议,使用 AI 和机器学习技术,研发治疗慢性肾病(CKD)和特发性肺纤维化(IPF)的创新疗法。
2018年6月,Akebia Therapeutics和Keryx Biopharmaceuticals两家公司达成合并协议,创建一家专注于慢性肾病(CKD)研究的生物医药公司,合并后的公司将被命名为Akebia Therapeutics。
2018年5月,Cara Therapeutics将Korsuva(CR845/difelikefalin)注射剂的全球许可权(除美国,日本和韩国外)授予Vifor Pharma和费森尤斯卡比成立的合资公司 Vifor Fresenius Medical Care Renif Pharma(VFMCRP)。
2018年3月,Vifor Pharma 与 Zeria Pharmaceuticals达成授权许可,将Veltassa 在日本的开发和商业化权利授权给后者。
2017年12月,复星医药与Ardelyx公司达成授权协议,获得后者NHE3小分子抑制剂tenapanor在中国的开发和商业化权益。tenapanor是一款在胃肠道局部抑制钠/氢交换蛋白3(NHE3)的小分子。NHE3在小肠和结肠表面表达,主要负责吸收食物中的钠离子。2019年,该药被FDA批准用于治疗便秘肠应激综合征(IBS-C),今年7月该药用于控制慢性肾脏病(CKD)透析成人患者血清磷水平的新适应症申请遭FDA拒批。
2017年5月,Akebia与Vifor Pharma签订一项协议,授予Vifor独家授权,以销售vadadustat(经FDA批准)并纳入医疗保险和医疗补助(CMS)终末期肾脏疾病预期付款系统(ESRD PPS) 捆绑销售给Fresenius Medical Care North America的分支机构Fresenius Kidney Care Group,仅在美国的透析设施内使用。2019年4月,两家扩展该协议,以便该许可证在过渡药物附加协议中也将有效付款调整(TDAPA)两年期,预计在ESRD捆绑销售期之前,并为Vifor提供向美国某些第三方透析组织出售vadadustat的许可。
2016年9月,拜耳和德国生物技术公司Evotec达成一项为期五年、多靶点的研发合作,旨在开发治疗慢性肾脏疾病的候选药物。
此外,我国专注于肾脏病及其相关慢性疾病创新药物研发的礼邦医药经过三年发展已经建立起了丰富的肾脏病新药产品管线,适应症涵盖慢性肾病(CKD)/透析并发症、IgA肾病、糖尿病肾病和和常染色体显性多囊肾病等疾病。今年9月,礼邦医药完成5450万美元B+轮融资,而本轮融资资金将用于推进礼邦医药产品临床研究、生产基地建设、研发管线以及团队扩充。
而且,我国创新药一哥——恒瑞医药也开始掘金肾病领域,其开发的低氧诱导因子—脯氨酰羟化酶抑制剂(HIF-PHI)DDO-3055被开发用于治疗慢性肾病所致贫血(包括透析和非透), HR19042 被开发用于治疗原发性 IgA 肾病。
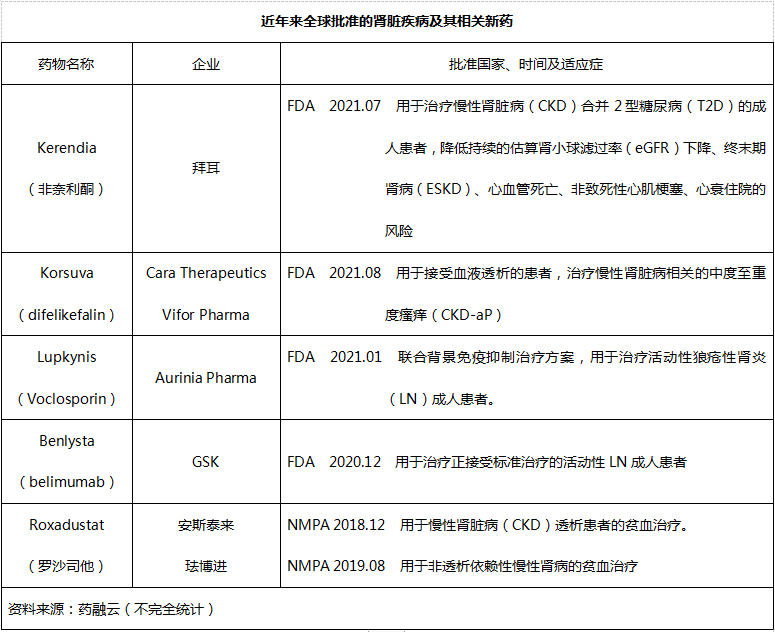
目前,企业的努力已经初见成效,近年来全球已经批准几款肾脏疾病及其相关药物,详见下表。而且,治疗2型糖尿病的药物SGLT2抑制剂Invokana(卡格列净)、Forxiga/Farxiga(达格列净)也被批准用于治疗糖尿病肾病。




 个人中心
个人中心
 我是园区
我是园区




