▎药明康德内容团队报道
中国国家药监局药品审评中心(CDE)最新公示显示,君境生物有两款1类新药获批临床,分别为EGFR-exon20抑制剂AP-L1898胶囊、以及XPO1抑制剂WJ01024片。公开资料显示,君境生物由君实生物与微境生物共同投资成立。2020年9月,君实生物与微境生物达成一项高达4.72亿元人民币的合作,在全球范围内共同开发、生产及商业化微境生物的4款在研抗肿瘤小分子药物,其中就包括本次获批临床的这两款在研药。
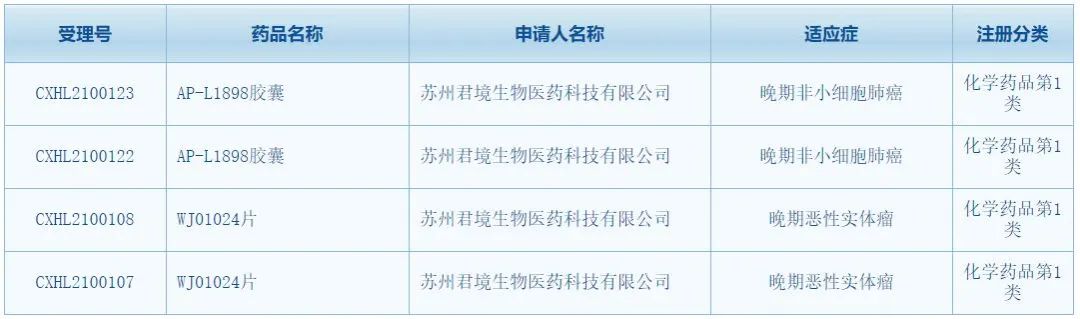
根据君实生物早前发布的公告,AP-L1898(项目代号“JS111”)是一种有效抑制EGFR(表皮生长因子受体)非常见突变的靶向小分子抑制剂。EGFR非常见突变占所有EGFR突变的比例约为10%,包括EGFR exon20插入、T790M原发点突变和复合突变以及以G719X为代表的位于外显子18-21之间的其他点突变和序列重复突变。对于携带EGFR exon 20插入等EGFR非常见突变的非小细胞肺癌患者,现有的EGFR-TKI、化疗和免疫疗法临床获益有限,患者具有迫切的临床治疗需求。
临床前数据显示,AP-L1898不仅保持了抑制T790M等EGFR常见变异的活性和对野生型EGFR的选择性,同时也克服了第三代EGFR抑制剂对exon 20插入等EGFR非常见突变的不敏感。因此,AP-L1898的开发有望给携带EGFR exon 20插入突变等EGFR非常见突变的肿瘤患者带来新的治疗方式。本次,AP-L1898胶囊获批两项临床默示许可,针对的适应症均为晚期非小细胞肺癌。
君实生物早前发布的公告显示,WJ01024片(项目代号“JS110”)是一种核输出蛋白XPO1的小分子抑制剂,拟用于治疗晚期肿瘤患者。
DNA损伤是癌细胞的典型特征之一。细胞中存在着一些肿瘤抑制蛋白,它们的作用是监控细胞核中DNA的状态,如果发现DNA出现损伤,它们可以介导DNA的修复或者导致细胞凋亡。然而,这些肿瘤抑制蛋白需要位于细胞核中才能正常发挥作用。癌细胞逃避肿瘤抑制蛋白监控的机制之一是通过过度表达一种名为XPO1的核输出蛋白。它可以将细胞核内的肿瘤抑制蛋白通过核孔运送到细胞核外,从而将肿瘤抑制蛋白从细胞核中清除。
临床前研究显示,作为一种在研XPO1抑制剂,WJ01024能特异性地阻断XPO1蛋白的功能,抑制包括p53在内的多种抑癌蛋白出核,加强抑癌蛋白功能。体外研究显示,WJ01024能抑制多种肿瘤细胞生长,诱发肿瘤细胞死亡。在肿瘤动物模型中,WJ01024单药或者联合用药均可抑制多种血液癌症和实体肿瘤的生长。这种独特的作用机制意味着,WJ01024的开发有望给晚期肿瘤病人带来一种全新的治疗手段。

除了上述两款药物,君实生物与微境生物的合作还包括另外两款在研抗肿瘤小分子药物。一款为口服小分子Aurora A抑制剂WJ05129,Aurora A抑制剂与RB1基因缺失或失活具有合成致死的效果,可以用于治疗小细胞肺癌和三阴乳腺癌等RB1缺失或失活的恶性肿瘤。另一款为WJ13404,这是一种第四代EGFR抑制剂。临床前数据显示,该候选药物分子不但对包括Del19/T790M/C797S和L858R/T790M/C797S在内的对第三代EGFR抑制剂不敏感的获得性EGFR变异有很好的抑制活性,而且对野生型EGFR也具有高度选择性。
根据君实生物与微境生物去年达成的合作协议,君实生物将获得微境生物这4款在研药物的50%权益,以及获批后在全球范围内的独家生产权、委托生产权及销售权。双方将按照协议共同推进上述药物的临床前研究工作,君实生物将负责进行临床试验申请。君实生物将向微境生物支付3600万元人民币首付款,并根据研发和商业化进度,向微境生物支付累计不超过4.36亿元人民币的里程碑付款。此外,君实生物还将向微境生物支付每个产品销售净利润50%的销售提成。
本次,AP-L1898胶囊和WJ01024片获批临床意味着,君实生物与微境生物的合作迎来了新的进展。期待这两款在研新药的后续临床试验顺利进行,早日惠及患者。
注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
[1]中国国家药监局药品审评中心(CDE).Retrieved Apr 25,2021, from http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=25
[2]君实生物与微境生物宣布就4款抗肿瘤小分子药物达成全球开发与商业化合作. Retrieved Sep 16, 2020, from https://www.junshipharma.com/News.html
[3]上海君实生物医药科技股份有限公司自愿披露关于 EGFR exon 20 插入等非常见突变抑制剂 JS111 获得药物临床试验申请受理通知书的公告. Retrieved Feb 24, 2021, from https://pdf.dfcfw.com/pdf/H2_AN202102231464538363_1.pdf?1614097212000.pdf
[4]上海君实生物医药科技股份有限公司自愿披露关于 XPO1 抑制剂 JS110 获得药物临床试验申请受理通知书的公告. Retrieved Feb 18, 2021, from https://pdf.dfcfw.com/pdf/H2_AN202102171462797925_1.pdf?1613579263000.pdf
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。







 个人中心
个人中心
 我是园区
我是园区




