2020 年 10 月 22 日,NMPA 发布批件,11 个品种通过一致性评价,其中包括两款注射剂「依诺肝素钠注射液」和「注射用帕瑞昔布钠」。除海南普利的注射用阿奇霉素以外,这是注射剂一致性评价落地以来,首次有注射剂品种以补充申请通过了一致性评价。
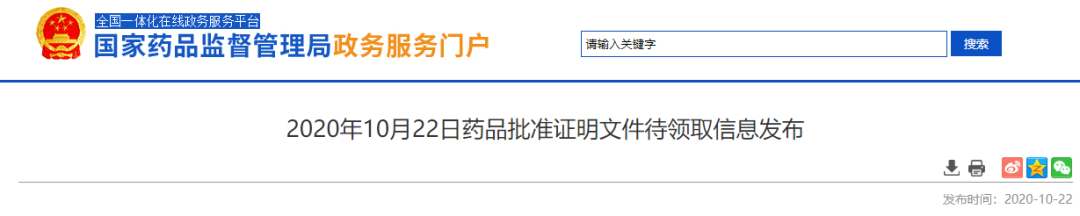

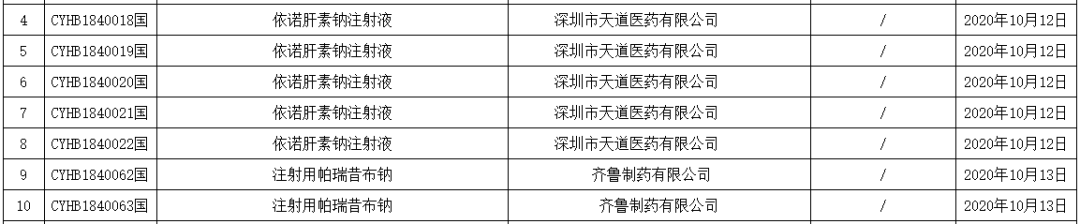
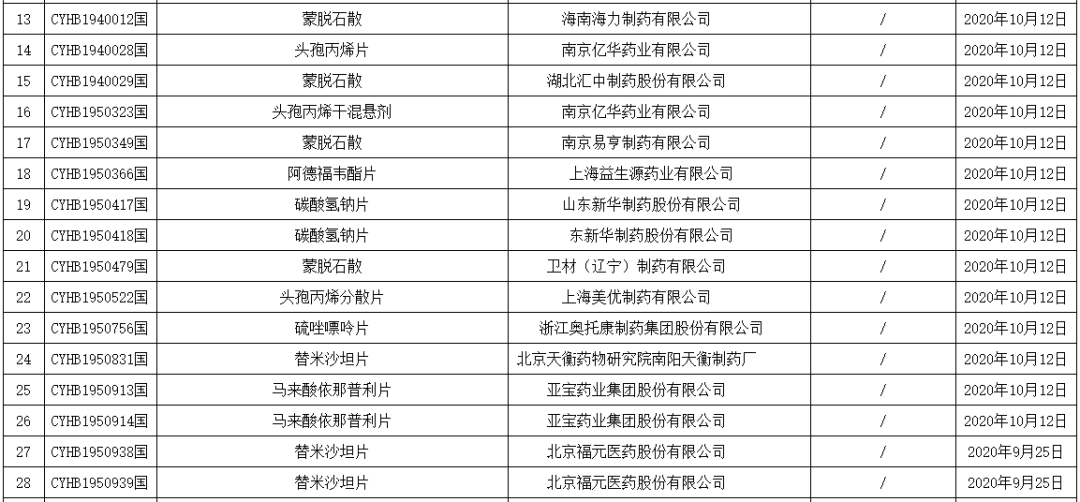
依诺肝素注射液,首家过评
依诺肝素钠注射液属于低分子肝素钠,可用于预防静脉血栓栓塞性疾病(预防静脉内血栓形成)。
公开数据显示,2018 年低分子在中国公立医疗机构终端的销售额为 87.32 亿元,同比增长 26.27%。目前国内市场上市销售的低分子肝素包括低分子量肝素钙注射液、依诺肝素钠注射液、那屈肝素钙注射液、达肝素钠注射液等。
目前,根据 Insight 数据库,包括原研企业赛诺菲在内,国内共 10 家企业生产销售依诺肝素注射液,共 7 家企业已提交一致性评价补充申请或新注册分类上市申请,但尚未有企业过评。本次深圳天道医药补充申请获批,意味着该品种迎来了首家过评;同时,注射剂也由此迎来了以补充申请通过一致性评价的新品种。
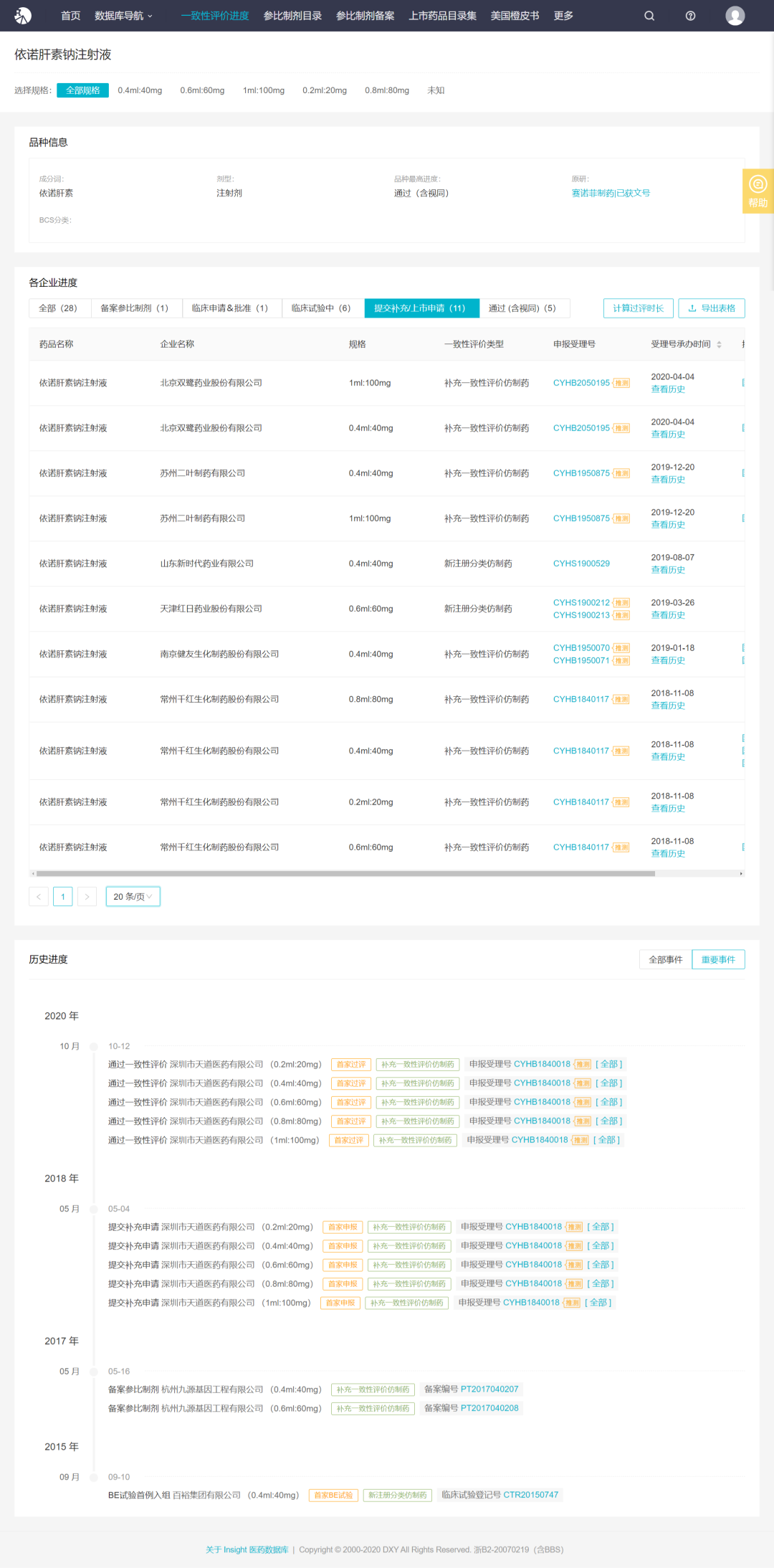
Insight 数据库一致性评价时光轴显示,天道医药于 2018 年 5 月 4 日提交补充申请,申请规格包括 0.2 ml:20 mg,0.4 ml:40 mg,0.6 ml:60 mg,0.8 ml:80 mg,1 ml:100 mg 共 5 个规格。本次这 5 个规格同时过评。
注射用帕瑞昔布钠
帕瑞昔布为选择性 COX-2 抑制剂,对 COX-2 具有高度抑制作用,通过降低前列腺素样递质的合成而达到抗炎镇痛的目的。该药既可达到抗炎镇痛的目的,又避免了抑制 COX-1 而导致的不良反应。可用于患者的术后轻、中度疼痛的镇痛,或中重度疼痛的多模式镇痛治疗。
Insight 数据库显示,目前该品种已有 3 家以新注册分类获批上市,并视同通过一致性评价,本次齐鲁过评后,成为该品种第 4 家过评。但以补充申请过评还属于首家。另外,截至当前,该品种已有 11 家企业递交了一致性评价补充申请,14 家企业递交了新注册分类上市申请,可谓是竞争激烈。
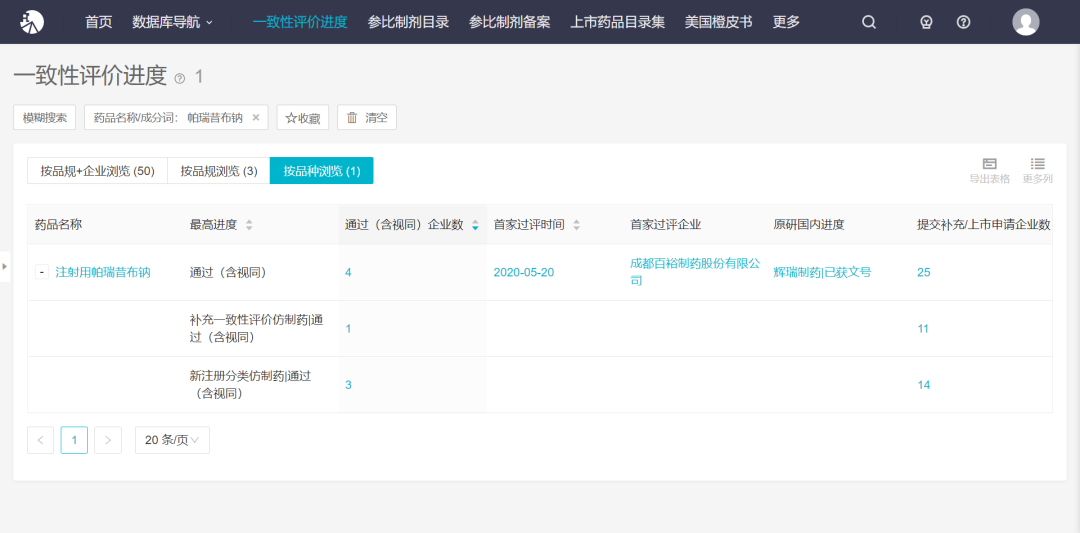
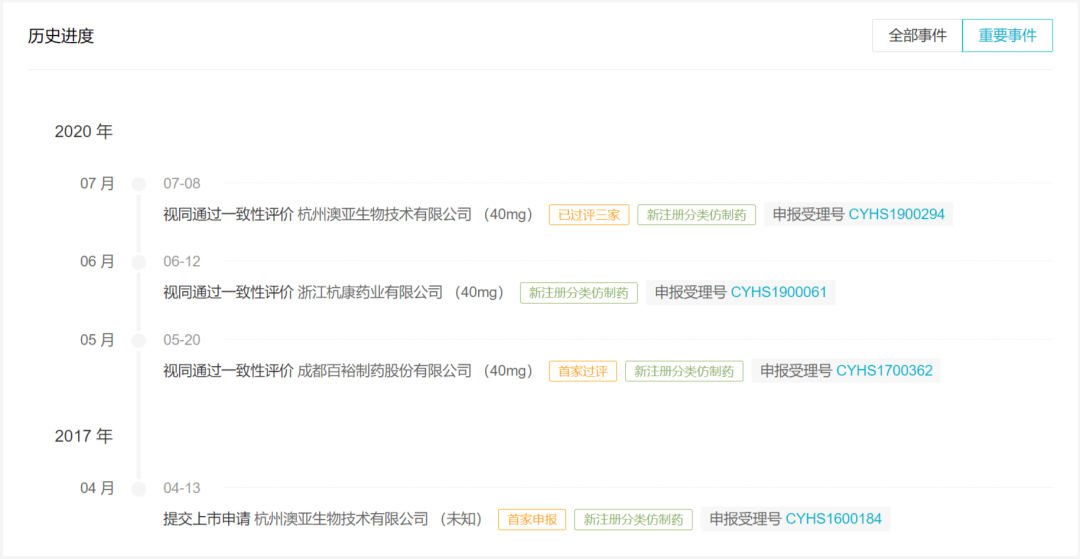
Insight 数据库一致性评价时光轴显示,该品种首家过评为成都百裕制药,于今年 5 月 20 日过评;至 7 月 8 日,该品种第三家过评,集齐三家。
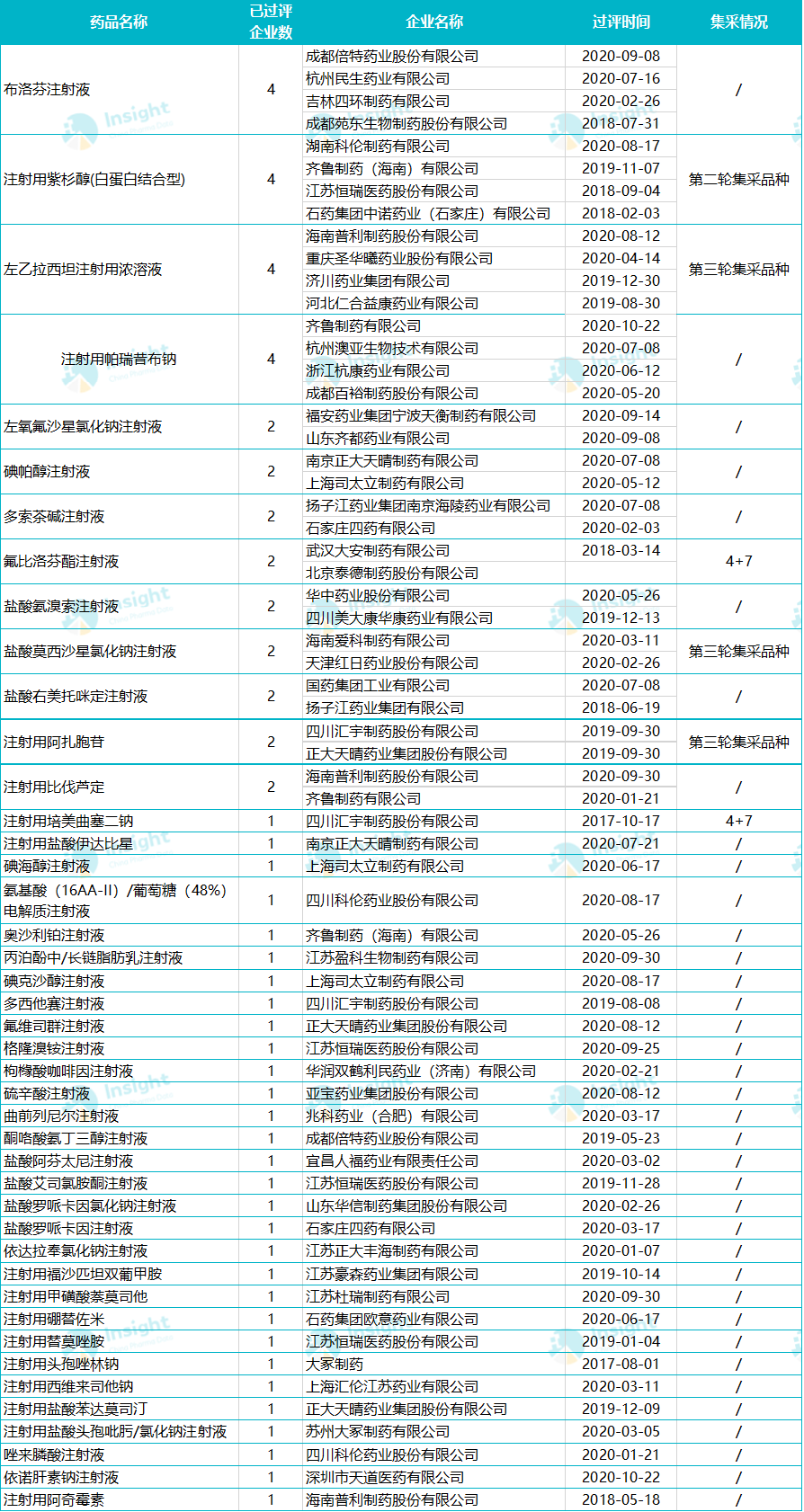
截至 10 月 22 日,已有 43 个注射剂品种过评。



 个人中心
个人中心
 我是园区
我是园区




