新冠疫情一轮又一轮肆虐,俨然已经成为了所有人生活中挥之不去的关键词之一。疫苗、中和抗体、小分子化药……药企和研究机构争分夺秒开发和迭代新药,以应对持续变化的疫情环境。
在已经过去的 2021 年度,辉瑞/BioNTech 的新冠疫苗以 367.8 亿美元的全球销售额荣登「药王」宝座,吉利德的瑞德西韦销售额也大涨 98%,收入 55.6 亿美元。随着 Paxlovid、Molnupiravir 等小分子药物的逐渐获批,其价值也将逐渐展现。 据 Insight 数据库,目前针对 COVID-19 的小分子化药开发在 3CLPRO、 RDRP 靶点密集扎堆,本文我们将简单概览 TOP 靶点们的研发进展。
全球在研 COVID-19 化药靶点分布情况
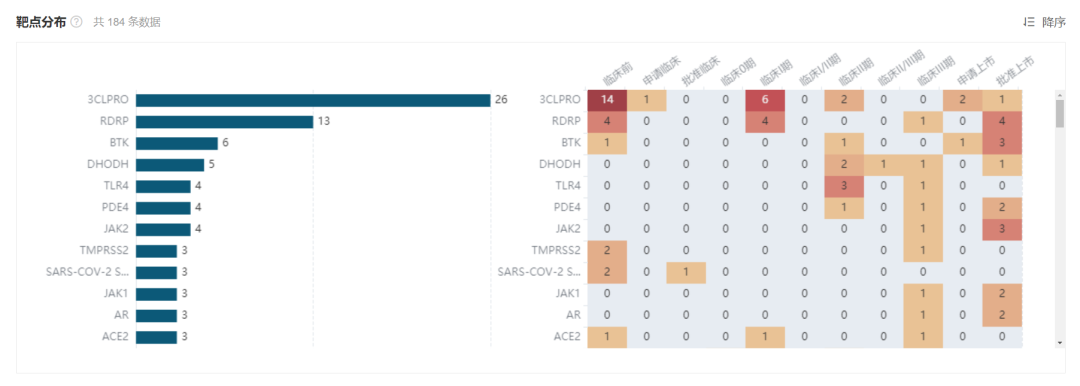
数据来自:Insight 数据库 全球新药(http://db.dxy.cn/v5/home/)
*仅筛选已有靶点披露的新药项目,不包括改良新和类似药/仿制药
3CL 蛋白酶
3CL 蛋白酶属于半胱氨酸蛋白酶,是新型冠状病毒复制必须的关键蛋白酶,且结构和功能较为保守,是抗新冠病毒小分子药物开发的重要靶点,相关小分子治疗药物具有效果好、广谱性、安全性好的优点。
这一靶点的典型代表是辉瑞的 PF-07321332,该成分与低剂量抗逆转录病毒药物利托那韦(Ritonavir)共同构成了口服复方制剂 Paxlovid 。Paxlovid 的疗效主要基于 3CL 蛋白酶抑制剂 PF-07321332 对新冠复制的抑制,利托那韦则用以减缓该成分的代谢或分解,使其在体内以更高浓度保持更长时间的活性。
3CLPRO 靶点新冠药物开发情况
Paxlovid 在去年 11 月公布了 2/3 期临床 EPIC-HR 研究数据,减少新冠肺炎非住院患者住院或死亡率 89%,一度引起轰动。12 月 22 日,美国 FDA 迅速对该药授予了 EUA 批准,用于高危成人和 12 岁及以上体重至少 40 公斤的高危儿科患者,这是该药全球首次获批;今年 2 月,国内 NMPA 也迅速批准 Paxlovid 进口。
尽管获批时间尚短,Paxlovid 已经成为业内乃至大众耳熟能详的重磅药物,其国内代理权、CMO 合作订单等都屡屡带来热议。这既基于 Paxlovid 突出疗效,也基于该药能给企业带来的极高收益。据辉瑞 2021 年报,预计 2022 年底将实现 1.2 亿疗程产能,实现超 220 亿美元的高收入。
据 Insight 全球新药库 显示,全球共 28 个 3CL 蛋白酶在研,除 Paxlovid 外,盐野义的 Ensitrelvir 也已经在日本提交了上市申请,另有 4 款药物处于临床 II 期开发,6 款药物处于临床 I 期开发。近期频繁的相关交易带来了早期临床前项目合作的不断涌现,15 个产品在临床前开发阶段,随时向临床试验发期冲击。
盐野义制药的 Ensitrelvir(S-217622)是仅次于辉瑞进度排位第 2 的 3CL 蛋白酶抑制剂,2022 年 2 月 25 日已经在日本提交上市申请。
据 Insight 数据库显示,Ensitrelvir 和其他新冠药物研发一样推进极快。盐野义在 2021 年 7 月启动了该药的 I 期临床(JPRN-jRCT2031210202),9 月启动 II/III 期临床(JPRN-jRCT2031210350),2022 年 3 月启动 III 期临床(NCT05305547)。盐野义表示,该药可单药给药,潜在疗效和安全性有望更优,公司已经推动 Ensitrelvir 的商业化生产,4 月份期实现 1000 万人份/年的产能。
而国内企业中,先声药业 2021 年 11 月与上海药物所合作引进了候选药物 SIM0417 ,在 2022 年 4 月 7 日启动 I 期临床;云顶新耀在今年 1 月超 2 亿美元从新加坡实验药物研发中心(EDDC)获得 EDDC-2214 的全球权益;君实生物合作苏州旺山旺水生物医药开发了 VV993;歌礼制药 ASC11 临床前数据也已公布,预计下半年递交 IND 申请……谁将脱颖而出成为首款上市来自中国药企的 3CL 蛋白酶抑制剂,让我们拭目以待。
RNA 聚合酶抑制剂排位仅次于 3CL 蛋白酶抑制剂,靶点为 RDRP(RNA-dependent RNA polymerase),以默沙东的 Molnupiravir、吉利德的瑞德西韦(Remdesivir)、君实生物/旺山旺水的 VV116 为典型代表。这三款药物目前已经获批上市,其中 VV116 获批于乌兹别克斯坦。
Molnupiravir
公布临床数据早于辉瑞的 Paxlovid,两者几乎前后脚获批,不过其光环似乎被 Paxlovid 夺走,此前中期分析数据和最终数据的差异使 FDA 举行了咨询委员会专家会议投票以决定是否批准,最终 Molnupiravir 以 13:10 的优势赢得了批准。
瑞德西韦
在疫情之初则表现出新冠疗效,2020 年 10 月就获 FDA 批准。2021 年度瑞德西韦已经成为吉利德销售榜首,增长 98% 达到 55.6 亿美元。
国内 VV116 是开发进展最快的新冠口服药物,该药由君实生物和中国科学院上海药物研究所、中国科学院武汉病毒研究所、中国科学院新疆理化技术研究所、中国科学院中亚药物研发中心/中乌医药科技城(科技部「一带一路」联合实验室)、旺山旺水共同研发。目前,VV116 的 I 期临床数据已经公布,III 期临床试验也完成了首例给药,日前还启动了一项头对头 Paxlovid 的 III 期临床试验,足以体现企业对该药的信心。
详细临床方案信息可查看:http://www.chictr.org.cn/showproj.aspx?proj=166475
据公开资料显示,
VV116 临床前在体内外都表现出显著的抗 SARS-CoV-2 作用,
对 SARS-CoV-2 原始株和已知重要变异
株(Alpha、Beta、Delta 和 Omicr
on)均表现出抗病毒活性,同时具有很高的口服生物利用度和良好的化学稳定性。
不过,同靶点其他药物针对新冠肺炎的适应症开发大多集中在临床前。
BTK
即布鲁顿氏酪氨酸激酶,
是 B 细胞受体(BCR)信号通路的关键调节因子, 参与 B 细胞的增殖、运输、趋化和粘附,在不同类型血液系统恶性肿瘤中广泛表达。目
前,BTK 抑制剂已经在血液瘤领域获得了广泛的批准和商业上的成功。同时,针对多发性硬化和肾病,药企也针对 BTK 抑制剂在做差异化的开发。
据 Insight 数据库 显示,全球有 6 款 BTK 抑制剂已经启动了针对新冠肺炎的临床试验,不过活跃期间均在 2020 年度。包括已经获批上市的 BTK 抑制剂泽布替尼(百济神州)、阿卡替尼(阿斯利康)和伊布替尼(强生制药),以及临床开发阶段的 M7583(默克)、DWP 212525(大熊制药),另外还包括另一款特殊的 BTK/EGFR 双靶点抑制剂艾维替尼 ,来自艾森医药(已被 Sorrento 收购)。
BTK 抑制剂开发新冠肺炎适应症主要是基于在肺巨噬细胞中 BTK 是产生多种细胞因子和趋化因子的关键调节因子,抑制 BTK 的活性则可减少这些细胞因子的产生,从而
成为减少 COVID-19 呼吸道并发症的一个有前景的策略。
不过,BTK 抑制剂针对 COVID-19 的开发并非一帆风顺,在 2021 年 4 月,百济神州宣布泽布替尼 用于新冠肺炎的 2 期临床试验 BGB-3111-219
(NCT04382586)
未能达到无呼吸衰竭生存或吸氧天数减少的并列主要有效性终点。这项研究起始于 2020 年 5 月,入组了 67 例需要辅助供氧或机械通气的新冠肺炎患者,旨在快速评估泽布替尼用于治疗出现呼吸窘迫新冠肺炎住院患者是否有效。
雄激素受体(AR)拮抗剂原本开发用于前列腺癌治疗,不过流行病学研究显示,成年女性重症率显著低于成年男性,且接受雄激素剥夺治疗(ADT)的患者重症率也有所降低,这为 AR 拮抗剂治疗新冠提供了最初证据。后续分子生物学研究又证实,雄激素可以调节两种人体细胞表面受体 ACE2 和 TMPRSS2 的表达,这些受体与新冠病毒的感染相关。
在 AR 拮抗剂治疗新冠肺炎的开发中,开拓药业走得最远,也吸引了最多期待值。普克鲁胺 是第二代雄激素受体(AR)拮抗剂,已经在多个国家和地区开展了多项 III 期临床试验,详见下图。
4 月 6 日开拓药业正式公布了普克鲁胺治疗轻中症非住院新冠患者 III 期全球多中心临床试验
(NCT04870606)
的关键数据结果
。
该研究是一项双盲、安慰剂对照(1:
1)、随机、全球多中心的注册性 III 期临床试验,自 2021 年 4 月 24 日开始全球首位受试者入组,于 2021 年 12 月 24 日完成全球 733 名受试者入组。
入组人群首次出现新冠症状不超过五天,且不排除风险因素和新冠疫苗接种。
结果显示,普克鲁胺可有效降低住院/死亡率,在完成服药大于 1 天的受试者中(N=721),对照组及普克鲁胺组的住院事件数分别为 7 例(含一例死亡)及 2 例(无死亡),相应保护率为 71%;在完成服药大于 7 天的受试者中 (N=693),对照组及普克鲁胺组住院事件数分别为 6 例(含一例死亡)及 0 例(p﹤0.02),相应保护率为 100%。
免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
投稿:微信 insightxb;邮箱 insight@dxy.cn
 戳此领取试用福利,解锁更多新功能!
戳此领取试用福利,解锁更多新功能!







 戳此领取试用福利,解锁更多新功能!
戳此领取试用福利,解锁更多新功能!



 个人中心
个人中心
 我是园区
我是园区




