2 月 22 日,Insight 数据库显示,复星医药的 PD-L1/FGFR 小分子抑制剂 FH-2001 首次公示启动临床试验(点此查看:CTR20220322),以评价 FH-2001 胶囊在晚期实体瘤患者中的安全性和耐受性,并确定 FH-2001 胶囊的最大耐受剂量(MTD)或 II 期推荐剂量(RP2D)。

来自:Insight 数据库(http://db.dxy.cn/v5/home/)
FH-2001 胶囊属于 PD-L1/FGFR 双机制小分子调节/抑制剂,该新药临床前研究主要由上海药明康德新药开发有限公司受托开展、临床研究及后续商业化拟由复星医药自主实施。据 Insight 数据库显示,在 2021 年 6 月该药首次提交临床试验申请,9 月获批临床,今日首次启动临床。
FH-2001 项目时光轴

随着 PD-1/L1 竞争白热化,药企已在探索相关靶点的差异化开发方向,挖掘更多价值。已有多家企业开发 PD-1/L1 抗体皮下注射剂,典型例子就是首款获批的国产 PD-L1 单抗恩沃利单抗,众多 PD-1 主要企业们也投身此领域的研发(Insight 往期报道:PD-(L)1 产品新战场);在单抗之外,国内企业还在开发双抗和双功能融合蛋白,以期实现「1+1>2」的疗效和安全性;小分子化药的开发也如火如荼,作为口服药有望提高依从性,同时兼具成本优势。
从 Insight 数据库 反映的申报趋势来看,无论是双抗还是小分子,在 2021 年均达到了一个高峰,甚至翻倍不止。17 款 PD-L1 相关双抗、3 款 PD-L1 小分子抑制剂在这一年首次申报临床。2022 年 1 月,贝达药业和和誉医药又先后申报了 PD-L1 小分子。
PD-L1 靶点创新药新项目趋势

来自 Insight 数据库(http://db.dxy.cn/v5/home/)
目前国内 PD-L1 小分子抑制剂已有 6 款进入临床。此外根据已公开专利信息,还有多家企业处于临床前研发阶段,包括微芯生物、歌礼制药、东阳光药、圣和药业等。歌礼制药在今年 1 月已经向美国 FDA 递交了 IND 申请。
国内临床阶段 PD-L1 小分子抑制剂

来自 Insight 数据库(http://db.dxy.cn/v5/home/)
红日药业:艾姆地芬
艾姆地芬(研发代号:IMMH-010)是国内首款进入临床阶段的 PD-L1 小分子抑制剂,在 2020 年上半年就已经启动了 I 期临床(登记号:NCT04343859 / CTR20200381)。
临床试验详情

来自 Insight 数据库(http://db.dxy.cn/v5/home/)
红日药业从中国医学科学院引进了这款新药,2017 年 5 月双方签订了正式项目合作开发协议,随即进行申报前的药学、药理毒理的研究;2019 年 7 月申报 IND,同年11 月取得临床批件。
再极医药:MAX-10181
再极医药的 MAX-10181 是国内第二款申报临床的 PD-L1 小分子抑制剂,2021 年 2 月首次在国内获批临床,用于晚期实体瘤。MAX-10181 启动临床时间较早,于 2019 年 10 月就已经在澳洲开始 I 期临床试验。目前,MAX-10181 已经启动了两项临床试验:
MAX-10181 临床试验卡片

来自 Insight 数据库(http://db.dxy.cn/v5/home/)
在 2019 年美国癌症研究协会的年会(AACR)上,再极医药曾公布了 MAX-10181 在人源化的肿瘤模型中与阿斯利康 PD-L1 度伐利尤单抗的头对头比较数据(摘要:LB-018)。在两次试验中,MAX-10181 与度伐利尤单抗都表现出相同的 MC38 肿瘤抑制活性,同时 MAX-10181 表现出了更高的 CD8+/Treg 比值(p<0.01)。
阿诺生物:AN4005
2021 年 5 月 20 日,阿诺医药宣布已向美国 FDA 递交了其原创新药口服 PD-L1 抑制剂 AN4005 的临床试验申请(IND),并将在美国启动安全性和药代动力学评估的临床 Ⅰ 期试验;10 月,阿诺医药在中国提交 AN4005 的临床试验申请,并于 12 月获批临床。
AN4005 I 期临床试验卡片

来自 Insight 数据库(http://db.dxy.cn/v5/home/)
作为一款口服活性的特异性 PD-L1 拮抗剂,AN4005 在临床前显示出强大的抗肿瘤活性。AN4005 可有效诱导和稳定 PD-L1 二聚体的形成及二聚化,从而有力地破坏 PD-1/PD-L1 蛋白质间的相互作用。与已获批上市的 PD-(L)1 抗体相比,AN4005 表现出相当的体外和体内活性。作为针对多种实体瘤的小分子药物,AN4005 在单药治疗以及组合用药方面都有着巨大的潜力。
作为单克隆抗体的替代品,小分子 PD-(L)1 抑制剂在肿瘤免疫治疗领域逐渐吸引了更多的关注。相较于单克隆抗体,小分子 PD-(L)1 抑制剂有望带来更大的益处,如口服给药可改善患者的依从性;小分子相对于抗体半衰期较短,使得与免疫相关的不良反应可以得到更好地控制;小分子的灵活性在接下来的联合疗法中将发挥便捷有效的特点。
截至目前,全球尚无获批或已上市的 PD-(L)1 小分子抑制剂。
阿诺医药全球研发负责人何南海曾在采访中提出肿瘤免疫鸡尾酒疗法构想,其中 AN4005 作为口服 PD-L1 抑制剂,有望成为这一构想的基石用药,增加 T 细胞的肿瘤杀伤作用,联合管线中其他产品解除免疫抑制。相关产品还包括 TNFR2 抑制剂 AN3025、HPK1 抑制剂 AN6025 等。
贝达药业:BPI-371153
据 Insight 数据库 显示,贝达药业的 PD-L1 小分子抑制剂 BPI-371153 于 2021 年 11 月首次在国内申报临床,今年 1 月份获批临床,拟用于局部晚期或转移性实体瘤或复发/难治性淋巴瘤患者的治疗。

BPI-371153 由贝达自主研发,拥有全球权益。临床前研究显示,高剂量 BPI-371153 的体内抗肿瘤活性较 PD-L1 单抗度伐利尤单抗更强,显著缩小肿瘤体积。

不仅 PD-L1 小分子抑制剂,贝达药业去年还曾引进了 PD-1 单抗巴替利单抗和 CTLA-4 单抗泽弗利单抗,在主要优势领域肺癌之外,拓展在其他肿瘤领域的新药管线。
和誉医药:ABSK043
去年 6 月,和誉医药在海外启动了一项 PD-L1 小分子抑制剂 ABSK043 的 I 期临床试验;今年 1 月 24 日,和誉医药首次在国内递交该药的临床试验申请(受理号:CXHL2200042)。
ABSK043 I 期临床试验卡片

来自 Insight 数据库(http://db.dxy.cn/v5/home/)
据和誉医药新闻稿,ABSK043 是一款全新的口服和具备优异活性及选择性的小分子 PD-L1 抑制剂,可与 PD-L1 特异性结合并诱导其从细胞表面内吞,有效地抑制 PD-1/PD-L1 的相互作用,恢复 PD-L1 介导的 T 细胞活化抑制。该药已在多个临床前模型中展现出与已获批 PD-L1 抗体相当的强大抗肿瘤功效。
和誉医药的肿瘤免疫管线主要聚焦在小分子领域,靶点布局覆盖了 CSF-1R、CXCR4、PD-L1、CD73 和 RORγt。相较于内卷严重的抗体药领域,小分子肿瘤免疫药物的竞争相对缓和,或许代表着更多机会。
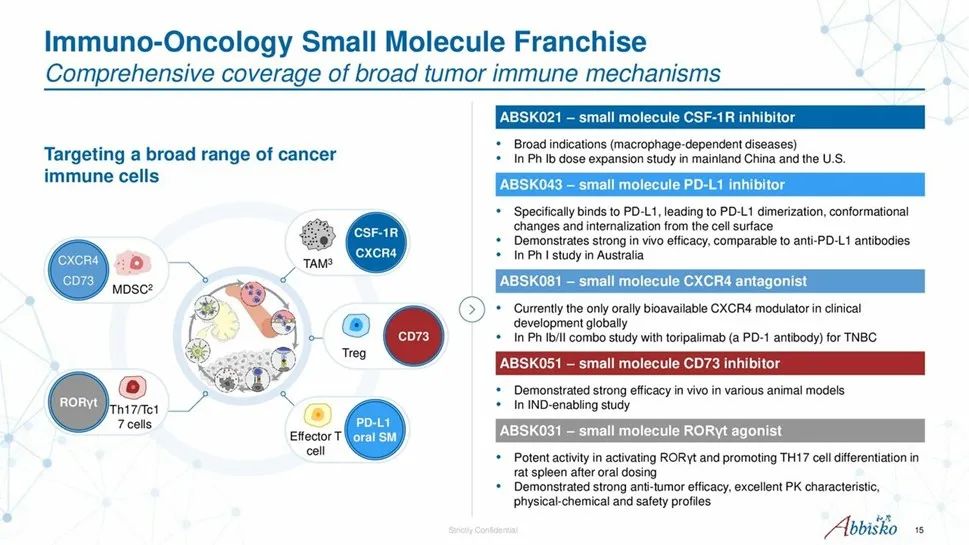
来自:和誉医药 2022JPM PPT
编辑:加一
PR 稿对接:微信 insightxb
投稿:微信 insightxb;邮箱 insight@dxy.cn
点击卡片进入 Insight 小程序
药品申报、临床、上市、一致性评价…
随时随地查!
↓↓ 点击解锁更多新功能



 个人中心
个人中心
 我是园区
我是园区




